1. Запишите уравнения реакций между алюминием и следующими веществами:
а) раствором гидроксида натрия;
б) расплавом гидроксида натрия;
в) соляной кислотой;
г) концентрированной фтороводородной кислотой.
2. Запишите уравнения реакций, при помощи которых можно осуществить следующие превращения:
AlCl3  Na3[Al(OH)6]
Na3[Al(OH)6]  Al(OH)3
Al(OH)3  Al
Al  AlCl3
AlCl3 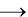 Al(OH)3
Al(OH)3 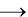 Al2O3.
Al2O3.
Укажите условия протекания реакций.
3. Запишите уравнения реакций между следующими веществами:
а) алюминием и оксидом железа (III);
б) хлоридом алюминия и гидридом лития;
в) оксидом алюминия и серной кислотой.
4. При полном растворении алюминия в 500 г раствора гидроксида натрия выделилось 33,6 л водорода, при этом образовался тетрагидроксоалюминат натрия. Вычислите массовую долю вещества в полученном растворе.
Ответ: w(Na[Al(OH)4]) =0,23.
5. При прокаливании природного соединения, содержащего 70 % (масс.) гидроксида алюминия образовалось 102,0 г оксида алюминия. Определите массу исходного соединения.
Ответ: m(соединения) = 222,9 г.
5. Элементы триады железа – железо, кобальт, никель
 2014-02-02
2014-02-02 1075
1075








