1. Запишите уравнения реакций между железом и следующими веществами:
а) разбавленной соляной кислотой;
б) концентрированной серной кислотой;
в) оксидом углерода (II);
г) серой.
2. Запишите уравнения реакций, при помощи которых можно осуществить следующие превращения:
Fe 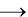 FeCl2
FeCl2 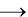 Fe(OH)2
Fe(OH)2 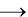 Fe(OH)3
Fe(OH)3 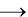 Fe2O3
Fe2O3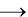 K2FeO4.
K2FeO4.
Укажите условия протекания реакций.
3. Запишите уравнения реакций между следующими веществами:
а) оксидом никеля (II) и соляной кислотой;
б) гидроксидом кобальта (II) и концентрированным раствором гидроксида натрия;
в) гидроксидом железа (II) и кислородом;
г) гидроксидом никеля (II) и избытком раствора аммиака.
4. Вычислите количество железа (в кг), которое можно получить из 1 тонны пирита, содержащего 80 % FeS2.
Ответ: m(FeS2) = 373,3 кг
 2014-02-02
2014-02-02 1618
1618