Реакции 9 и 10 выглядят, как тримолекулярные, или как реакции третьего порядка. В водной забуференной среде, однако, концентрация протонов постоянна, и эту величину можно включить в постоянную - константу скорости k9. Поэтому мы будем рассматривать реакцию 9 как бимолекулярную с константой скорости второго порядка k9. Также и концентрация субстрата окисления LH внутри мембраны достаточно велика и мало изменяется во времени, поэтому и реакцию 10 можно рассматривать как бимолекулярную (второго порядка) с константой скорости kp. После этого введения, запишем дифференциальные уравнения кинетики, описывающие скорости приведенных выше частных (или парциальных) реакций цепного окисления липидов:
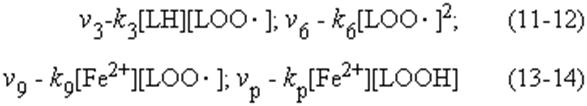
Дифференциальные уравнения, описывающие изменение концентраций основных участников реакции с учётом уравнений, приведенных выше, можно записать так:
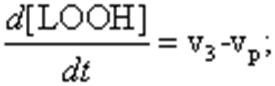 (15)
(15)
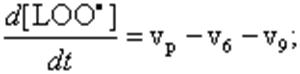
(16)
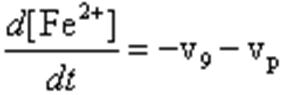
(17)
 2014-02-03
2014-02-03 364
364








