Индикаторы окислительно-восстановительного титрования
Классификация индикаторов ОВ титрования. В титриметрических редокс-методах определяют КТТ индикаторным методом. При этом роль индикатора может играть либо сам реагент, участвующий в ОВ реакции, либо специально вводимый индикатор. В соответствии с этим индикаторы, применяемые в редоксметрии, можно классифицировать следующим образом.
Индикатор — реагент, участвующий в ОВ реакции. Примером может служить раствор титранта — перманганата калия KMnO4 в перманганатометрии. Раствор перманганата калия обладает интенсивной малиново-фиолетовой окраской, поэтому первая же капля избыточного титранта после ТЭ окрашивает титруемый раствор в розово-малиновый цвет. Титрование оканчивают при появлении устойчивой розово-малиновой окраски раствора.
Примером может служить свежеприготовленный раствор крахмала, который в присутствии иода окрашивается в синий цвет.
Другой пример — тиоцианат-ионы NCS‾, используемые в качестве индикатора при титровании железа(III), с которым они образуют комплексы, окрашенные в интенсивно-красный цвет. Так. при титровании железа(III) титрантом, содержащим титан(III), протекает реакция
Fe3+ + Ti3+ = Fe2+ + Ti4+
В исходный титруемый раствор прибавляют тиоцианат аммония или калия, поэтому раствор имеет красный цвет за счет образования тиоцианатных комплексов железа(III). В процессе титрования железо(III) переходит в железо(II). В ТЭ железо(III) уже отсутствует, поэтому в ТЭ красная окраска раствора исчезает.
Индикатор — вещество, которое при определенном потенциале раствора окисляется или восстанавливается с изменением окраски. Такие индикаторы называют редокс-индикаторами, или окислительно-восстановительными индикаторами. Другими словами, редокс-индикаторы — это индикаторы, способные окисляться или восстанавливаться с изменением окраски в ТЭ или вблизи ее.
Окислительно-восстановительные индикаторы бывают о6ратимыми и необратимыми. Обратимые индикаторы меняют окраску обратимо при потенциале раствора в ТЭ или вблизи ее и при этом не разрушаются. Необратимые индикаторы изменяют окраску при достижении определенного значения потенциала в ТЭ или вблизи ее и при этом необратимо разрушаются.
Обратимые редокс-индикаторы. Окисленная и восстановленная формы индикатора имеют различную окраску. Изменение цвета индикатора происходит при определенном значении потенциала раствора.
Полуреакцию, соответствующую изменению окраски редокс-индикатора, можно представить в виде
Indoх, + пе = Ind red,
где Indoх, Ind red — соответственно окисленная и восстановленная формы индикатора.
ОВ потенциал Е редокс-пары Indoх½Ind red описывается уравнением Нернста, которое для комнатной температуры можно представить в виде
| Е = Еo+ | 0,059 | lg | [Indox] |
| n | [Indred] |
где E ° ‑ стандартный ОВ потенциал данной редокс-пары.
Как и для кислотно-основных индикаторов, полагают, что при приблизительно одинаковой интенсивности окраски обеих форм индикатора человеческий глаз воспринимает окраску раствора той формой индикатора, концентрация которой примерно в 10 раз больше концентрации другой формы того же индикатора, т.е. при Indoх½Ind red = 10 раствор принимает окраску окисленной формы индикатора, а при Indoх½Ind red - 0,1 раствор окрашивается в цвет восстановленной формы индикатора. Следовательно, окраске окисленной формы индикатора соответствует потенциал раствора
| Е ³ Е°+ | 0,059 | lg10 = E° + | 0,059 |
| n | n |
а окраске восстановленной формы — потенциал раствора
| Е ≤Е°+ | 0,059 | lg0,1 = E° ‑ | 0,059 |
| n | n |
Объединяя оба эти выражения, получаем для интервала изменения окраски редокс-индикатора (интервала перехода) приближенно:
| Е =Е° ± | 0,059 |
| n |
т.е. окраска индикатора изменяется в пределах изменения потенциала раствора от Е° + 0,059/n В до Е° ‑ 0,059/n В. Наиболее резкое изменение окраски наблюдается при равенстве концентраций обеих форм, т.е. при значении потенциала раствора, равного
| Е =Е° ± | 0,059 | lg 1 = Е° |
| n |
Известно большое число обратимых редокс-индикаторов. В табл. 4.1 охарактеризованы в качестве примера некоторые ОВ индикаторы.
Одним из первых предложенных обратимых редокс-индикаторов является дифениламин С6Н5—NH—С6Н5. Полагают, что в присутствии окислителей дифениламин претерпевает в растворе превращения в соответствии с полуреакцией
| 2С6Н5—NH—С6Н5 ® С6Н5—NH—С6Н4‑С6Н4—NH—С6Н5+ 2Н+ + 2 е | ||
| дифениламин бесцветный | дифенилбензидин бесцветный |
Формулы выведены для случаев, когда в ОВ реакции не участвуют ионы водорода, а стехиометрические коэффициенты восстановленной и окисленной форм редокс-пар в соответствующих полуреакциях равны единице. В более сложных ситуациях логическая схема вывода формул для расчета индикаторных ошибок остается прежней, хотя сами расчеты становятся более громоздкими.
В практике фармацевтического анализа, когда индикаторная ошибка составляет сотые доли процента или еще меньше, ею обычно пренебрегают.
Считается возможным использование редокс-индикатора для фиксации КТТ тогда, когда индикаторная ошибка титрования с применением этого индикатора не превышает 0,1—0,2%.
Таблица 4.1.
Некоторые окислительно-восстановительные индикаторы
| Индикатор | Е°, В | Цвет формы индикатора | |
| окисленная | восстановленная | ||
| Нейтральный красный | -0,325 (рН 7) 0,240 (рН 0) | красный | бесцветный |
| Индигокармин | -0,125 (рН 7) 0,291 (рН 0) | синий | » |
| Метиленовая синяя | 0,011 (рН 7) 0,532 (рН 0) | » | » |
| Толуиленовый синий | 0,115(рН7) 0,601 (pHO) | » | » |
| Вариаминовый синий | 0,71 | фиолетовый | » |
| Дифениламин | 0,76 | » | бесцветный |
| Дифенилбензидин | 0,76 | » | » |
| п-Этоксихризоидин | 0,76 | бледно-желтый | красный |
| Дифениламин-4-сульфоновая кислота | 0,84 | сине-фиолетовый | бесцветный |
| N-Фенилантраниловая кислота | 1,00 | фиолетовый | » |
| Ферроин | 1,06 | бледно-голубой | красный |
| Нитроферроин | 1,25 | » | » |
Эта стадия необратима. Образовавшийся бесцветный дифенилбензидин затем обратимо окисляется по схеме
| С6Н5—NH—С6Н4‑С6Н4—NH—С6Н5 ⇆ |
| дифенилбензидин бесцветный |
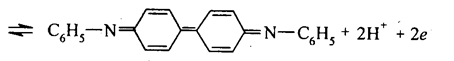
дифенилдифенохинондиимин фиолетовый
с образованием окисленной окрашенной фиолетовой формы индикатора (В присутствии нитрат-ионов в кислой среде раствор окрашивается в синий цвет). Интервал перехода окраски индикатора изменяется в пределах Е = 0,76 ± 0,0295 В.
Таким образом, собственно обратимым редокс-индикатором является не дифениламин, а дифенилбензидин, обратимо переходящий в дифенилдифено-хинондиимин.
К недостаткам дифениламина как редокс-индикатора относится его малая растворимость в воде (обычно готовят его 1%-ный раствор в концентрированной серной кислоте).
В качестве редокс-индикатора применяют также N-фенилантрониловую кислоту (2-дифениламинкарбоновую кислоту):
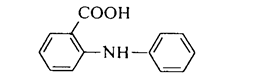
окисленная форма которой имеет фиолетово-красную окраску. Интервал (потенциал) перехода составляет Е = 1,00 ± 0,059 В. В отличие от дифениламина N-фенилантраниловая кислота растворяется в воде, поэтому обычно готовят ее 0,2%-ный водный раствор или же 0,1%-ный раствор в 0,2%-ном растворе соды.
Индикатор ферроин представляет собой комплекс железа(II) с ортофенан-тролином состава [FеL3]2+, где L — молекула ортофенантролина (1,10-фенантролина)
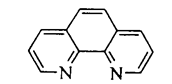
Ферроин обратимо претерпевает окислительно-восстановительное превращение
[FеL3]3+ + е = [FеL3]2+
окисленная форма восстановленная форма
(бледно-голубая) (красная)
Интервал (потенциал) перехода составляет Е = 1,06 В. Ферроин как редокс-индикатор обладает целым рядом достоинств: его растворы стабильны; окисленная форма индикатора устойчива по отношению к действию сильных окислителей; он проявляет резкое изменение окраски, которое осуществляется быстро и обратимо; допускает титрование при нагревании вплоть до ~60 °С.
Обычно раствор этого индикатора готовят, смешивая 1,624 г гидрохлорида фенантролина и 0,695 г FeSO4 • 7Н2`О в 100 мл воды.
Необратимые ОВ индикаторы. К индикаторам этой группы относятся метиловый оранжевый, метиловый красный, нейтральный красный. При потенциале раствора, равном потенциалу, а в ТЭ, они необратимо окисляются, вследствие чего исчезает присущая им окраска раствора.
Другая классификация индикаторов ОВ титрования. Кроме рассмотренной выше предложена также следующая классификация индикаторов ОВ титрования:
1. Индикаторы группы соединений дифениламина и дифенилбензидина.
2. Индикаторы группы трифенилметановых и других красителей.
3. Хелатные комплексы дииминжелеза.
4. Индикаторы особого (специфического) действия.
5. Необратимые индикаторы, подвергающиеся деструкции.
6. Различные другие соединения.
7. Смешанные индикаторы.
 2014-02-03
2014-02-03 5341
5341
