А. По функции
Денатурация
Это разрыв связей, стабилизирующих четвертичную, третичную, вторичную структуры.
1. Физическая: повышение температуры, ультрафиолетовое и микроволновое излучение, механические воздействия, ионизация заряженными частицами.
2. Химическая:
Кислоты и щелочи образуют водородные связи с пептидными группами
Органические растворители образуют водородные связи и вызывают дегидратацию
Алкалоиды и тяжелые металлы образуют связи с полярными группами и разрывают систему водородных и ионных связей.
Коллоидные свойства:
1. Рассеивание луча света, проходящего через белковый раствор – эффект Тиндаля (светящийся конус)
2. Малая скорость диффузии
3. Неспособность проникать через полунепроницаемые мембраны
Например, работа искусственной почки, диализ.
4. Создание онкотического давления, то есть перемещение воды в сторону более высокой концентрации белка.
Например, формирование отеков.
5. Высокая вязкость – силы сцепления между молекулами.
Например, образование гелей и студней.
См выше "Функции белков"
1. По форме молекулы:
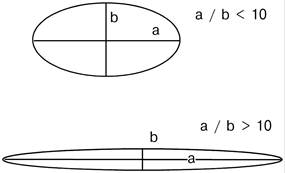 Глобулярные – соотношение продольной и поперечной осей составляет <10 и в большинстве случаев не более 3‑4. Они характеризуются компактной укладкой полипептидных цепей. Например: инсулин, альбумин, глобулины плазмы крови.
Глобулярные – соотношение продольной и поперечной осей составляет <10 и в большинстве случаев не более 3‑4. Они характеризуются компактной укладкой полипептидных цепей. Например: инсулин, альбумин, глобулины плазмы крови.
Фибриллярные – соотношение осей >10. Они состоят из пучков полипептидных цепей, спиралью навитых друг на друга и связанные между собой поперечными ковалентными и водородными связями. Выполняют защитную и структурную функции.
Например: кератин, миозин, коллаген, фибрин.
 2014-02-03
2014-02-03 1001
1001








