B-структура
 |
В этом способе укладки белка его молекула вытянута, пептидные группы аминокислот взаимодействуют с отдаленными пептидными группами той же цепи, или же с другими цепями (числом от 2 до 5). Ориентация цепей может быть параллельна или антипараллельна.
Это взаимная укладка областей и отдельных аминокислотных остатков полипептидной цепи. Четкой границы между вторичной и третичной структурами провести нельзя, однако под третичной структурой понимают стерические взаимосвязи между аминокислотами, отстоящими далеко друг от друга в цепи. Благодаря третичной структуре происходит еще более компактное формирование цепи.
Наряду с a-спиралью и b-структурой в третичной структуре обнаруживается так называемая неупорядоченная конформация, которая может занимать значительную часть молекулы. В разных белках наблюдается разное соотношение типов структур.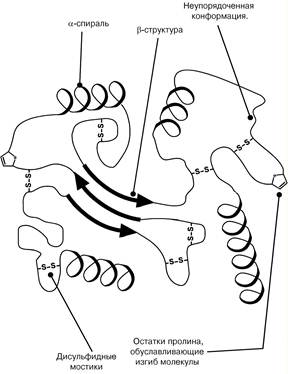
Например, инсулин содержит 52% a-спирали и 6% b-структуры, трипсин содержит 14% a-спирали и 45% b-структуры.
В формировании третичной структуры принимают участие различные связи:
1. В основном:
водородные
ван-дер-ваальсовы
2. Как дополнительные, но не менее значимые:
дисульфидные
псевдопептидные
ионные
 2014-02-03
2014-02-03 951
951








