Вторичная структура
Это способ укладки полипептидной цепи в упорядоченную структуру, при которой аминокислоты взаимодействуют через пептидные группы. Формирование вторичной структуры вызвано стремлением пептида принять конформацию с наибольшим количеством водородных связей между пептидными группами. Вторичная структура определяется:
устойчивостью пептидной связи
подвижностью С-С связи
размером аминокислотного радикала.
Все это вкупе с аминокислотной последовательностью приводтт к строго определенной конфигурации белка.
Можно выделить два возможных варианта вторичной структуры: a-спираль и b‑складчатый слой. В одном белке, как правило, присутствует и a-спираль и b-структура (складчатый слой). В глобулярных белках преобладает a-спираль, в фибриллярных – b-структура.
Правозакрученная спираль, образуется при помощи водородных связей между пептидными группами 1-го и 4-го, 4-го и 7-го, 7-го и 10-го аминокислотных остатков.
Формированию спирали препятствуют пролин и гидрооксипролин, которые обуславливают “перелом” цепи, ее резкий изгиб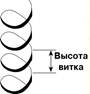 .
.
Высота витка составляет 0,54 нм и соответствует 3,6 аминокислотных остатков, 5 витков соответствуют 18 аминокислотам и занимают 2,7 нм.
 2014-02-03
2014-02-03 1428
1428








