Молекулярные спектры, в отличие от атомных спектров, обусловлены:
1) электронными переходами;
2) колебаниями атомов в молекуле;
3) вращением молекулы как целого.
В зависимости от этого различают электронные, колебательные и вращательные молекулярные спектры.
Энергия молекулы (Е) складывается из энергии движения электронов (Еэл), энергии колебания атомов (Екол) в молекуле и энергии вращения молекулы как целого(Евр):
Е = Е эл + Е кол + Е вр,
причём
Е эл >> Е кол >> Е вр.
Поэтому электронные спектры наблюдаются в более высокоэнергетических областях спектрального диапазона, а колебательные и вращательные спектры – в области более низких энергий внешнего излучения (табл.5).
Таблица 5
Виды молекулярных спектров поглощения
| УФ | vis | ближняя ИК | средняя ИК | дальняя ИК | микроволны |
| Электронные спектры | |||||
| Колебательные спектры | |||||
| Вращательные спектры | |||||
| ® уменьшение Е ® уменьшение ν ® увеличение λ |
Происхождение молекулярных спектров поглощения
и их использование в аналитической химии
Вращательные спектры возникают при изменении Евр под действием внешнего излучения. Они имеют линейчатый вид, причём линии равноудалены на расстояние 2В, где В – вращательная простоянная (рис.42).
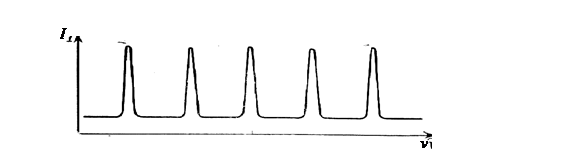
Рис. 41. Вращательный спектр.
Применение вращательных спектров: по значениям В и 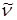 можно определять межъядерные расстояния, силовые константы. В аналитической химии эти спектры применяются редко.
можно определять межъядерные расстояния, силовые константы. В аналитической химии эти спектры применяются редко.
Колебательные спектры. Изменение Е кол под действием внешнего излучения сопровождается изменением Е вр, поскольку Е кол >> Е вр. В результате вместо чисто колебательных переходов у молекулы наблюдаются колебательно–вращательные переходы. При этом колебательная спектральная линия превращается в полосу, состоящую из множества линий:

|
|

|
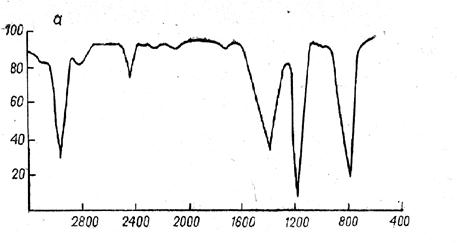
Рис. 42. Колебательный спектр.
Колебательные спектры применяются:
§ для качественного анализа по положению ПП. Это очень надёжный метод идентификации веществ, поскольку колебательные спектры различных веществ так же индивидуальны, как отпечатки пальцев у людей. Их так и называют «finger prints»;
§ для количественного анализа – реже из-за низкой точности и необходимости работать в области высоких концентраций.
Электронные спектры. При изменении Е эл у молекулы одновременно изменяются Е кол и Е вр, поскольку Е эл >> Е кол >> Е вр. В результате вместо чисто электронных переходов наблюдаются электронно–колебательно-вращательные переходы. Их число весьма велико, поэтому электронный спектр имеет вид широких перекрывающихся полос, которые возникают в результате наложения большого числа узких полос (рис. 43)
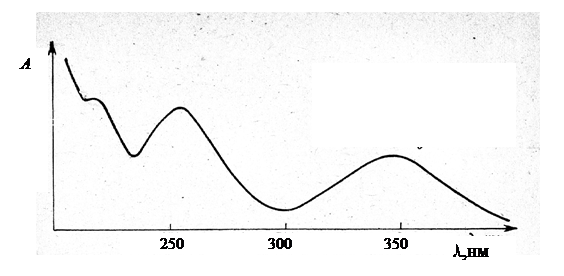
Рис. 43. Электронный спектр.
Электронные спектры применяются:
§ для качественного анализа – редко, т. к. ПП очень широкие. Но многие органические вещества можно идентифицировать по положению полос в УФ и vis областях (бензол, нафталин, пиридин, витамины А, В12 и т. д.).
§ для количественного анализа – очень точный и надёжный метод.
 2014-02-13
2014-02-13 5943
5943








