Работа в термодинамике, так же как и в механике, определяется произведением действующей на рабочее тело силы на путь ее действия. Рассмотрим газ массой М и объемом V, заключенный в эластичную оболочку с поверхностью F (рисунок 2.1). Если газу сообщить некоторое количество теплоты, то он будет расширяться, совершая при этом работу против внешнего давления р, оказываемого на него средой. Газ действует на каждый элемент оболочки dF с силой, равной pdF и, перемещая ее по нормали к поверхности на расстояние dn, совершает элементарную работу pdFdn.
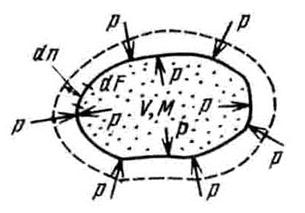
Рис. 2.1 – К определению работы расширения
Общую работу, совершенную в течение бесконечно малого процесса, получим, интегрируя данное выражение по всей поверхности F оболочки:
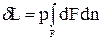 .
.
Из рисунок 2.1 видно, что изменение объема dV выражается в виде интеграла по поверхности: 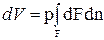 , следовательно
, следовательно
δL = pdV. (2.14)
При конечном изменении объема работа против сил внешнего давления, называемая работой расширения, равна
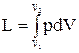 . (2.15)
. (2.15)
Из (2.14) следует, что δL и dV всегда имеют одинаковые знаки:
если dV > 0, то и δL > 0, т.е. при расширении работа тела положительна, при этом тело само совершает работу;
если же dV < 0, то и δL< 0, т. е. при сжатии работа тела отрицательна: это означает, что не тело совершает работу, а на его сжатие затрачивается работа извне.
Единицей измерения работы в СИ является джоуль (Дж).
Отнеся работу расширения к 1 кг массы рабочего тела, получим
l = L/M; δl = δL/М = pdV/M = pd(V/M) = pdv. (2.16)
Величина l, представляющая собой удельную работу, совершаемую системой, содержащей 1 кг газа, равна
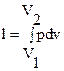 . (2.17)
. (2.17)
Поскольку в общем случае р – величина переменная, то интегрирование возможно лишь тогда, когда известен закон изменения давления p = p(v).
Формулы (2.14) – (2.16) справедливы только для равновесных процессов, при которых давление рабочего тела равно давлению окружающей среды.
В термодинамике для исследования равновесных процессов широко используют рv – диаграмму, в которой осью абсцисс служит удельный объем, а осью ординат – давление. Поскольку состояние термодинамической системы определяется двумя параметрами, то на рv – диаграмме оно изображается точкой. На рисунке 2.2 точка 1 соответствует начальному состоянию системы, точка 2 – конечному, а линия 12 – процессу расширения рабочего тела от v1 до v2.
При бесконечно малом изменении объема dv площадь заштрихованной вертикальной полоски равна pdv = δl, следовательно, работа процесса 12 изображается площадью, ограниченной кривой процесса, осью абсцисс и крайними ординатами. Таким образом, работа изменения объема эквивалентна площади под кривой процесса в диаграмме рv.
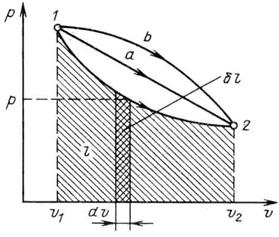
Рис. 2.2 – Графическое изображение работы в рv – координтах
Каждому пути перехода системы из состояния 1 в состояние 2 (например, 12, 1а2 или 1b2) соответствует своя работа расширения: l1b2>l1a2>l12 Следовательно, работа зависит от характера термодинамического процесса, а не является функцией только исходного и конечного состояний системы. С другой стороны, ∫pdv зависит от пути интегрирования и, следовательно, элементарная работа δl не является полным дифференциалом.
Работа всегда связана с перемещением макроскопических тел в пространстве, например перемещением поршня, деформацией оболочки, поэтому она характеризует упорядоченную (макрофизическую) форму передачи энергии от одного тела к другому и является мерой переданной энергии.
Поскольку величина δl пропорциональна увеличению объема, то в качестве рабочих тел, предназначенных для преобразования тепловой энергии в механическую, целесообразно выбирать такие, которые обладают способностью значительно увеличивать свой объем. Этим качеством обладают газы и пары жидкостей. Поэтому, например, на тепловых электрических станциях рабочим телом служат пары воды, а в двигателях внутреннего сгорания – газообразные продукты сгорания того или иного топлива.
2.4 Работа и теплота
Выше отмечалось, что при взаимодействии термодинамической системы с окружающей средой происходит обмен энергией, причем один из способов ее передачи – работа, а другой – теплота.
Хотя работа L и количество теплоты Q имеют размерность энергии, они не являются видами энергии. В отличие от энергии, которая является параметром состояния системы, работа и теплота зависят от пути перехода системы от одного состояния в другое. Они представляют две формы передачи энергии от одной системы (или тела) к другой.
В первом случае имеет место макрофизическая форма обмена энергией, которая обусловлена механическим воздействием одной системы на другую, сопровождаемым видимым перемещением другого тела (например, поршня в цилиндре двигателя).
Во втором случае осуществлена микрофизическая (т.е. на молекулярном уровне) форма передачи энергии. Мера количества переданной энергии – количество теплоты. Таким образом, работа и теплота – энергетические характеристики процессов механического и теплового взаимодействия системы с окружающей средой. Эти два способа передачи энергии эквивалентны, что вытекает из закона сохранения энергии, но неравноценны. Работа может непосредственно преобразовываться в теплоту – одно тело передает при тепловом контакте энергию другому. Количество же теплоты Q непосредственно расходуется только на изменение внутренней, энергии системы. При превращении теплоты в работу от одного тела – источника теплоты (ИТ) теплота передается другому – рабочему телу (РТ), а от него энергия в виде работы передается третьему телу – объекту работы (ОР).
Следует подчеркнуть, что если мы записываем уравнение термодинамики, то входящие в уравнения L и Q означают энергию, полученную соответственно макро– или микрофизическим способом.
 2014-02-09
2014-02-09 8074
8074
