В течение суток до 3% гемоглобина может спонтанно окисляться в метгемоглобин:
Hb (Fe2+) ® Met Hb (Fe3+) +e-
Восстановление метгемоглобина до гемоглобина осуществляет метгемоглобинредуктазная система. Она состоит из цитохрома b5 и цитохром b5 редуктазы (флавопротеин), донором водорода служит НАДН2, образующийся в гликолизе.
1). Цитохром b5 восстанавливает Fe3+ метгемоглобина в Fe2+ гемоглобина:
MetHb(Fe3+) + цитb5 восст → Hb(Fe2+) + цит b5 окисл
2). Окисленный Цитохром b5 восстанавливается цитохром b5 редуктазой:
цит b5 окисл + НАДН2 → цитb5 восст + НАД+
Восстановление метгемоглобина может осуществляться также неферментативным путём, например, за счёт витамина В12, аскорбиновой кислоты или глутатиона.
У здорового человека концентрация метгемоглобина в крови не превышает 1%.
Генетический дефект ферментов гликолиза и метгемоглобинредуктазной системы приводит к накоплению метгемоглобина и увеличению образования активных форм кислорода. Активные формы кислорода вызывают образование дисульфидных мостиков между протомерами метгемоглобина, что приводит к их агрегации с образованием телец Хайнца. Последние способствуют разрушению эритроцитов при попадании их в мелкие капилляры. Накопление метгемоглобина в крови из-за нарушения транспорта кислорода ведет к гипоксии.
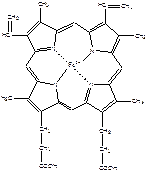 | Гем - это порфирин, в центре которого находиться Fe2+. Fe2+ включается в молекулу порфирина с помощью 2 ковалентных и 2 координационных связей. В зависимости от заместителей различают несколько типов порфиринов: протопорфирины, этиопорфирины, мезопорфирины и копропорфирины. В основе порфиринов находится порфин, который представляет собой конденсированную систему из 4 пирролов, соединенных между собой метиленовыми мостиками (-СН=). Молекула гема имеет плоское строение. При окислении железа, гем превращается в гематин (Fe3+). |
 2014-02-17
2014-02-17 1511
1511







