Под концентрацией раствора b понимается отношение массы сухого вещества Gc,, кг,содержащегося в растворе, к общей массе раствора. Она может выражаться в процентах или относительных величинах.
b=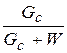 , (1.1)
, (1.1)
где W – количество растворителя в растворе, кг.
Растворителями могут быть вода, спирты, органические жидкости и т.д. В технике чаще всего имеют дело с водными растворами солей.
Для большинства растворов в определенном количестве воды или другого растворителя нельзя растворить неограниченное количество твердого вещества. Раствор, содержащий при данных условиях предельное количество растворенного вещества, называется насыщенным [1].
Количество растворенного вещества в насыщенном растворе, отнесенное к определенному количеству раствора или растворителя, называется растворимостью (табл. 1.1). Растворимость твердых веществ в воде не является постоянной величиной, а изменяется в значительных пределах в зависимости от температуры. Для большинства солей растворимость в воде с повышением температуры растет; для некоторых солей она понижается (CaCrO4, MnSO4, NaSO4 и др.), и избыток соли выпадает в виде кристаллов. У поваренной соли NaCI растворимость от температуры практически не зависит [1].
Присутствие кристаллов в растворе при выпаривании нежелательно, так как они осаждаются на стенках аппарата и поверхностях нагрева кипятильников и образуют слой накипи или осадка, которые снижают теплопередачу и ухудшают работу выпарных аппаратов.
Таблица 1.1. Растворимость некоторых веществ в воде при температуре 20 оС
| Вещество | Растворимость в воде г/100 г H2О | Концентрации насыщенного раствора, % | Вещество | Растворимость в воде г/100 г H2О | Концентрации насыщенного раствора, % |
| NaCI | 35,8 | 26,4 | BaSO4 | 0,00023 | 0,00023 |
| КCI | 34,2 | 25,5 | Mg(OH)2 | 0,001 | 0,001 |
| Na2СO3 | 21,2 | 17,6 | CaCO3 | 0,0014 | 0,0014 |
| NaOН | 107,0 | 51,7 | Ca(OH)2 | 0,16 | 0,16 |
| ВаCI | 35,6 | 26,3 | NaSO4 | 32,8 | 24,7 |
| СаSO4 | 0,2 | 0,2 | MgCI2 | 35,3 | 26,1 |
Процесс выпаривания характерен значительным изменением физико-химических свойств растворов, связанных с изменением его концентрации.
С повышением концентрации увеличиваются плотность и вязкость, понижаются удельная теплоемкость, теплопроводность и интенсивность теплоотдачи, изменяется теплота растворения [1].
Плотность раствора можно легко определить по правилу аддитивности, зная его концентрацию и плотности чистых компонентов при данной температуре:
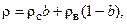 , (1.2)
, (1.2)
где 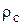 - плотность безводного нелетучего вещества, кг/м3;
- плотность безводного нелетучего вещества, кг/м3; 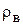 - плотность растворителя (воды), кг/ м3.
- плотность растворителя (воды), кг/ м3.
Все жидкие растворы обладают вязкостью, характерной для данного раствора. Вязкость всех растворов существенно зависит от температуры, уменьшаясь с ее повышением.
Численные значения динамической и кинематической вязкости растворов даются в справочной и специальной литературе. Изменение вязкости в зависимости от концентрации для некоторых растворов приведено
 |
на рис. 1.2.
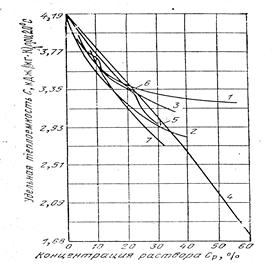
Рис.1.2. Изменение массовой удельной теплоемкости водных растворов в зависимости от концентрации раствора при 20 оС:
1 – NaOH; 2 – KOH; 3 – (NH4)2SO4; 4 – NaNO2; 5 – NH4NO3; 6 – K2CO3; 7 – CACI2
Удельную теплоемкость раствора с р, кДж/(кг·К), приближенно можно определить также по правилу аддитивности:
с р= с с b + с в(1- b), (1.3)
где с с – удельная теплоемкость безводного нелетучего вещества в растворе (табл. 1.2); с в – удельная теплоемкость воды при 20 оС.
 2014-02-09
2014-02-09 1864
1864