Первый закон термодинамики – частный случай всеобщего закона природы, т.е. закона сохранения и превращения энергии применительно к тепловым процессам. Если газу сообщить количество теплоты dQ, то часть её идёт на изменение энергии газа dU (внутренняя энергия), а другая часть на совершение работы dL против сил внешнего давления «р». Перемещение поршня dx, элементарная работа: 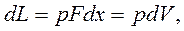
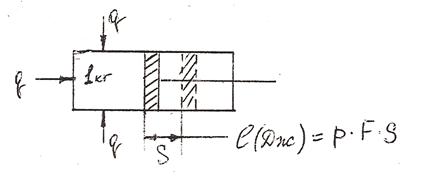
интегрируя данное выражение в пределах от V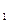 до V
до V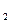 , находим работу:
, находим работу:
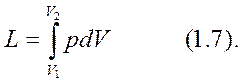
Обычно в термодинамике используют удельные значения соответствующих величин, т.е. 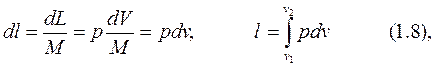
здесь v-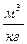 удельный объём рабочего тела.
удельный объём рабочего тела.
Данные соотношения справедливы для равновесных процессов, однако с известной долей приближения их используют для практических термодинамических расчётов. Для простого тела внутренняя энергия функция двух параметров: u=f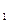 (р,T); u=f
(р,T); u=f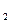 (р,v); u=f
(р,v); u=f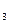 (v,T) (1.9).
(v,T) (1.9).
Таким образом, первый закон термодинамики можно сформулировать в такой редакции – теплота, которой обменивается термодинамическая система с окружающей средой, равна изменению внутренней энергии этой системы и работе, совершаемой в процессе изменения состояния термодинамической системы, т.е. dq=du+рdv (1.10)
Полная теплоёмкость системы равна:
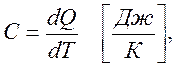
На практике пользуемся понятием удельной теплоёмкости. Различают удельную массовую, объёмную, мольную теплоёмкости. Изохорная теплоёмкость с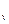 определяет скорость изменения внутренней энергии системы при T=var в процессе v=const. Для изобарного процесса теплоёмкость с
определяет скорость изменения внутренней энергии системы при T=var в процессе v=const. Для изобарного процесса теплоёмкость с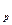 найдём воспользовавшись выражением:
найдём воспользовавшись выражением:
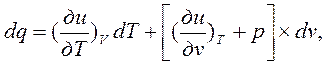 разделив это выражение на dT
разделив это выражение на dT
Получим: 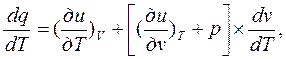 т.к. «u» не зависит от объёма «v»,
т.к. «u» не зависит от объёма «v»,
поскольку отсутствуют силы межмолекулярного взаимодействия, т.е. 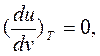 кроме того
кроме того 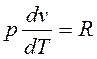 , соответственно
, соответственно 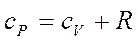 , это уравнение Майера. Для реальных газов
, это уравнение Майера. Для реальных газов 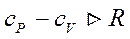 . Среднее значение теплоёмкости в определённом интервале температур определяется из выражения:
. Среднее значение теплоёмкости в определённом интервале температур определяется из выражения:
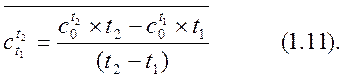
В термодинамических расчётах часто используется вспомогательная функция – энтальпия «H». Данная функция равна сумме «U» и произведения давления на объём термодинамической системы, Дж, т.е.:
H=U+рV
U, р, V- функции состояния термодинамической системы, следовательно, «H» - также функция состояния. Таким образом, изменение энтальпии в термодинамическом процессе не зависит от пути процесса и может быть представлена в виде функции двух любых параметров состояния простого тела:
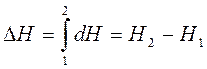 , где
, где 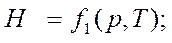
 удельная энтальпия
удельная энтальпия
h=u+рv, т.к. рdv=d(рv)-vdр, тогда dq=d(u+рv)-vdр=dh-vdр, при р=const, dq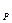 =dh.
=dh.
Таким образом элементарное изменение энтальпии:
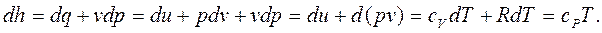
 2014-02-09
2014-02-09 2155
2155








