В трасляции участвуют мРНК, тРНК, рибосомы.
ТРАНСЛЯЦИЯ.
ГЕНЕТИЧЕСКИЙ КОД…..
Матричной (мРНК) считают РНК, которая в последовательности нуклеотидов в молекуле несет информацию, обеспечивающую синтез специфического белка непосредственно на ней самой, а также информацию о времени, количестве, месте и условиях синтеза этого белка.
Строение мРНК эукариот специфично: в их составе есть информативные, т.е. работающие как матрицы в процессе биосинтеза белка зоны и неинформативные участки. Неинформативные участки содержат кэп, 5'-нетранслируемую область (5'-НТО или 5'-UTR), 3'-нетранслируемую область (3'-НТО или 3'-UTR), полиадениловый фрагмент.
В эукариотических мРНК сразу за кэпом располагается 5'-нетранслирующая область (5'-UTR), с которой связываются белки, играющие важнейшую роль в регуляции инициации трансляции. К их числу относятся собственно белковые факторы инициации
(elF), а также белки-репрессоры трансляции. В инициации трансляции принимают участие также З'-нетранслируемая область (3'-UTR) и поли(А)-хвосты мРНК. В З'-UTR имеются и особые последовательности: сигналы полиаденилирования и сигнал внутриклеточной локализации. С З'-UTR способны связываться маскирующие белки (они делают мРНК недоступной для трансляции рибосомами) и дестабилизирующие белки, контролирующие доступность мРНК для атаки нуклеаз и таким образом определяющие время жизни мРНК в клетке.
В кодирующем участке (транслируемая область) с мРНК связываются факторы элонгации (eEF), АРСазы (аминоацил-тРНК-синтетазы), рибосомы, а также определенные ферменты, необходимые для процесса трансляции. В кодирующей области мРНК расположены также сигналы перекодирования (репрограммирования) трансляции, благодаря которым с одной и той же мРНК могут транслироваться разные белки.
З'-UTR играет, важную роль в активации и деградации мРНК,. Эта область отвечает за маскирование мРНК и усиление трансляции. Маскирование осуществляется белками, которые делают мРНК недоступной ни рибосомам, ни ферментам деградации (нуклеазам). Такая мРНК приобретает стабильную и неактивную в смысле трансляции форму и называется запасной мРНК. Эта РНК свойственна ооцитам и сперматозоидам, а в отдельных случаях и соматическим клеткам.
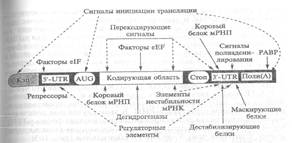
Рис. 162. (Коничев, с.323)Схема расположения функциональных участков в молекуле мРНК эукариот (по А.С.Спирину, 1996, с дополнениями).
Сплошные стрелки - области присоединения белков, участвующих в регуляции
трансляции, пунктирные стрелки - расположение тех или иных регуляторных
последовательностей (сигналов) в различных участках мРНК
.
Весьма существенную роль в регуляции трансляции играет и поли(А) последовательность на З'-конце мРНК. Часть мРНК эукариот полиаденилируется в ходе процессинга в ядре клеток (см. гл. 10), а сигналом для ядерного полиаденилирования служит последовательность AAUAAA, расположенная вблизи З'-конца молекулы.
Транспортные РНК: первичная, вторичная и третичная структура, роль модифицированных нуклеотидов (см. лк. Синтез РНК).слайд 5.
АКТИВАЦИЯ АМИНОКИСЛОТ.
Перед началом трансляции аминокислоты должны пройти стадию активации и присоединиться к тРНК, осуществляющими их доставку к рибосомам. тРНК, по сути, служат адаптерами при переводе нуклеотидных последовательностей мРНК в аминокислотные последовательности белков. В структуре тРНК содержится несколько функционально важных участков (петель ), главными из которых для адаптерной функции являются антикодон и акцептирующий конец (см. рис. 55).
Антикодон служит для взаимодействия с соответствующим кодоном мРНК, а акцептирующий конец (ЦЦА -последовательность, расположенная на 3'-конце тРНК) - для присоединения аминокислоты.
Каждая тРНК может переносить только одну из аминокислот, вов-лекаемых в биосинтез белка. Для большей части аминокислот име-ется несколько тРНК, которые называются изоакцепторными и обозначаются соответственно тPHKGly и т.д. Существование изоак-цепторных тРНК связано с вырожденностью генетического кода.
В результате присоединения аминокислот к З'-концу молекулы тРНК аминокислоты активируются — между карбоксильным концом молекулы аминокислоты и концевым аденозином акцептирующего конца тРНК возникает макроэргическая связь, энергия которой используется далее для синтеза пептидной связи в ходе биосинтеза белка на рибосомах (см. рис. 157,Коничев).
В результате специфического взаимодействия тРНК и соответствующей аминокислоты возникает аминоацил-тРНК — молекула, содержащая активированный аминокислотный остаток и соответствующий антикодон.
Активация аминокислот и их последующее присоединение к тРНК катализируются специфическими ферментами аминоацил-тРНК-синтетазами.
Суммарная реакция превращений, приводящих к образованию аминоацил-тРНК, может быть записана следующим образом:
Аминокислота + АТР + тРНК + Н2О →Амимоацил-тРНК + АМР + 2Рi.
Из этой реакции следует, что на синтез аминоацил-тРНК затрачиваются две богатые энергией фосфатные связи. Одна из них расходуется на образование эфирной связи между аминокислотой и тРНК, а другая (при гидролизе пирофосфата) сдвигает равновесие всей реакции в сторону образования продукта.
Ключевой особенностью реакции, приводящей к аминоацилированию тРНК, является специфичность участвующих в ней ферментов. Присоединение к тРНК каждой из 20 аминокислот, катализируется определенной аминоацил-тРНК-синтетазой. Фермент должен отличать одну аминокислоту от 19 других и переносить ее на одну или несколько (изоакцепторных) тРНК. Специфичность фермента определяется его прочным связыванием не менее чем с тремя участками тРНК. К этим участкам относятся акцепторный конец, D участок (D петля)и вариабельнаяпетля.
Кроме того, многие аминоацил-тРНК-синтетазы содержат, помимо участков синтеза, гидролитические участки. Возможно, что эти два участка действуют как двойные фильтры. Участок синтеза отбрасывает аминокислоты, превышающие по размеру нужную аминокислоту, а гидролитический участок разрушает те активиро-анные промежуточные продукты, которые меньше по размеру, чем требуется.
Т.о., синтетазы используют механизм коррекции с целью предотвращения ошибок в аминоацилировании тРНК. Частота таких ошибок чрезвычайно низка.
После образования аминоацил-тРНК эти молекулы направляются к рибосомам.
 2014-02-09
2014-02-09 8460
8460