Агрегатное состояние вещества характеризуется следующими фазами:
- твердая
- жидкая
- газообразная
которые зависят от температуры и давления.
Диаграмма фазового состояния диоксида углерода (СО2).



 Р, кПа Д С
Р, кПа Д С


I II
III
517 
 B
B
A
- 56,6 + 31 t (0C)
I - твердая фаза
II - жидкая фаза
III - газообразная фаза (перегретый газ, пар)
Пограничная линия между этими агрегатными состояниями представляет собой совокупность точек, в которых могут находиться в термодинамическом равновесии какие - либо две фазы:
твердое тело - пар (АВ),
жидкость - пар (ВС),
жидкость - твердое тело (ВД).
Кривая АВ - характеризует давление насыщенных паров диоксида углерода (СО2).
Из диаграммы видно, что при давлении ниже 517 Па, или при температуре ниже - 56,6 0C СО2 может, находится лишь в твердой фазе и газообразной фазах. Только при этих давлениях (Р) возможна сублимация твердого СО2 (тв. -газ). t сублимации является функцией давления.
Кривая ВС - характеризует давление насыщенных паров жидкой углекислоты
Р критическая = 7846 кПа
t = 31 0C
Кривая ВД - плавления (затвердевания) СО2
В отличие от аналогичной кривой для водного льда кривая ВД имеет положительный наклон к оси абцис.
В (·) В термодинамическое равновесие находится одновременно в трех фазах.
Параметрами этой (·) - называемой тройной точкой является давление 517 кПа и температура -56,6 0C.
При давлении 702 кПа и подводе теплоты, твердый СО2, как и водный лед последовательно переходит в жидкую, а из жидкой в газообразную фазу.
При давлении больше 517 кПа жидкой фазы СО2 не существует.
Сведения о термодинамических свойствах СО2 (энтальпия и энтропия) содержится в диаграммах i (t) и S (t).
Однако, эти даграммы непозволяют судить о количественном соотношении фаз в тройной точке, а значит не дает возможность определить энтропию и энтальпию в трех фазной смеси.
Поэтому, для определения энтальпии трехфазной смеси пользуются уравнениями:
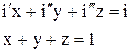

где:
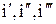 - энтальпии соответственно жидких, газообразных и твердых фаз.
- энтальпии соответственно жидких, газообразных и твердых фаз.
x,y,z - массовые доли этих фаз.
Холодопроизводительность 1 кг СО2 равна разности энтальпий парообразной фазы имеющий Р и t охлаждающей среды и твердых фаз.
Теплота плавления (замерзания) СО2 в тройной точке равна разности энтальпий жидкой и твердой фазы при давлении 517 кПа. Значение теплоты плавления тройной точки составляет 195,7 кДж / кг.
При давлении выше 517 кПа и температурах выше -56,6 0C теплота плавления практически мало отличается от теплоты плавления в тройной точке.
Удельная теплоемкость твердого диоксида углерода (кДж / кг· к) СО2 в диапазоне температуре от 57 до -110 0C определяется по формуле:
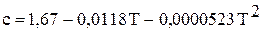
Теплопроводность СО2 при 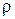 =1400 кг/м3 составляет 0,384 Вт/ м·К.
=1400 кг/м3 составляет 0,384 Вт/ м·К.
Лучшим сырьем для заводов сухого льда является углекислота спиртового брожения (почти 100 % СО2).
Фазовые превращения является физические процессы (плавление, кипение, сублимация) в которых вещества поглощают относительно большое количество теплоты при низкой температуре, что позволяет применить их для получения охладительного эффекта.
 2014-02-09
2014-02-09 540
540








