Тепловые процессы можно разделить на два основных типа – квазистатические (квази-равновесные) и неравновесные.
Квазистатические процессы состоят из непрерывно следующих друг за другом состояний равновесия. Для описания такого процесса можно пользоваться соответствующим уравне-нием состояния. Термодинамические параметры при этом могут изменяться со временем.
В неравновесных процессах система термодинамические параметры могут существенно изменяться как в зависимости от координат, так и от времени.
Работа газа в квазистатическом процессе.
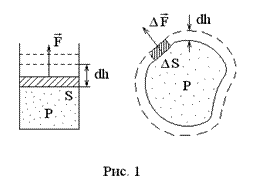 Рассмотрим газ в цилиндре с поршнем (рис. 1). Со стороны газа на поршень действует сила
Рассмотрим газ в цилиндре с поршнем (рис. 1). Со стороны газа на поршень действует сила 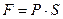 . При перемещении поршня на малое расстояние
. При перемещении поршня на малое расстояние 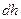 эта сила совершает работу
эта сила совершает работу
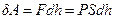 ,
, 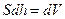 , где
, где 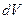 - изменение объема газа.
- изменение объема газа.
Таким образом, работа газа
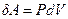 . (1)
. (1)
При расширении газа 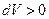 и
и 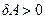 . При сжатии
. При сжатии 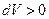 и
и 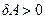 . Аналогичное выражение получается и в случае газа внутри эластичной оболочки произвольной формы (рис. 1). Полная работа при смещении поверхности оболочки на расстояние
. Аналогичное выражение получается и в случае газа внутри эластичной оболочки произвольной формы (рис. 1). Полная работа при смещении поверхности оболочки на расстояние 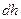 находится путем суммирования по малым элементам
находится путем суммирования по малым элементам 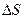 . Обозначение
. Обозначение 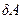 для бесконечно малой работы введено по той же причине, что и в курсе механики. Величина
для бесконечно малой работы введено по той же причине, что и в курсе механики. Величина 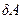 не всегда является полным дифференциалом. Более подробно мы обсудим этот вопрос далее.
не всегда является полным дифференциалом. Более подробно мы обсудим этот вопрос далее.
Работа газа в квазистатическом процессе с конечным изменением параметров от начального состояния 1 до конечного состояния 2 может быть найдена путем суммирования элементар-ных работ (1), что приводит к выражению
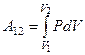 .
.
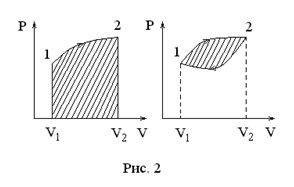 Тепловые процессы удобно изображать графически на плоскости каких-либо двух термоди-намических переменных, например,
Тепловые процессы удобно изображать графически на плоскости каких-либо двух термоди-намических переменных, например, 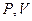 (рис. 2). При этом работа равна площади заштри-хованной фигуры под кривой, описывающей данный процесс. В круговом процессе система возвращается в исходное состояние (рис. 2). В этом случае работа по пути 1 – 2 положительна, а по пути 2 – 1 отрицательна. Полная работа равна площади заштрихованной фигуры внутри замкнутого контура на плоскости
(рис. 2). При этом работа равна площади заштри-хованной фигуры под кривой, описывающей данный процесс. В круговом процессе система возвращается в исходное состояние (рис. 2). В этом случае работа по пути 1 – 2 положительна, а по пути 2 – 1 отрицательна. Полная работа равна площади заштрихованной фигуры внутри замкнутого контура на плоскости 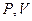 , описывающего круговой процесс.
, описывающего круговой процесс.
Если тело не получает энергию извне, то работа при его расширении совершается за счет его внутренней энергии.
Внутренняя энергия тела 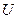 - сумма всех видов энергии, содержащихся в теле, за исключением энергии, которой тело обладает при взаимодействии с другими телами.
- сумма всех видов энергии, содержащихся в теле, за исключением энергии, которой тело обладает при взаимодействии с другими телами.
В данном курсе лекций мы будем пользоваться более простым определением.
Внутренняя энергия тела 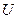 равна сумме кинетической энергии теплового движения молекул вещества и потенциальной энергии их взаимодействия друг с другом.
равна сумме кинетической энергии теплового движения молекул вещества и потенциальной энергии их взаимодействия друг с другом.
Такое определение справедливо, если можно пренебречь другими видами энергии, содержащимися в теле (магнитной энергии, ядерной энергии, энергии излучения т.д.)
В тепловых процессах, в отличие от механических, имеет место еще один вид энергии.
Количество тепла 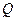 - энергия, передаваемая от одного тела к другому без совершения работы.
- энергия, передаваемая от одного тела к другому без совершения работы.
Количество тепла, или теплота, передается, например, от более нагретого тела к менее нагретому при их контакте друг с другом. Считается, что 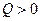 , если тело получает тепло и
, если тело получает тепло и 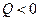 , если оно отдает тепло.
, если оно отдает тепло.
Все приведенные выше величины, 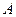 ,
, 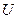 и
и 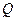 , имеют размерность энергии. Для количества тепла
, имеют размерность энергии. Для количества тепла 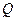 часто используется внесистемная единица калория. Она равна количеству тепла, необходимому для нагревания 1 г воды на 10C в интервале температур от 19,50С до 20,50С. 1 калория = 4,187 Джоуля (механический эквивалент теплоты). Эти три вида энергии связаны между собой следующим законом сохранения.
часто используется внесистемная единица калория. Она равна количеству тепла, необходимому для нагревания 1 г воды на 10C в интервале температур от 19,50С до 20,50С. 1 калория = 4,187 Джоуля (механический эквивалент теплоты). Эти три вида энергии связаны между собой следующим законом сохранения.
 2014-02-09
2014-02-09 550
550








