Прочность тел, ее изменение, переходы вещества из одного состояния в другое при повышении температуры, различие механических свойств по разным направлениям кристалла (анизотропия).
Атомы в молекуле связаны силами химических связей. Молекулы в теле – силами межмолекулярного взаимодействия. Для разрушения этих связей необходима добавочная энергия. Если нагретость связать с энергией движения молекул, то при достижении некоторой нагретости межмолекулярное взаимодействие уже будет неспособно удержать молекулы вместе – произойдет изменение структуры вещества (фазовый переход). Если сообщить большую энергию, то можно разрушить саму молекулу на составляющие ее атомы. Тогда свойства исходного вещества будут утеряны.
Одно и то же вещество может находиться в нескольких фазовых состояниях: кристалл, жидкость и пар. В кристаллическом состоянии взаимодействие молекул велико. Взаимодействие характеризуется потенциальной энергией Wp. В кристалле она во много раз больше кинетической энергии теплового движения частиц Ek. (Wp>> Ek). Поэтому молекулы в кристалле находятся вблизи определенных положений равновесия, которые расположены в строгом геометрическом порядке. На рисунке изображен кубический кристалл.
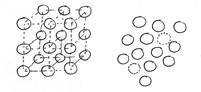
В жидкости (правый рисунок) молекулы сохраняют ближний порядок и расположены довольно плотно, однако в жидкости есть «дырки» - положения равновесия, в которых нет молекул (показаны пунктиром). Поскольку в жидкостях кинетическая энергия теплового движения сравнима с энергией взаимодействия молекул, (Wp~ Ek) то молекула может время от времени «перескакивать» в соседние положения. Поэтому жидкость под действием внешних сил легко течет. Объемное сжатие жидкости затруднено плотным расположением молекул. ПОЧЕМУ ТРУДНО УПЛОТНИТЬ ДЫРКИ – НУЖНО ПРЕОДОЛЕТЬ СРАЗУ ВСЕ БАРЬЕРЫ (ОПЯТЬ РОЛЬ ХВОСТОВ РАСПРЕДЕЛЕНИЯ м) В паре молекулы находятся на больших расстояниях, движутся хаотично и слабо взаимодействуют друг с другом (Wp<< Ek). Поэтому объем пара изменить очень легко. Ясно, что при увеличении нагретости, когда кинетическая энергия движения молекул растет, а энергия взаимодействия почти не меняется, кристалл должен перейти в жидкость (плавление), а затем жидкость – в пар (испарение). В кристаллических телах оба перехода происходят при определенных температурах. В аморфных телах переход твердое тело – жидкость происходит постепенно с нагреванием (тело размягчается), переход жидкость - пар часто не осуществляется вовсе (поскольку при дальнейшем нагревании начинает разрушаться химическая структура вещества, например, воска). Газом называется пар вещества, которое в привычном нам температурном диапазоне пребывает только в парообразном состоянии (например, кислород). «Водяной газ» говорить не принято, поскольку в привычных условиях мы можем наблюдать воду в твердом и жидком состояниях.
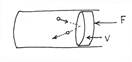 Некоторые явления, например тепловое расширение твердых тел и жидкостей, объяснить очень непросто. То, что об этом пишут в учебниках для школьников, как правило, чушь. Однако многие наблюдаемые явления (как было упомянуто в цитате Фейнмана) находят простое и изящное объяснение. Например, давление газа. Пусть мы имеем газ в цилиндре, ограниченном подвижным поршнем. Поскольку молекулы ударяются о поршень с левой стороны, чтобы удержать его, справа нужно прикладывать некоторую силу. Она будет компенсировать силу давления газа, которое, как мы видим, имеет динамический характер (то есть, возникает в силу движения молекул газа И ВЗАИМ С ПОРШН).
Некоторые явления, например тепловое расширение твердых тел и жидкостей, объяснить очень непросто. То, что об этом пишут в учебниках для школьников, как правило, чушь. Однако многие наблюдаемые явления (как было упомянуто в цитате Фейнмана) находят простое и изящное объяснение. Например, давление газа. Пусть мы имеем газ в цилиндре, ограниченном подвижным поршнем. Поскольку молекулы ударяются о поршень с левой стороны, чтобы удержать его, справа нужно прикладывать некоторую силу. Она будет компенсировать силу давления газа, которое, как мы видим, имеет динамический характер (то есть, возникает в силу движения молекул газа И ВЗАИМ С ПОРШН).
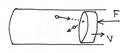
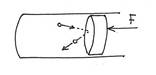
При этом скорость молекул после упругого столкновения не меняется. Нагретость газа не меняется. Приведем поршень в движение налево. Видно, что после соударения молекула будет иметь скорость большую, чем до него. Значит, по мере сжатия поршнем газ будет нагреваться! То есть, механическая работа, совершаемая поршнем, превратится в энергию молекул. При движении поршня направо..(проведите рассуждения сами). Конечно, можно придумать и другие теоретические объяснения, но столь просто объяснить такой обширный круг явлений вряд ли получится.
Далеко не все так просто, например нельзя объяснить, почему гелий при очень низких температурах совершенно лишается вязкости. Для этого нужна теория помощнее.
 2014-02-10
2014-02-10 782
782







