Максимальные отклонения от положения равновесия показаны прямоугольниками на графике (повтор рисунка)

Газ- разреженная, легко сжимаемая субстанция. Сравним характерные плотности газов и жидкостей на примере воздуха и воды:
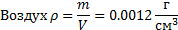
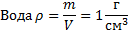
Жидкость – не сжимаема, но легко меняет форму. Твердые тела – несжимаемы и сохраняют форму.
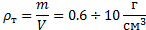
Рассмотрим характерные газы, жидкости и твердые тела с точки зрения параметра  , где l - среднее расстояние между молекулами, d – диаметр молекулы:
, где l - среднее расстояние между молекулами, d – диаметр молекулы:
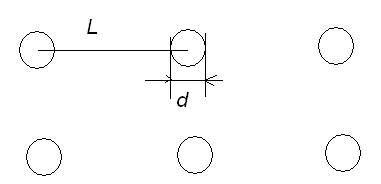
Газ:

Жидкость и твердое тело –
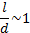
Причем атомы в твердых телах упакованы в решетку, причем возможны два случая:
аморфная фаза или кристаллическая фаза.
Отличие агрегатных состояний с точки зрения соотношения потенциальной энергии взаимодействия и кинетической энергии молекул.
Как мы уже упоминали, агрегатное состояние вещества в основном определяется соотношением между средней кинетической энергии молекулы при расстоянии, соответствующем максимальной глубине потенциальной ямы, и самой глубиной потенциальной ямы в межмолекулярном потенциале для парного взаимодействия молекул, обозначим этот параметр Pа
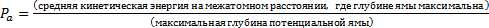
Твердому агрегатному состоянию вещества соответствует 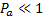 , жидкому состоянию
, жидкому состоянию 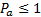 , газообразному
, газообразному 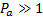 . Данным значениям параметра соответствуют следующие соотношения между осредненными во времени характеристиками отдельной молекулы (Ek - средняя кинетическая энергия, U 0 – глубина потенциальной ямы):
. Данным значениям параметра соответствуют следующие соотношения между осредненными во времени характеристиками отдельной молекулы (Ek - средняя кинетическая энергия, U 0 – глубина потенциальной ямы):
Газы – Ek >> U 0
Жидкости – Ek ≈ U 0
Твердые тела Ek << U 0
К настоящему времени твердые тела изучены достаточно хорощо, а вот как движутся молекулы жидкости – в точности неизвестно, предполагается, что осуществляются перескоки по связям (положительный заряд одной молекулы – отрицательный заряд другой).
Среди твердых тел наиболее хорошо изучена твердая фаза, а вот аморфная фаза изучена недостаточно. Аморфные тела напоминают фотоснимок жидкости, который существует неограниченное время – отклонения атомов от положений равновесия очень малы. Или очень быстро замороженная жидкость, которая не успела принять строгую кристаллическую структуру.
Свойства твердых тел во многом зависят от типа решетки, в которую упакованы атомы. Например, NaCl – это куб. А вот для углерода возможны два типа решетки. Тетраэдрический тип соответствует алмазу, имеющему высокую прочность:
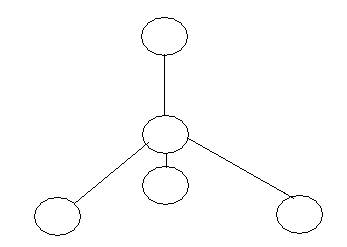
А вот графит представляет собой совсем другой тип – слои из шестиугольников, связь между которыми осуществляется слабыми  -электронамными орбитали (на рисунке они выглядят как восьмерки). Благодаря этому графитовым стержнем можно рисовать – происходит отслоение слоев графита.
-электронамными орбитали (на рисунке они выглядят как восьмерки). Благодаря этому графитовым стержнем можно рисовать – происходит отслоение слоев графита.
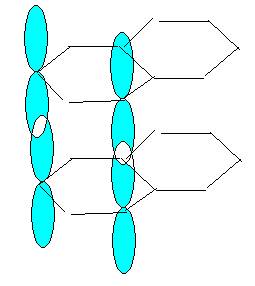
Получено вещество, состоящее из одного слоя – его сняли скотчем…
Однако газы, жидкости и твердые тела тела – классификация прошлого века. Сейчас появились такие агрегатные состояния, как «жидкие кристаллы». Они состоят из асимметричных молекул, например, узких и длинных, способных принимать определенную ориентацию во внешнем поле. Они обладают свойствами жидкости и кристалла.
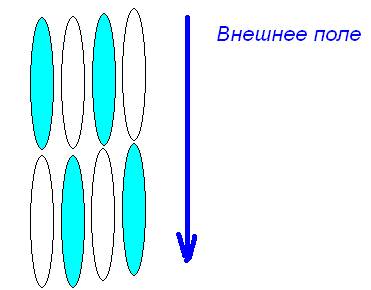
Жидкие кристаллы открыли в 30гг, и 60 лет они были никому не нужны. Через 60 лет им нашли применение – дисплей.
 2014-02-12
2014-02-12 868
868








