Термодинамическая температурная шкала определяется по одной реперной точке, в качестве которой взята тройная точка воды (температура, при которой лед, вода и насыщенный пар при давлении 609 Па находятся в термодинамическом равновесии). Температура этой точки по термодинамической шкале равна 273,16 К, (точно). Градус Цельсия равен Кельвину. В термодинамической шкале температура замерзания воды равна 273,15 К (при том же давлении, что и в Международной практической шкале), поэтому, по определению, термодинамическая температура и температура по Международной практической шкале связаны соотношением T=273,15+t. Температура T=0 называется нулем кельвин. Анализ различных процессов показывает, что 0 К недостижим, хотя приближение к нему сколь угодно близко возможно.
Удельный объем v — это объем единицы массы. Когда тело однородно, т. е. его плотность r=const, то v= V/m= 1/r. Так как при постоянной массе удельный объем пропорционален общему объему, то макроскопические свойства однородного тела можно характеризовать объемом тела.
Параметры состояния системы могут изменяться. Любое изменение в термодинамической системе, связанное с изменением хотя бы одного из ее термодинамических параметров, называется термодинамическим процессом. Макроскопическая система находится в термодинамическом равновесии, если ее состояние с течением времени не меняется (предполагается, что внешние условия рассматриваемой системы при этом не изменяются).
Молекулярно-кинетическая теория идеальных газов
§ 41. Опытные законы идеального газа
В молекулярно-кинетической теории пользуются идеализированной моделью идеального газа, согласно которой:
1) собственный объем молекул газа пренебрежимо мал по сравнению с объемом сосуда;
2) между молекулами газа отсутствуют силы взаимодействия;
3) столкновения молекул газа между собой и со стенками сосуда абсолютно упругие.
Модель идеального газа можно использовать при изучении реальных газов, так как они в условиях, близких к нор-
мальным (например, кислород и гелий), а также при низких давлениях и высоких температурах близки по своим свойствам к идеальному газу. Кроме того, внеся поправки, учитывающие собственный объем молекул газа и действующие молекулярные силы, можно перейти к теории реальных газов.
Опытным путем, еще до появления молекулярно-кинетической теории, был установлен целый ряд законов, описывающих поведение идеальных газов, которые мы и рассмотрим.
Закон Бойля — Мариотта: для данной массы газа при постоянной температуре произведение давления газа на его объем есть величина постоянная:
pV = const (41.1) при Т= const, m =const.
Кривая, изображающая зависимость между величинами р и V, характеризующими свойства вещества при постоянной температуре, называется изотермой. Изотермы представляют собой гиперболы, расположенные на графике тем выше, чем выше температура, при которой происходит процесс (рис. 60).

Закон Гей-Люссака: 1) объем данной массы газа при постоянном давлении изменяется линейно с температурой:
V=V0( 1 +at) (41.2) при p = const, m = const;

2) давление данной массы газа при постоянном объеме изменяется линейно с температурой:
p = p0( 1 +at) (41.3) при V =const, m =const.
В этих уравнениях t — температура по шкале Цельсия, р 0и V 0 — давление и объем при 0°С, коэффициент a=1/273,15 К-1.
Процесс, протекающий при постоянном давлении, называется изобарным. На диаграмме в координатах V, t (рис.61) этот процесс изображается прямой, называемой изобарой. Процесс, протекающий при постоянном объеме, называется изохорным. На диаграмме в координатах р, t (рис. 62) он изображается прямой, называемой изохорой.
Из (41.2) и (41.3) следует, что изобары и изохоры пересекают ось температур в точке t =-1/a=-273,15 °С, определяемой из условия 1+at=0. Если сместить начало отсчета в эту точку, то происходит переход к шкале Кельвина (рис. 62), откуда
T=t+ 1 /a.

Вводя в формулы (41.2) и (41.3) термодинамическую температуру, законам Гей-Люссака можно придать более удобный вид:
V=V0(1+at)=V0[1+a(T-1/a)]=v0at,
p=p0(1+at)=p0 [1 +a(Т- 1 /a)]=р0aТ, или
V 1 /V 2 = T 1 /T 2 (41.4)
при p = const, m = const,
р 1/ р 2 = T 1/ T 2 (41.5) при V =const, m =const,
где индексы 1 и 2 относятся к произвольным состояниям, лежащим на одной изобаре или изохоре.
Закон Авогадро: моли любых газов при одинаковых температуре и давлении занимают одинаковые объемы. При нормальных условиях этот объем равен 22,41•10-3м3/моль.
По определению, в одном моле различных веществ содержится одно и то же число молекул, называемое постоянной Авогадро:
n а = 6,022•1023 моль-1.
Закон Дальтона: давление смеси идеальных газов равно сумме парциальных давлений входящих в нее газов, т. е.
p=p 1 +p 2 +... + pn,
где p 1, p 2,..., p n— парциальные давления — давления, которые оказывали бы газы смеси, если бы они одни занимали объем, равный объему смеси при той же температуре.
Уравнение Клапейрона — Менделеева
Как уже указывалось, состояние некоторой массы газа определяется тремя термодинамическими параметрами: давлением р, объемом V и температурой Т.

Между этими параметрами существует определенная связь, называемая уравнением состояния, которое в общем виде дается выражением
f(р, V, Т) =0,
где каждая из переменных является функцией двух других.
Французский физик и инженер Б. Клапейрон (1799—1864) вывел уравнение состояния идеального газа, объединив законы Бойля — Мариотта и Гей-Люссака. Пусть некоторая масса газа занимает объем V 1, имеет давление р 1и находится при температуре Т 1. Эта же масса газа в другом произвольном состоянии характеризуется параметрами р 2, V 2, Т 2 (рис.63). Переход из состояния 1 в состояние 2 осуществляется в виде двух процессов: 1) изотермического (изотерма 1 — 1 '), 2) изохорного (изохора 1 '— 2).
В соответствии с законами Бойля — Мариотта (41.1) и Гей-Люссака (41.5) запишем:
p 1 V 1= p '1 V 2, (42.1)
p '1/ p '2=T1/T2. (42.2)
Исключив из уравнений (42.1) и (42.2) р' 1, получим
p 1 V 1 /T 1 =p 2 V 2 /Т 2.
Так как состояния 1 и 2 были выбраны произвольно, то для данной массы газа
величина pV/T остается постоянной,
т. е.
pV/T =B=const. (42.3)
Выражение (42.3) является уравнением Клапейрона, в котором В — газовая постоянная, различная для разных газов.
Русский ученый Д. И. Менделеев (1834—1907) объединил уравнение Клапейрона с законом Авогадро, отнеся уравнение (42.3) к одному молю, использовав молярный объем Vт. Согласно закону Авогадро, при одинаковых р и Т моли всех газов занимают одинаковый молярный объем Vm, поэтому постоянная В будет одинаковой для всех газов. Эта общая для всех газов постоянная обозначается R и называется молярной газовой постоянной. Уравнению
pVm = RT (42.4)
удовлетворяет лишь идеальный газ, и оно является уравнением состояния идеального газа, называемым также уравнением Клапейрона — Менделеева.
Числовое значение молярной газовой постоянной определим из формулы (42.4), полагая, что моль газа находится при нормальных условиях (р 0 = 1,013•105 Па, T0=273,15 K:, Vm= 22,41•10-3м3/моль): R = 8,31 Дж/(моль•К).
От уравнения (42.4) для моля газа можно перейти к уравнению Клапейрона — Менделеева для произвольной массы газа. Если при некоторых заданных давлений и температуре один моль газа занимает молярный объем l/m, то при тех же условиях масса т газа займет объем V = (m/M) Vm, где М — молярная масса (масса одного моля вещества). Единица молярной массы — килограмм на моль (кг/моль). Уравнение Клапейрона — Менделеева для массы т газа
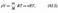
где v = m/M — количество вещества.
Часто пользуются несколько иной формой уравнения состояния идеального газа, вводя постоянную Больцмана:
k=R/NА=1,38•10-23 Дж/К.
Исходя из этого уравнение состояния (42.4) запишем в виде
p = RT/Vm = kNAT/Vm = nkT,
где N A/ V m = n —концентрация молекул (число молекул в единице объема). Таким образом, из уравнения
p = nkT (42.6)
следует, что давление идеального газа при данной температуре прямо пропорционально концентрации его молекул (или плотности газа). При одинаковых температуре и давлении все газы содержат в единице объема одинаковое число молекул. Число молекул, содержащихся в 1 м3 газа при нормальных условиях, называется числом Лошмидта:
NL = P0/(kT0) = 2,68•1025 м-3.
Основное уравнение молекулярно-кинетической теории идеальных газов
Для вывода основного уравнения молекулярно-кинетической теории рассмотрим одноатомный идеальный газ. Предположим, что молекулы газа движутся хаотически, число взаимных столкновений между молекулами газа пренебрежимо мало по сравнению с числом ударов о стенки сосуда, а соударения молекул со стенками сосуда абсолютно упругие. Выделим на стенке сосуда некоторую элементарную площадку DS (рис. 64) и вычислим давление, оказываемое на эту площадку. При каждом соударении молекула, движущаяся перпендикулярно площадке, передает ей импульс m 0 v-(-m 0 v)=2m 0 v, где т 0— масса молекулы, v — ее скорость.
За время Dt площадки DS достигнут только те молекулы, которые заключены в объеме цилиндра с основанием DS и высотой v D t (рис.64). Число этих молекул равно n D Sv D t (n— концентрация молекул).
Необходимо, однако, учитывать, что реально молекулы движутся к площадке

DS под разными углами и имеют различные скорости, причем скорость молекул при каждом соударении меняется. Для упрощения расчетов хаотическое движение молекул заменяют движением вдоль трех взаимно перпендикулярных направлений, так что в любой момент времени вдоль каждого из них движется 1/3 молекул, причем половина молекул (1/6) движется вдоль данного направления в одну сторону, половина — в противоположную. Тогда число ударов молекул, движущихся в заданном направлении, о площадку DS будет 1/6nDSvDt. При столкновении с площадкой эти молекулы передадут ей импульс
D Р = 2 m 0 v •1/6 n D Sv D t =1/3n m 0 v 2D S D t.
Тогда давление газа, оказываемое им на стенку сосуда,
p =DP/(DtDS)=1/3nm0v2. (43.1)
Если газ в объеме V содержит N молекул,
движущихся со скоростями v 1, v 2,..., vN, то
целесообразно рассматривать среднюю квадратичную скорость
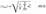
характеризующую всю совокупность молекул газа.
Уравнение (43.1) с учетом (43.2) примет вид
р = 1/3пт0 <vкв>2. (43.3)
Выражение (43.3) называется основным уравнением молекулярно-кинетической теории идеальных газов. Точный расчет с учетом движения молекул по все-
возможным направлениям дает ту же формулу.
Учитывая, что n = N/V, получим

где Е — суммарная кинетическая энергия поступательного движения всех молекул газа.
Так как масса газа m = Nm 0, то уравнение (43.4) можно переписать в виде
pV =1/3m<vкв>2.
Для одного моля газа т = М (М — молярная масса), поэтому
pV m=1/3M<vкв>2,
где Vm — молярный объем. С другой стороны, по уравнению Клапейрона — Менделеева, pVm=RT. Таким образом,
RT=1/3М <vкв>2, откуда
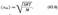
Так как М = m0NA, где m0—масса одной молекулы, а NА — постоянная Авогадро, то из уравнения (43.6) следует, что
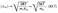
где k = R/NA —постоянная Больцмана. Отсюда найдем, что при комнатной температуре молекулы кислорода имеют среднюю квадратичную скорость 480 м/с, водорода — 1900 м/с. При температуре жидкого гелия те же скорости будут соответственно 40 и 160 м/с.
Средняя кинетическая энергия поступательного движения одной молекулы идеального газа
<e0) =E/N = m0 <vкв> )2/2 = 3/2kT(43.8)
(использовали формулы (43.5) и (43.7)) пропорциональна термодинамической температуре и зависит только от нее. Из этого уравнения следует, что при T=0 <e0> =0,,т. е. при 0 К прекращается поступательное движение молекул газа, а следовательно, его давление равно нулю. Таким образом, термодинамическая температура является мерой средней кинетической энергии поступательного движения молекул идеального газа и формула (43.8) раскрывает молекулярно-кинетическое толкование температуры.
 2014-02-12
2014-02-12 1623
1623