Система уравнений химического равновесия состоит в случае одной химической реакции из аппроксимации закона действующих масс в виде уравнения:
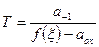 , (19)
, (19)
и уравнения баланса энтальпии Н 3= Н 2 в виде:
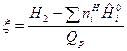 . (20)
. (20)
Эта система уравнений решается графоаналитическим способом.
В уравнении (20) 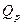 -изобарный тепловой эффект химической реакции, определяемый по формуле:
-изобарный тепловой эффект химической реакции, определяемый по формуле:
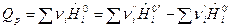 . (21)
. (21)
Задаваясь рядом значений температуры (например, Т=2000, 4000, 5000К), определяются значения величины пробега химической реакции по формуле (20) и строится график зависимости 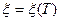 , которая при пересечении с прямой
, которая при пересечении с прямой 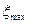 определяет максимальное значение температуры Tmax..
определяет максимальное значение температуры Tmax..
Для определения коэффициентов аппроксимации а-1 и аох, входящих в формулу (19), используется аппроксимация константы равновесия, выраженной через парциальные давления:
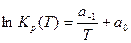 , (22)
, (22)
которая зависит только от температуры и является линейной функцией от 1/Т. Коэффициенты а-1 и ао определяются из решения системы из двух уравнений (22)для двух значений температуры, например, 1000 и 3000К.
Натуральный логарифм константы Кр определяется по формуле
ln Kp = ln10 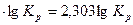 , (23)
, (23)
где lg Kp =- 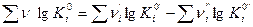 ;
;
K 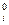 -константа равновесия химической реакции распада i-го вещества на газообразные атомы; lg Ki определяется из справочной литературы для индивидуальных веществ, входящих в термодинамическую систему. Коэффициент аппроксимации аох определяется по формуле:
-константа равновесия химической реакции распада i-го вещества на газообразные атомы; lg Ki определяется из справочной литературы для индивидуальных веществ, входящих в термодинамическую систему. Коэффициент аппроксимации аох определяется по формуле:
a 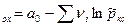 , (24)
, (24)
где 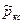 - относительное давление в камере сгорания.
- относительное давление в камере сгорания.
Задаваясь рядом значений пробега химической реакции x определяется значение функции f (x), входящей в формулу (19):
f (x)=ln Kx (p,T)=å ni ln xi, (25)
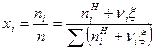 ,
,
f (x)= 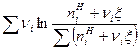 . (26)
. (26)
где Kx - константа равновесия, выраженная через молярные доли хi, зависит от температуры и давления:
Kx(p,T)=Kp(T)  , (27)
, (27)
или ln Kx =ln Kp - 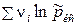 .
.
Подставляя полученные значения функции f (x) по (26) и коэффициентов а-1 и аох по (22) и (24) в уравнение(19), определяется температура смеси газов для заданных значений пробега химической реакции и строится график зависимости T=T (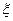 ). Пересечение этой зависимости с зависимостью x=x (T), полученной при решении уравнения (20), дает искомые равновесные значения x
). Пересечение этой зависимости с зависимостью x=x (T), полученной при решении уравнения (20), дает искомые равновесные значения x  и Т 3, что является решением системы уравнений химического равновесия (19) и (20) в сечении 3-3 для случая протекания в камере сгорания ЖРД одной химической реакции.
и Т 3, что является решением системы уравнений химического равновесия (19) и (20) в сечении 3-3 для случая протекания в камере сгорания ЖРД одной химической реакции.
Определяется погрешность определения пробега химической реакции
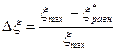 100%.
100%.
 2015-01-21
2015-01-21 494
494








