Строение карбонат иона (СО3)2-. Экспериментальный факт:
По данным рентгеноструктурного анализа, в карбонат-ионе все связи С—О имеют одинаковую длину, все атомы кислорода — одинаковую электронную плотность.
Чтобы передать строение этой частицы, необходимо воспользоваться набором из трёх предельных структур:
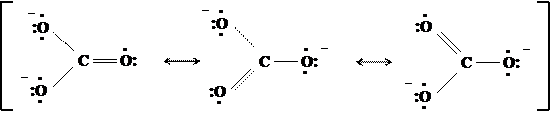
Как видно, данные резонансные структуры не отличаются расположением атомов, они различаются только распределением электронов между ними. Хотя, согласно концепции резонанса, граничные структуры в действительности не существуют, а являются лишь формулами, однако наложением их друг на друга можно представить распределение электронов в реальной частице. Такой «резонансный гибрид» называется мезоформулой. Если канонические структуры равноценны между собой по энергии (как в карбонат-ионе), то они вносят равный вклад в реальное строение молекулы (имеют одинаковый «удельный вес»).
Для карбонат-иона мезоформула имеет вид:
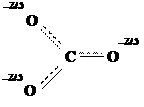
Мезоформула показывает, что в этом анионе нет чисто простых и чисто двойных связей. Все связи имеют нецелочисленную кратность. Аналогично, ни на одном из атомов кислорода нет целого отрицательного заряда: все заряды дробные, их величины равны между собой. Такое распределение электронов называется делокализацией. Оно соответствует экспериментальным данным.
Из солей угольной кислоты наибольшее значение имеют карбонат натрия (сода), карбонат калия (поташ), карбонат кальция (мел, мрамор, известняк), гидрокарбонат натрия (питьевая сода) и основной карбонат меди (CuOH)2CO3 (малахит).
Основные соли угольной кислоты в воде практически нерастворимы и при нагревании легко разлагаются:
(CuOH)2CO3 = 2CuO + CO2 + H2O.
Термическая устойчивость карбонатов зависит от поляризационных свойств ионов, входящих в состав карбоната. Чем больше поляризующее действие оказывает катион на карбонат-ион, тем ниже температура разложения соли. Если катион способен легко деформироваться, то карбонат-ион сам также будет оказывать поляризующее действие на катион, что приведет к резкому снижению температуры разложения соли.
Карбонаты натрия и калия плавятся без разложения, а большинство остальных карбонатов при нагревании разлагаются на оксид металла и углекислый газ:
MgCO3 = MgO + CO2.
Мочеви́на (карбамид) — химическое соединение, диамид угольной кислоты. Белые кристаллы, растворимые в полярных растворителях (воде, этаноле, жидком аммиаке).
 2015-01-30
2015-01-30 2741
2741








