Одним из решающих факторов, определяющих поведение веществ при распределительной хроматографии, является коэффициент распреде-ления Kр в данной системе фаз. Для некоторого вещества и определенной системы фаз Kр есть величина постоянная, не зависящая от концентрации вещества. Расчет величины Kр проводят по формуле (3.5).
Различие в коэффициентах распределения компонентов разделяемой смеси между двумя несмешивающимися жидкостями положено в основу хроматографического разделения и анализа. Такой вид хроматографии называется жидкостно-жидкостной распределительной хроматографией (ЖЖРХ). В зависимости от природы твердого носителя, жидкой неподвиж-ной фазы и способа проведения эксперимента ЖЖРХ делят на бумажную, тонкослойную и колоночную (см. табл. 3.1).
Различают три вида распределительной хроматографии: одномерную, двухмерную и трехмерную. Первые два вида относятся к бумажной и тонкослойной хроматографии, тогда как хроматограммы третьего вида получают на колонке.
3.4.1. Бумажная распределительная хроматография
Хроматография на бумаге применяется для разделения микроколи-честв смеси веществ. Метод приобрел огромное значение в исследовании белков, углеводов, жиров и многих других биологически активных и природных соединений.
В качестве носителя неподвижной жидкой фазы в бумажной хрома-тографии применяется специальная фильтровальная бумага, способная удерживать в своих порах значительные количества жидкости, являю-щейся неподвижной фазой. Неподвижной фазой обычно служит вода. Подвижной фазой является органический растворитель или смесь органи-ческих жидкостей и воды в разных соотношениях. Подвижная и неподвиж-ная фазы не должны смешиваться.
Для водорастворимых веществ в качестве подвижной фазы применя-ются органические растворители, насыщенные водой, которая служит неподвижной фазой. Нерастворимые в воде вещества должны хроматогра-фироваться водными растворами органических веществ; неподвижной фазой в этом случае должны быть неполярные органические соединения.
В бумажной хроматографии в одних случаях встречаются признаки распределительного механизма, в других – адсорбционного, однако подав-ляющее большинство случаев хроматографирования на бумаге основы-вается на принципе распределительной хроматографии.
Одномерная и двухмерная бумажные хроматографии могут выпол-няться в двух вариантах: в восходящем и нисходящем потоке растворителя. В настоящее время известна еще и горизонтальная, или радиальная, хроматография.
С помощью одномерных хроматограмм не всегда удается разделить сложные смеси веществ – в одной зоне может оказаться более одного компонента. В этом случае используют двухмерную хроматографию.
Качественный анализ хроматограммы, т.е. идентификацию разделя-емых веществ, проводят несколькими способами. Наиболее простой – способ «свидетелей» – заключается в том, что если параллельно с каплей анализируемой смеси на полоску бумаги нанести каплю смеси, содержа-щей известные вещества, то после проявления хроматограммы можно, сравнивая положения пятен компонентов анализируемой смеси с положе-ниями пятен известных соединений, идентифицировать неизвестные ве-щества. Недостатком метода является его громоздкость, необходимость каждый раз наносить и хроматографировать искусственно приготовлен-ную смесь известных веществ.
Другим методом идентификации является определение степени удерживания (коэффициента подвижности) Rf (ratio – отношение, f – фронт) и сравнение полученных значений Rf со значениями Rf для контрольной смеси. Коэффициент подвижности представляет собой отно-шение скорости движения зоны компонента к скорости движения фронта подвижной фазы.
Величина Rf может быть определена экспериментально (рис. 3.3). На хроматограмме измеряют расстояние l от линии старта смеси веществ до центра пятен и расстояние от линии старта до линии финиша раствори-теля – L. Величину Rf рассчитывают по формуле:
Rf = Vi / VE = (li / t) / (L / t) = li / L, (3.7)
где Vi = li / t и VE = L / t –соответственно скорости перемещения i -го компонента и растворителя Е; li и L – путь, пройденный i -м компонентом и растворителем соответственно; t – время, необходимое для перемещения растворителя от линии старта до линии фронта растворителя. Расстояния li отсчитывают от линии старта до центра пятна соответствующего компонента.
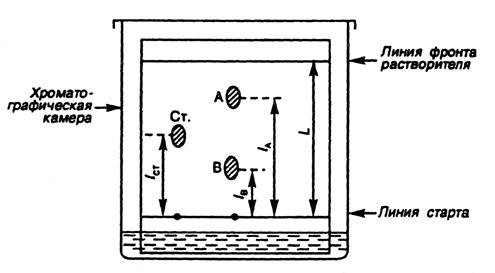
Рис. 3.3. Схема разделения компонентов А и В
методом бумажной распределительной хроматографии
Обычно коэффициент подвижности лежит в пределах от 0 до 1. Оптимальное значение составляет 0,3 – 0,7. Условия хроматографирования подбирают так, что величина Rf отличалась и от нуля, и от единицы.
Коэффициент подвижности является важной характеристикой систе-мы «сорбент – сорбат». Для воспроизводимых и строго постоянных усло-вий хроматографирования величина Rf постоянна.
Коэффициент подвижности Rf зависит от целого ряда факторов: при-роды и качества растворителя, его чистоты; природы и качества сорбента, толщины его слоя; активности сорбента (содержания в нем влаги); техники эксперимента (массы образца, длины L пробега растворителя); навыка экспериментатора и т.д. Постоянство воспроизведения всех параметров на практике иногда бывает затруднительным. Для нивелирования влияния условий проведения процесса вводят относительный коэффициент подвижности:
RS = l / l ст = Rf / Rf (ст),
где Rf = l / L; Rf (ст)= l ст / L; l ст – расстояние от линии старта до центра пятна стандарта (см. рис. 3.3).
Относительный коэффициент подвижности RS является более объек-тивной характеристикой подвижности вещества, чем коэффициент подвижности Rf.
В качестве стандарта часто выбирают такое вещество, для которого в данных условиях Rf ≈ 0,5. По химической природе стандарт выбирается близким к разделяемым веществам. С применением стандарта величина RS обычно лежит в пределах 0,1 – 10, оптимальные пределы – от 0,5 до 2.
Для характеристики разделения двух компонентов А и В в данных условиях вводят степень (критерий) разделения:
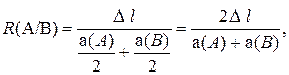 (3.8)
(3.8)
где ∆ l – расстояние между центрами пятен компонентов А и В; а(А) и а(В) – соответственно диаметры пятен А и В на хроматограмме (рис. 3.4).
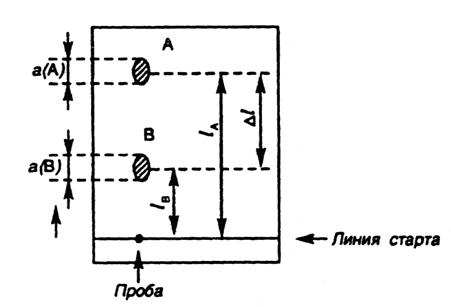
Рис. 3.4. Схема определения степени разделения R (A/B)
компонентов А и В
Чем больше величина R (A/B), тем четче разделяются пятна компо-нентов А и В на хроматограмме.
Для оценки селективности разделения двух веществ А и В исполь-зуют коэффициент разделения:
α = lB / lA. (3.9)
Если α = 1, то компоненты А и В не разделяются.
Бумажная хроматография позволяет проводить не только качественный, но и количественный анализ. На специальных приборах по интенсивности окраски пятен на бумаге можно судить о том, какова кон-центрация исследуемого вещества в анализируемой смеси.
3.4.2. Тонкослойная хроматография
Метод тонкослойной хроматографии (ТСХ) объединяет в себе ряд достоинств хроматографии на бумаге и адсорбционной хроматографии. В методе ТСХ твердая (неподвижная) фаза (силикагель, оксид алюминия, целлюлоза) наносится на подложку – пластинку из алюминиевой фольги, стекла, полиэфирной пленки. Анализируемая жидкая проба помещается на расстоянии 2 – 3 см от края пластинки, которая погружается в раство-ритель (подвижная фаза). Растворитель под действием капиллярных сил движется вдоль слоя сорбента и с разной скоростью переносит компоненты смеси, разделяя их. Сорбционные свойства системы в ТСХ также характеризуются подвижностью Rf, которая рассчитывается по формуле (3.7).
Выбор растворителя зависит от свойств анализируемых веществ и природы сорбента. Чаще всего применяют такие универсальные раствори-тели, как петролейный эфир, бензол, этиловый и другие спирты, диэтило-вый эфир, этилацетат, вода, а иногда также смеси из двух или трех компо-нентов. При анализе неорганических ионов в качестве растворителей могут применяться буферные растворы.
ТСХ выполняется как восходящая, нисходящая и горизонтальная хроматография. В первых двух случаях компоненты смеси после хромато-графирования располагаются в виде отдельных пятен; в последнем случае – в виде концентрических колец. Если разделяемые компоненты не имеют окраски, то зоны на хроматограмме проявляют химическим или физичес-ким способом. При химическом способе пластинку обрабатывают раство-ром реактива, который с компонентом смеси образует окрашенное соеди-нение. Физический способ проявления основан на том, что некоторые вещества способны флуоресцировать под действием ультрафиолетового облучения.
Для качественной идентификации веществ наиболее надежным способом является метод «свидетелей»: на стартовую площадку рядом с пробой наносят индивидуальные соединения, соответствующие предпола-гаемым компонентам смеси. Совпадение Rf компонента пробы и свидетеля является убедительным основанием для отождествления веществ.
Для количественного определения содержания компонентов в смеси возможны два варианта: анализ непосредственно на пластинке и после удаления вещества с пластинки. Наиболее точным является метод, когда определяемое вещество после разделение удаляется с пластинки (чаще всего механическим путем), а затем его содержание находят тем или иным методом количественного анализа. Для определения количества вещества непосредственно на пластинке используют фотометрический метод коли-чественного детектирования с помощью спектроденситометра. Спектро-денситометр позволяет установить содержание вещества в пятне путем измерения интенсивности отраженного света: белый свет сорбента отража-ет практически весь свет, а окрашенные пятна поглощают часть светового потока.
Более простой метод определения количества вещества в пятне состоит в измерении площади пятна. По предварительно построенному градуировочному графику зависимости площади пятна от массы вещества находят количество адсорбированного в пятне анализируемого компонен-та. При содержании вещества в пределах 1 – 80 мкг зависимость площади пятна от массы вещества линейная.
3.4.3. Качественный анализ смеси солей железа и кобальта (работа № 24)
Цель работы: ознакомление с основами плоскостной хроматогра-фии; разделение и идентификация ионов Fe3+ и Co2+ методом бумажной хроматографии.
Сущность метода. При движении элюента под действием капилляр-ных сил в тонком слое фильтровальной бумаги происходит разделение ионов железа и кобальта.
Оборудование: 1) камера для хроматографирования с крышкой; 2) капиллярная пипетка; 3) пинцет; 4) пульверизатор.
Реактивы: 1) хроматографическая бумага № 3 или 4 (полоска ши-риной 4 см, длиной 15 см); 2) раствор солей железа (III) и кобальта (II), содержащий по 2 мг/см3 каждого элемента; 3) элюент – смесь н -бутилового спирта (80% об.) и концентрированной соляной кислоты (20% об.); 4) проявитель – 1%-ный раствор роданида аммония в этаноле.
Ход работы. На полоске бумаги на расстоянии 15 мм от края отме-чают простым карандашом стартовую линию. На нее при помощи капил-лярной пипетки наносят каплю исследуемого раствора и сушат в сушиль-ном шкафу при 110 °С. В сосуд для хроматографирования вливают 20 см3 элюента, опускают в него полоску бумаги и фиксируют ее так, чтобы нижний конец был погружен в элюент на 2 – 3 мм, а края полоски не каса-лись стенок сосуда. Разделение продолжается 2 часа.
Когда фронт растворителя достигнет верхнего края полоски бумаги (не ближе 5 мм к верхнему краю), опыт прекращают, полоску бумаги вы-нимают и сушат. Высушенную бумагу опрыскивают из пульверизатора раствором роданида аммония (проявитель) и снова сушат. В случае присутствия ионов железа Fe3+ и кобальта Co2+ после опрыскивания появляются окрашенные пятна. Красное пятно соответствует ионам железа, голубое – ионам кобальта. Внешний вид хроматограмм соответ-ствует рис. 3.4. Проводят обмер хроматограмм. По формуле (3.7) рассчи-тывают коэффициент Rf для железа и кобальта. Затем по формулам (3.8) и (3.9) находят степень разделения R (Fe/Co) и коэффициент разделения α. Делают вывод о возможности разделения этих ионов методом бумажной хроматографии.
Контрольные вопросы
1. Механизм хроматографического разделения на бумаге и в тонком слое.
2. Восходящая, нисходящая, градиентная, двумерная хроматография. Особенности методики хроматографии на бумаге.
3. Выбор неподвижной и подвижной фаз, выбор проявителя.
4. Количественный анализ в тонкослойной и бумажной хроматографии.
3.4.4. Качественный анализ смеси катионов металлов (работа № 25)
Цель работы: ознакомление с основами плоскостной хроматогра-фии; разделение и идентификация катионов Co2+, Ni2+, Cu2+, Fe3+, Al3+, Zn2+.
Сущность метода. Различная сила взаимодействия катионов метал-лов с целлюлозой позволяет с помощью специально подобранного элюента разделить их в тонком слое хроматографической бумаги и идентифициро-вать по величине Rf.
Оборудование: 1) две камеры для хроматографирования (с крышка-ми); 2) капиллярная пипетка; 3) пинцет; 4) пульверизатор; 5) кисточка.
Реактивы: 1) хроматографическая бумага № 3 или 4 (полоска шири-ной 10 – 12 см, длиной 30 – 35 см); 2) растворы солей кобальта (II), никеля (II), меди (II), железа (III), алюминия и цинка, содержащие по 2 мг/см3 каждого металла; 3) элюент – смесь ацетона (87% об.), концен-трированной соляной кислоты (8% об.) и воды (5% об.); 4) проявитель – 1%-ный водный раствор сульфида аммония в этаноле; 5) раствор ализа-рина; 6) раствор дитизона в четыреххлористом углероде.
Ход работы. На полоске бумаги на расстоянии 15 мм от края отметьте простым карандашом стартовую линию. Разделите ее на 6 при-мерно равных отрезков, отметьте графитовым карандашом середины этих отрезков и пронумеруйте точки (рис. 3.5). Затем при помощи капиллярной пипетки нанесите по одной капле раствора каждого катиона на эти точки и дайте бумаге просохнуть. Запишите в лабораторный журнал номера точек, соответствующие нанесенным катионам.
В сосуд для хроматографирования налейте элюент так, чтобы слой его покрывал дно сосуда не более чем на 3 – 4 мм. Закрепите лист бумаги с нанесенными на нем пятнами катионов к крышке хроматографической камеры. Закройте камеру крышкой, обращая внимание на то, чтобы нижний край листа коснулся растворителя одновременно по всей ширине. Оставьте прибор на некоторое время, пока фронт растворителя не подни-мется до крышки сосуда.
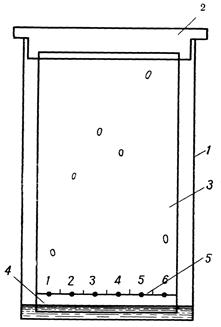
Рис. 3.5. Хроматографическая камера для качественного анализа смеси катионов металлов: 1– сосуд; 2 – крышка; 3 – лист хроматографической бумаги; 4 – растворитель; 5 – линия старта
Тем временем приготовьте тем же способом вторую хроматографи-ческую камеру, на стартовую линию нанесите несколько (5 – 6) пятен неизвестного раствора, полученного у инженера лаборатории, и тем же растворителем проведите хроматографическое разделение неизвестной смеси.
Как только в первой хроматографической камере фронт раствори-теля поднимется к верхней части бумаги, снимите крышку, освободите бумагу и отметьте карандашом положение фронта растворителя. Вместо карандаша можно пользоваться иголкой, делая проколы. Затем обработай-те хроматографическую бумагу из пульверизатора раствором сульфида аммония. Отметьте карандашом положение пятна каждого катиона. Запишите цвет каждого пятна и составьте уравнения реакций, происходя-щих при обработке бумаги сульфидом аммония. Отметьте, какие катионы не проявились сульфидом аммония.
Часть хроматограммы, относящуюся к иону алюминия, смочите при помощи кисточки раствором ализарина. Запишите свои наблюдения. Часть хроматограммы цинка обработайте раствором дитизона в четыреххлорис-том углероде. Отметьте положение и цвет пятен катионов.
После просушки хроматограммы измерьте длину фронта раствори-теля L и расстояние центра каждого пятна от стартовой линии li. Если пятно дает «хвост» или получилось очень большим, то положение центра пятна определить затруднительно. В этом случае измеряйте расстояние до верхнего края пятна. По формуле (3.7) вычислите относительную скорость передвижения пятна каждого катиона Rf, полученные данные занесите в табл. 3.4.
Таблица 3.4
Результаты определения коэффициента подвижности катионов металлов
| № точки | Катион | Rf |
| Co2+ Ni2+ Cu2+ Fe3+ Al3+ Zn2+ | … … … … … … |
Сделайте вывод об относительной силе взаимодействия каждого катиона с целлюлозой бумаги, расположите катионы в ряд в порядке убывания этой силы.
Когда фронт растворителя во второй хроматографической камере достигнет верхней части бумаги (опыт может быть прерван, даже если фронт растворителя находится ниже), выньте бумагу из сосуда и быстро отметьте карандашом положение фронта растворителя. Обработайте хроматографическую бумагу из пульверизатора раствором сульфида аммо-ния, отметьте положение проявившихся капель. Затем части хроматограм-мы, относящиеся к отдельным пятнам, обработайте кисточкой: одну – раствором ализарина, другую – раствором дитизона. Если появились новые пятна, отметьте их положение карандашом или проколом иголкой. Высушите хроматограмму, после чего измерьте длину фронта раствори-теля L и расстояние от стартовой линии li для каждого пятна. По формуле (3.7) вычислите относительные скорости передвижения Rf для всех пятен неизвестных катионов.
Сравните полученные значения с результатами предыдущего опыта. Сделайте вывод о катионном составе неизвестной смеси, проверьте резуль-тат анализа у инженера лаборатории.
Контрольные вопросы
1. В чем сущность распределительной хроматографии на бумаге?
2. Как рассчитывается и что характеризует коэффициент подвижнос-ти Rf?
3. Что является подвижной и неподвижной фазой в распределитель-ной жидкостной хроматографии на бумаге?
4. Как выполняют качественный и количественный анализ методом распределительной жидкостной хроматографии на бумаге?
5. Каковы области применения, достоинства и недостатки тонкослой-ной хроматографии?
 2015-01-30
2015-01-30 9179
9179








