Растворами называются молекулярно-дисперсные и ионно-дисперсные гомогенные системы, состоящие из двух и более химически индивидуальных веществ.
Концентрацией раствора называется количество растворенного вещества, содержащееся в единице массы или единице объема раствора.
Пример 1. Вычислите: а) массовую долю растворенного вещества (%); б) молярную концентрацию вещества (СМ, М); в) молярную концентрацию эквивалентов вещества (Сн); г) моляльность вещества в растворе (Сm), который получен растворением 60 г карбоната калия в 250 мл воды (плотность раствора r = 1190 кг/м3 = 1,19 г/см3 = 1,19 г/мл). Чему равен титр (Т) этого раствора?
Решение. а) массовая доля (w) показывает, сколько единиц массы растворенного вещества содержится в 100 единицах массы раствора. Массовая доля – безразмерная величина, ее выражают в долях единицы или в процентах.
Так как массу 250 мл воды можно принять равной 250 г (r 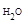 =1г/мл), то масса полученного раствора равна: 60 + 250 = 310 г и, следовательно:
=1г/мл), то масса полученного раствора равна: 60 + 250 = 310 г и, следовательно:
в 310 г раствора содержится 60 г К2СО3
в 100 г раствора содержится х г К2СО3
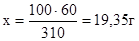
Таким образом, массовая доля К2СО3 равна 19,35 % (w 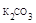 =19,35%).
=19,35%).
б) молярная концентрация вещества – отношение количества растворенного вещества (в молях) к объему раствора. Единица измерения молярной концентрации моль/л.
Для расчета молярной концентрации карбоната калия необходимо найти массу 1 л раствора: 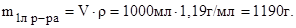
Массу карбоната калия (m) в 1 л раствора находим из соотношения:
в 310 г раствора содержится 60 г К2СО3
в 1190 г раствора содержится m г К2СО3
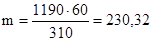 г К2СО3
г К2СО3
Число молей соли, содержащихся в 1 л раствора равно отношению: 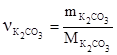 , где
, где 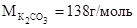 .
.
Следовательно, 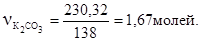
Молярная концентрация карбоната калия  (1,67М)
(1,67М)
в) молярная концентрация эквивалентов (нормальная концентрация) – отношение количества эквивалентов растворенного вещества (в молях эквивалентов) к объему раствора. Единица измерения моль/л.
Молярная масса эквивалента кислоты равна отношению ее молярной массы к основности. Например: 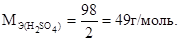
Молярная масса эквивалента основания равна отношению ее молярной массы к кислотности. Например: 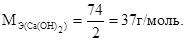
Молярная масса эквивалента соли равна отношению ее молярной массы к произведению числа атомов металла на валентность металла. Например:
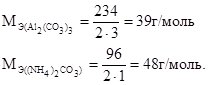
Так как молярная масса эквивалента карбоната калия равна: 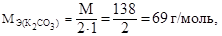 то число молей эквивалентов К2СО3, содержащихся в 1 л раствора равно отношению:
то число молей эквивалентов К2СО3, содержащихся в 1 л раствора равно отношению:
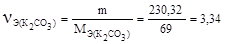 молей эквивалентов.
молей эквивалентов.
Молярная концентрация эквивалентов карбоната калия 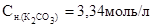 (3,34 н.)
(3,34 н.)
г) моляльность вещества в растворе – отношение количества растворенного вещества (в молях) к массе растворителя. Единица измерения моляльности вещества в растворе моль/кг.
Масса раствора складывается из суммы масс растворенного вещества и растворителя: mр-ра = mв-ва + mр-ля.
По условию задачи масса растворителя (воды) равна 250 г. Массу карбоната калия в 1000 г растворителя находим из соотношения:
на 250 г растворителя приходится 60 г К2СО3
на 1000 г растворителя приходится m г К2СО3
Отсюда, 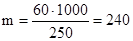 г К2СО3.
г К2СО3.
Число молей соли, содержащихся в 1000 г (1 кг) растворителя равно отношению: 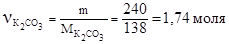
Моляльность карбоната калия в растворе Сm = 1,74 моль/кг
Титр раствора (Т) показывает количество граммов растворенного вещества, содержащегося в 1 мл (1 см3) раствора.
Так как в 1 л раствора карбоната калия содержится 230,32 г К2СО3, то 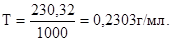
Пример 2. На нейтрализацию 20 мл раствора гидроксида калия, содержащего 0,4 г КOH, израсходовано 42 мл кислоты. Вычислите молярную концентрацию эквивалентов кислоты в растворе.
Решение. Согласно закону эквивалентов вещества взаимодействуют между собой в эквивалентных количествах, следовательно,
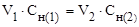 или
или 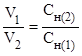
Таким образом, объемы растворов реагирующих веществ обратно пропорциональны их молярным концентрациям эквивалентов.
Рассчитываем молярную концентрацию эквивалентов гидроксида калия:
в 0,02 л раствора содержится 0,4 г КOH
в 1 л раствора содержится m г КOH
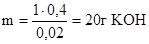
Число молей эквивалентов гидроксида калия, содержащихся в 1 л раствора, равно  молей эквивалентов, где 56 г/моль – молярная масса эквивалента гидроксида калия.
молей эквивалентов, где 56 г/моль – молярная масса эквивалента гидроксида калия.
Следовательно, молярная концентрация эквивалентов гидроксида калия Сн(КOH) = 0,36 моль/л.
На основании зависимости между объемами растворов реагирующих веществ и их молярными концентрациями эквивалентов рассчитываем молярную концентрацию эквивалентов кислоты:  ; отсюда
; отсюда
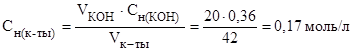 (0,17н.)
(0,17н.)
Пример 3. К 1 л раствора серной кислоты с массовой долей Н2SO4 12% (плотность 1,083 г/см3) прибавили 0,5 л раствора той же кислоты с массовой долей Н2SO4 8 % (плотность 1,055 г/см3).Объем смеси довели до 2 л. Вычислите молярную концентрацию серной кислоты в полученном растворе.
Решение. Масса 1 л раствора серной кислоты с массовой долей Н2SO4 12 % равна: 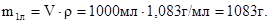
В этом растворе содержится 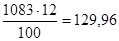 г Н2SO4.
г Н2SO4.
Масса 0,5 л раствора серной кислоты с массовой долей Н2SO4 8 % равна: 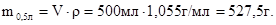 В этом растворе содержится
В этом растворе содержится 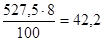 г Н2SO4.
г Н2SO4.
По условию задачи объем смеси довели до 2 литров, следовательно, в общем объеме полученного раствора (2 л) масса H2SO4 составляет
129,96 + 42,2 = 172,16 г.
Таким образом, в 1 л раствора содержится: 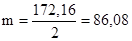 г Н2SO4. Рассчитаем число молей серной кислоты, содержащихся в 1 л раствора:
г Н2SO4. Рассчитаем число молей серной кислоты, содержащихся в 1 л раствора:
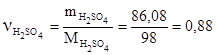 молей, где 98 г/моль – молярная масса H2SO4.
молей, где 98 г/моль – молярная масса H2SO4.
Следовательно, молярная концентрация серной кислоты в полученном растворе СМ = 0,88 моль/л (0,88М).
Пример 4. Какой объем хлороводородной кислоты с массовой долей HCl 36 % (r = 1,183 г/см3 = 1,183 г/мл) потребуется для приготовления 2,5л 0,5н. раствора этой кислоты?
Решение. Молярная масса эквивалента хлороводородной кислоты
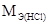 =
=  г/моль. Масса HCl, необходимая для приготовления 2 л 0,5н. раствора хлороводородной кислоты равна:
г/моль. Масса HCl, необходимая для приготовления 2 л 0,5н. раствора хлороводородной кислоты равна:
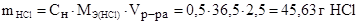
Находим, в каком количестве раствора хлороводородной кислоты с массовой долей 36 % содержится 45,63 г HCl:
в 100 г 36% - го раствора содержится 36 г HCl
в m г 36% - го раствора содержится 45,63 г HCl
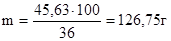
Следовательно, объем раствора хлороводородной кислоты с массовой долей HCl 36 % равен: 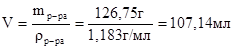
ЗАДАНИЯ
141. Вычислите молярную концентрацию, молярную концентрацию эквивалентов и титр раствора хлорида кальция с массовой долей СаCl2 20%, плотность раствора 1,178 г/см3.
142. Вычислите молярную концентрацию, молярную концентрацию эквивалентов, моляльность и титр раствора щелочи с массовой долей NaOH 30%. Плотность раствора щелочи 1,328 г/см3.
143. К 3 л раствора азотной кислоты (r = 1,054 г/см3) с массовой долей HNO3 10% прибавили 5 л раствора той же кислоты (r = 1,009 г/см3) с массовой долей HNO3 2%. Вычислите молярную концентрацию полученного раствора и массовую долю (%) HNO3 в этом растворе.
144. Вычислите молярную концентрацию, молярную концентрацию эквивалентов, моляльность и титр раствора азотной кислоты
(r = 1,120 г/см3) с массовой долей HNO3 20,8%.
145.Вычислите молярную концентрацию, молярную концентрацию эквивалентов, моляльность и титр раствора хлорида алюминия
(r=1,149 г/см3) с массовой долей AlCl3 16%.
146.Сколько и какого вещества останется в избытке, если к 7 мл 0,3н. раствора серной кислоты прибавить 125 мл 0,2н. раствора гидроксида калия.
147. Для осаждения в виде хлорида серебра всего серебра, содержащегося в 100 мл раствора нитрата серебра потребовалось 50 мл 0,2 н. раствора хлороводородной кислоты. Вычислите молярную концентрацию эквивалентов и титр раствора нитрата серебра.
148.Какой объем раствора хлороводородной кислоты (r=1,100 г/см3)
с массовой долей HCl 20,01% требуется для приготовления 1 л раствора
(r = 1,050 г/см3) с массовой долей HCl 10,17%?
149. Смешали 10 мл раствора азотной кислоты (r = 1,056 г/см3) с массовой долей HNO3 10% и 100 мл раствора той же кислоты
(r =1,184 г/см3) с массовой долей HNO3 30%. Вычислите молярную концентрацию и массовую долю (%) HNO3 в полученном растворе.
150.Какой объем раствора гидроксида калия (r = 1,056 г/см3) с массовой долей КОН 50% требуется для приготовления 3 л раствора
(r=1,048 г/см3) с массовой долей КОН6%?
151. Какой объем раствора карбоната натрия (r = 1,105 г/см3) с массовой долей Na2CО3 10% требуется для приготовления 5л раствора (r=1,020г/см3) с массовой долей Na2CО3 2%?
152.На нейтрализацию 31мл 0,16н. раствора щелочи требуется 217мл раствора серной кислоты. Вычислите молярную концентрацию эквивалентов и титр раствора серной кислоты.
153. Какой объем 0,3н. раствора кислоты требуется для нейтрализации раствора, содержащего 0,32 г NaOH в 40 мл раствора гидроксида натрия.
154. На нейтрализацию 1 л раствора, содержащего 1,4 г гидроксида калия, требуется 50 мл раствора кислоты. Вычислите молярную концентрацию эквивалентов кислоты.
155. Вычислите молярную концентрацию, молярную концентрацию эквивалентов, моляльность и титр раствора хлорида натрия
(r = 1,148 г/см3) с массовой долей NaCl 20%?
156. Вычислите молярную концентрацию, молярную концентрацию эквивалентов, моляльность и титр раствора серной кислоты
(r = 1,040 г/cм3), в 200 мл которого содержится 9 г Н2SО4.
157. Вычислите молярную концентрацию, молярную концентрацию эквивалентов, моляльность и титр раствора азотной кислоты
(r = 1,054 г/см3) с массовой долей HNO3 10%.
158. Какой объем раствора азотной кислоты (r = 1,367 г/см3) с массовой долей HNO3 60% требуется для приготовления 0,5 л раствора той же кислоты (r = 1,054 г/см3) с массовой долей HNO3 10%?
159. Смешали 50 мл раствора серной кислоты (r = 1,098 г/см3) с массовой долей Н2SО4 14% и 100 мл раствора той же кислоты
(r = 1,224 г/см3) с массовой долей Н2SО4 30%. Вычислите молярную концентрацию и массовую долю (%) Н2SО4 в полученном растворе.
160. Смешали 25 мл раствора хлорида натрия (r = 1,029 г/см3) с массовой долей NaCl 4% и 225 мл раствора той же соли (r = 1,151 г/см3) с массовой долей NaCl 20%. Вычислите молярную концентрацию и массовую долю (%) NaCl в полученном растворе.
 2015-01-30
2015-01-30 1678
1678
