В четырехвалентном состоянии уран образует ряд минералов. В основном, это первичные минералы, среди которых важное место занимает уранинит – UO2. Кроме того, четырехвалентный уран встречается в серии сложных танталатов, ниобатов, в различных окислах, фосфатах редкоземельных элементов, где он изоморфно замещает редкоземельные.
Минералы U(IV) имеют слабую растворимость; в природных условиях они трудно поддаются выветриванию. На воздухе двуокись урана UO2 медленно окисляется, образуя UO3.
В растворах U(IV) неустойчив, легко окисляется до шестивалентного состояния. Устойчив он в природных условиях только в сильнокислых сульфатной и хлоридной средах, однако, в отсутствии окислителей.
Например, в присутствии окислителя Fe3+ в кислой среде U(IV) легко окисляется:
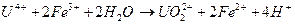
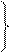
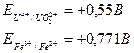 åЕ>0
åЕ>0
Кислород воздуха также окисляет четырехвалентный уран, причем скорость окисления в значительной степени зависит от кислотности среды, так как сопровождается освобождением протонов или связыванием гидроксильных ионов:
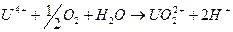
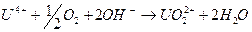
В слабокислых растворах скорость окисления выше, чем в сильнокислых, ускорение окисления в слабокислых и нейтральных средах объясняется появлением кислородсодержащих гидролизованных форм U4+ типа U(OH)3+ и других, окисление которых до кислородсодержащих ионов пяти и шестивалентного урана, т.е. UO2+ и UO22+, происходит легче, чем негидролизованных ионов U4+ /4/.
Устойчивость U(IV) в сильнокислых сульфатных и хлоридных растворах объясняется процессами комплексообразования: в присутствии ионов SO42- и Cl- происходит стабилизация четырехвалентного состояния урана вследствие того, что ионы U(IV) более склонны к комплексообразованию с этими лигандами, чем ионы UO22+ /4/.
Для сульфатных комплексов U(IV) характерна недостаточно прочная внутренняя сфера, на которую оказывают значительное влияния солевой состав раствора, избыток или недостаток сульфатогрупп, температура, кислотность, присутствие других лигандов и т.д.. В достаточно концентрированных по сульфат-ионам растворах образуются анионные комплексы состава:
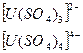
В разбавленных растворах полярные молекулы воды, находясь в громадном концентрационном избытке, вытесняют сульфато-группы с образованием аква-сульфатных анионных и нейтральных комплексов:
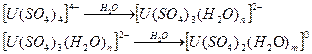
Вытеснение сульфато-групп может происходить и дальше с образованием в конце концов аква-комплекса /5/:
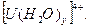
В водных растворах соли четырехвалентного урана сильно гидролизуются, придавая раствору кислую реакцию. Установлено /6/, что гидролиз протекает по схеме:
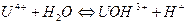
При глубоком гидролизе образуется гидроокись U(OH)4.
В содовой среде в присутствии карбонат-ионов U(IV) образует карбонатные комплексы. Для соединений урана (IV) характерна высокая растворимость в избытке концентрированных растворов карбонатов щелочных металлов, аммония. В карбонатных растворах процесс окисления U(IV) происходит быстрее, чем в сульфатных. Высокое значение рН карбонатных растворов способствует протеканию реакций гидролиза, который усиливается при разбавлении, подщелачивании и подкислении /5/.
 2015-01-30
2015-01-30 408
408








