Эта стадия закисления характеризуется изменением рН растворов от 4,5 до 1,5-1,0.
На этой стадии закисления серная кислота в активной зоне выщелачивания большей частью растворила находящиеся в породе карбонаты и расходуется на растворение минералов урана и тех составляющих породы, которые растворяются в этой области рН. Химические реакции серной кислоты с породообразующими компонентами те же, что и реакции, описанные в первой и во второй стадии, происходящие в первой подзоне активной зоны выщелачивания. Однако растворение этих компонентов с увеличением концентрации серной кислоты увеличивается, что является негативным явлением.
В этой области рН начинает интенсивно выщелачиваться уран.
Оптимальной концентрацией серной кислоты является область со значением рН, равным 1,5 – 2,0 /27/. Выше этой области рН уран может осаждаться в виде гидроксила уранила (рН = 4-7), в виде фосфата уранила (рН = 1,9-2,5), в виде арсената уранила (рН = 1,3-1,7), а также может соосаждаться за счет окклюзии с гидроокисями железа и алюминия (рН = 2-4).
При этом возможно образование минералов /19/:
отенита Ca(UO2)2 РO8 .12H2O
цейнерита Cu(UO2)2 As2O8 . 12H2O
карнотита К2(UO2)2 U3O8 . 3H2O
Увеличение кислотности ниже области рН = 1,5 приводит к большому расходу килоты на взаимодействие с породосотавляющими, что приводит к увеличению солевого состава растворов и усложняет дальнейшую переработку.
Итак, в области рН = 1,5-2,0 трехокись урана хорошо растворяется. При этом наиболее вероятно протекание реакции /5/:
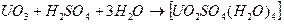 .
.
Также при растворении UO3 возможно образование ряда генетически связанных между собой комплексов /17/:
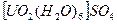
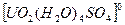
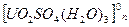
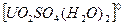
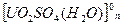
В этой области рН при наличии в растворе ионов трехвалентного железа интенсивно выщелачивается двуокись урана.
В работе /18/ изучено влияние ионов Fe(III) на растворение UO2.
Найдено, что в отсутствие ионов Fe(III) в пределах рН от 3,5 и до отрицательной области (H2SO4=200 г/л) процесс растворения UO2 практически не протекает. При введении Fe(III) в раствор степень растворения UO2 в области рН от 2,0 до 0,3 высокая:
рН Растворено UO2, %
2,0 49,2
1,5 71,9
1,2 69,2
0,95 63,1
0,60 51,0
0,30 48,0
Из этих данных видно, что оптимальной областью рН при растворении двуокиси урана серной кислотой в присутствии трехвалентного железа является область от 1,0 до 1,5. Объясняется это тем, что в процессе окисления принимают участие гидролизованные ионы Fe(III), а именно Fe(OH)2+ и Fe(OH)2+.
При этом процесс окисления описывается уравнениями:

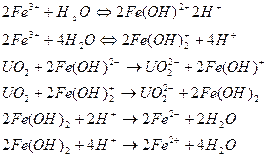
В работе /20/ отмечается, что в присутствии ионов SO42- (растворимые сульфаты), ClO4-, H+ наблюдается окисление двуокиси урана трехвалентным железом.
В этой области рН может происходить растворение силикатов четырехвалентного железа с переходом его в раствор. однако, состояние U(IV) в растворе неустойчивое, он легко окисляется трехвалентным железом от уранил-иона.
В области рН = 2-3 в сернокислых растворах уран (VI) может восстанавливаться органическими веществами, находящимися в породе, в частности, древесиной. В процессе углификации органического вещества от органики отщепляются такие продукты, как СО2, Н2О, NH4, H2S, тяжелые углеводороды. Почти все элементы, входящие в состав органических веществ и продуктов их углификации, обладают переменной валентностью (N, C, S) и в соответствии с этим - способностью участвовать в окислительно-восстановительных реакциях. Кроме того, восстановительной способностью обладают активные группы, входящие в молекулу органического вещества (спиртовые группы, альдегидные и т.д.)
Процесс восстановления уранила органическим веществом можно представить реакциями /21/:
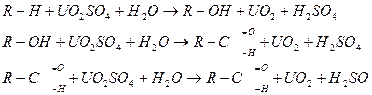
где R – органический радикал
В работе /21/ изучено восстановление урана на природных органических веществах. Найдено, что рН среды и характер органического вещества сильно влияют на процесс восстановления урана. Так, например, в кислой среде торф, древесина и целлюлоза наиболее интенсивно восстанавливают уран. Данные восстановления приведены в таблице:
| № опыта | Наименование Органического восстановителя | РН водной среды | Е (мв) водной среды | % восстановления урана | ||
| До опыта | После опыта | До опыта | После опыта | |||
| Торф | 2,18 | 3,24 | +356 | +274 | 97,5 | |
| Торф | 5,15 | 4,78 | +182 | +195 | 97,0 | |
| Торф | 7,06 | 7,36 | +51 | +57 | 54,8 | |
| Древесина | 2,55 | 2,80 | +315 | +313 | 93,5 | |
| Древесина | 5,15 | 5,12 | +150 | +163 | - | |
| Древесина | 7,71 | 7,30 | -32 | +61 | 78,5 | |
| Кероген сланца | 2,90 | 5,43 | +270 | +154 | 73,7 | |
| Кероген сланца | 4,86 | 6,56 | +177 | +94 | 100,0 | |
| Кероген сланца | 6,76 | 6,82 | +66 | +68 | 100,0 | |
| Целлюлоза | 2,82 | 3,08 | +307 | +324 | 96,4 | |
| Целлюлоза | 5,52 | 4,83 | +141 | +201 | 93,7 | |
| Целлюлоза | 7,36 | 8,02 | +36 | -16 | 93,7 | |
| Оксицеллюлоза | 2,59 | 2,86 | +325 | +347 | 80,0 | |
| Оксицеллюлоза | 4,96 | 4,52 | +206 | +197 | 65,1 | |
| Оксицеллюлоза | 7,95 | 8,07 | -28 | -10 | 73,6 | |
| Крахмал | 3,01 | 2,90 | +304 | +314 | 43,9 | |
| Крахмал | 5,46 | 4,70 | +152 | +202 | 83,2 | |
| Крахмал | 7,68 | 6,37 | +22 | +73 | 96,0 |
В этой работе сделан вывод, что сопряженные процессы окисления – восстановления в гетерогенных системах с нерастворимыми органическими веществами проходят не в растворе, а на поверхности твердой фазы. Вступая в контакт с активными группами органического вещества, уран (VI) переходит из раствора в твердую фазу, давая соответствующие внутрикомплексные или солеобразные соединения.
Находясь в составе уран-органического комплекса, шестивалентный уран восстанавливается до четырехвалентного, окисляя органическое вещество с образованием новых активных групп. В результате равновесие все время сдвигается в сторону извлечения новых количеств солей урана (VI) из водного раствора и перехода его через стадию уран-органических соединений типа комплексов или солей в состояние уран (IV) в виде нерастворимых черней. Последние накапливаются в наиболее активных местах органического вещества. Процесс идет до тех пор, пока не будет израсходовано органическое вещество или не прекратится поступление новых порций раствора урана (VI).
Следовательно, в природных условиях компоненты растительной ткани и продукты её окислительных превращений могут явиться непосредственными восстановителями урана без обязательного участия в этих процессах сероводорода.
При снижении рН раствора менее 4,5 растворяются выпавшие ранее в осадок гидроокиси железа, алюминия:
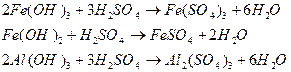
Таким образом, третья стадия закисления характеризуется следующими признаками:
1. рН откачных растворов снижается в пределах от 4,5 до 1,5 и стабилизируется при значении 1,5-2,0.
2. В продуктивных растворах наблюдается высокое содержание урана. Состояние урана в растворе устойчивое, уран присутствует в основном в виде сульфатных аква-комплексов уранила.
3. В растворе повышается содержание ионов Fe3+, Fe2+, Al3+.
4. Наблюдается увеличение коэффициента фильтрации выщелачиваемой зоны за счет химической декольматации.
 2015-01-30
2015-01-30 616
616








