Весьма привлекательным с точки зрения сохранения проницаемости и устранения выделения осадков кальцита в недрах на насосах и другом поверхностном оборудовании является получение растворителя, который образуется путём насыщения воды газообразным CO2 и окислителем.
В процессе используется раствор угольной кислоты с концентрацией, достаточной для поддержания рН раствора ~ 7. Максимальная концентрация не должна превышать значения, при котором количество образующегося карбоната кальция будет выше его растворимости в растворе выщелачивания; в противном случае произойдет образование осадков. Максимальная концентрация угольной кислоты варьируется широко в зависимости от количества кальция в залежи, типа используемой воды для приготовления растворов, отношение объёма закачиваемого раствора к объёму откачиваемого и других факторов. Общепринятой мерой содержания угольной кислоты является количество бикарбонат-иона, образующегося в растворе. Обычно концентрация угольной кислоты, выражаемая в виде бикарбонат-иона, составляет 300 – 1000 мг/л, а предпочтительно от 460 до 700 мг/л.
Окислитель может быть введён перед или одновременно с раствором выщелачивания в как в виде газа, так и в виде раствора. Однако предпочтительно вводить окислитель и растворитель одновременно, растворяя окислитель в растворителе выщелачивания. Предпочтительная концентрация окислителя (на основе свободного кислорода) – 50 – 200 мг/л. В качестве окислителя могут использоваться перманганат калия, ферроцианид калия, гипохлорит натрия, пероксисульфат калия, перекись водорода, кислород и кислородосодержащие газы. Последние могут быть предварительно растворены в воде или растворе выщелачивания. Перекись водорода и кислород являются наиболее предпочтительными окислителями. В организации процесса важно сохранение значения рН. Соли кальция выносятся из породы и переходят в раствор; когда их концентрация превышает предел растворимости для данного раствора выщелачивания, они осаждаются, вызывая химическую кольматацию. Следовательно, возникает необходимость добавки «умягчённой» воды для разбавления содержания кальция и других солей в растворе выщелачивания. Это совершается либо введением дополнительной воды из пласта в систему, либо откачкой большего объёма раствора по сравнению с закачкой (более предпочтительно) или же добавкой воды в растворы после сорбции. В том и в другом случаях некоторое количество раствора выводится из системы и сбрасывается; таким образом, общий объём раствора выщелачивания в системе сохранятся неизменным. Несмотря на эти меры, в некоторых скважинах могут образовываться осадки, снижаемую приемистость. В этих случаях следует подавать прямо в скважину под давлением CO2, в результате рН раствора снизится, и произойдет растворение карбонатов кальция. Эта обработка идентична традиционной кислотной обработке.
На практике готовят раствор угольной кислоты централизованно и используют подводку для индивидуальной обработки скважин, если в них отмечается кольматация.
Использование угольной кислоты широко распространено в практике ПВ урана в США. Опытные испытания выявили ряд несомненных преимуществ этого растворителя. Он в наименьшей степени влияет на недра и не вызывает набухания глин, обеспечивает наиболее легкое восстановление водоносного горизонта после выщелачивания, чем любой другой растворитель. По молярному эквиваленту является самым дешёвым растворителем. Однако он не может быть рекомендован повсеместно для выщелачивания урана. По опыту работы отдельных компаний США, он с успехом может быть использован на месторождениях, имеющих чистые пески, но не столь эффективен там, где присутствует много органического углерода. По предварительным данным, на рудах штата Вайоминг в лабораторных условиях выщелачивание урана этим растворителем происходит медленнее, чем карбонат-бикарбонатом аммония. На некоторых месторождениях, как утверждают отдельные владельцы, этот растворитель эффективнее чем карбонат-бикарбонат аммония.
Продуцируемый растворитель, получаемый пропусканием CO2 через подземную воду, не представляет собой чистую угольную кислоту. Растворённый CO2 наиболее эффективен там, где в подземной воде содержится достаточное количество карбонатов, чтобы служить в качестве буфера и образовывать бикарбонаты.
Реакции, протекающие при этом на первой стадии:
CO2 + Na2CO3 + H2O 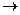 2Na2CO3,
2Na2CO3,
CO2 + K2CO3 + H2O 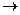 2Na2CO3,
2Na2CO3,
а затем:
CO2 +H2O 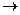 H2CO3.х
H2CO3.х
Значение рН растворов обычно 6,5 –7,5.
Для большинства процессов отношение количества потребляемого CO2 к количеству производимой закиси-окиси урана составляет 5 – 10 %.
Для получения наиболее высокого результата от использования CO2 необходимо иметь эффективную систему растворения газа в виде очень мелких пузырьков в растворителе. В противном случае потери CO2 могут составлять около 50% пропускаемого газа. Это особенно важно, так как величина пропускаемого рН поддерживается обычно вблизи нейтрального значения. Дополнительные затраты связаны с хранением CO2, так как жидкий газ требует специальной ёмкости и оборудования для охлаждения.
Рассмотренный процесс имеет неоценимое преимущество, позволяя исключить использование иона NH4+, который в недрах обменивается на ионы Са и Na, создавая загрязняя подземные воды. Система СО2/О2 особенно приемлема для месторождений, в которых расход окислителя невелик. Однако установлено, что многие урановые месторождения содержат значительные количества восстановителей, таких как H2S и другие сульфиды, органические вещества, которые действуют как поглотители кислорода. Многие ролловые образования, пригодные для ПВ урана, содержат также FeS2 и MoS2. Эти и вышеперечисленные соединения предпочтительно потребляют кислород, подавляя растворение урана до тех пор, пока большинство из этих “поглотителей” не будет окислено. Побочная реакция с молибденитом MoS2 вызывает загрязнение желтого кека, так как, продуцируя кислоту, потребляет кислород по реакции:
MoS2(тв.) + 9[O] +3H2O 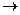 MoO4-2 + 6H+ + 2SO4-2
MoO4-2 + 6H+ + 2SO4-2
Во многих случаях восстановительная ёмкость столь высока, что скорость выщелачивания лимитируется подачей кислорода. Это особенно проявляется для систем выщелачивания СО2/О2, так как растворимость О2 в растворе выщелачивания низка, а поглощение О2 наиболее интенсивно происходит на первых стадиях выщелачивания. В типичном процессе ПВ, когда растворитель подаётся в одну скважину, а продуктивный раствор откачивается из других скважин, расположенных на расстоянии, при карбонатном выщелачивании уран переходит в раствор лишь после полного окисления пласта. С получения продуктивных растворов с повышенным содержанием урана предлагается окислять соединения - «поглотители» в пласте до начала процесса выщелачивания. Перед выщелачиванием в пласт вводится газообразный кислород или воздух, которые “протягиваются” до появления их в откачной скважине. Затем скважины закрываются на некоторый период времени, чтобы О2 в недрах мог окислить восстановители в рудах и поровой воде. С целью контроля расходования кислорода непрерывно осуществляют измерения значения ОВП воды. В случае недостатка кислорода он может быть вновь введён в пласт. На стадии предварительного окисления добыча урана не производится, откачивается лишь минимальное количество воды. После завершения этой стадии окисления начинается обычный процесс выщелачивания с CO2/О2.
Смесь газов CO2/О2 может использоваться также для доизвлечения урана. Целесообразно обработку смесью газов производить после снижения содержания урана в растворах откачки ниже предельного уровня. Молярное отношение СО2:О2 может быть от 0,001: 1 до 100: 1.
Процесс можно интенсифицировать путем закачки в рудное тело смеси углекислого газа и кислорода и выдерживании без откачки в течение от одного дня до одного месяца и дольше. Затем процесс выщелачивания вновь возобновляется. Эта схема позволяет увеличить извлечение урана из упорных руд и повысить содержание его в товарных растворах.
Скорость выщелачивания урана в системе CO2/О2 может быть увеличена введением в систему сульфат-иона. Он вводится в начале выщелачивания и рециркулирует в течение всего процесса без дополнительного ввода SO42- В некоторых рудных залежах, богатых FeS2 или другими соединениями серы, сульфат-ион получается в виде побочного продукта окисления.
 2015-01-30
2015-01-30 830
830








