1. По результатам титрований находят средние значения m(Na2CO3) и m(NaOH) из серии параллельных определений.
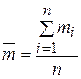
2. Рассчитать абсолютную и относительную ошибку определения, сравнив полученные результаты, с истинным значением, выданным лаборантом.
Абсолютная ошибка составляет:
d = m – mист.
Относительную ошибку определения вычисляют по формуле
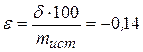 %
%
Контрольные вопросы
1. Дайте определение понятию «массовая доля растворенного вещества»; молярная концентрация; молярная концентрация эквивалента (эквивалентная концентрация).
2. Вычислите молярные массы эквивалентов и факторы эквивалентности в реакциях полной нейтрализации следующих веществ: HNO3; NH3; H2SO4; KHSO4; Na2CO3.
3. Рассчитайте объем 0,1 н. HNO3, необходимой для нейтрализации 5,3 г Na2CO3.
4. Расчет рН слабых и сильных кислот и оснований в водных растворах.
5. Буферные растворы, используемые в химическом анализе, их состав, свойства, расчет рН. Буферная емкость.
6. Использование реакций гидролиза в анализе. Принцип расчета рН гидролизующихся солей.
7. Кривые кислотно-основного титрования, расчет и построение теоретических кривых титрования сильных и слабых кислот и оснований.
8. Скачок кислотно-основного титрования. Способы индикации конечной точки титрования.
9. Кислотно-основные индикаторы, механизм изменения их окраски. Интервал перехода окраски индикатора. Показатель титрования рТ. Правило выбора индикатора по теоретическим кривым титрования. Примеры двухцветных и одноцветных индикаторов.
 2015-01-30
2015-01-30 714
714








