1. Составьте электронную формулу атомов железа, графически укажите валентные электроны в нормальном и возбужденном состояниях. Какие степени окисления может проявлять атом железа? Приведите примеры оксидов и гидроксидов железа в соответствующих степенях окисления, укажите их характер.
2. Установите правильную последовательность действий при определении типа гибридизации Ц.А. в частице:
1. Определите тип гибридизации;
2. Вычислите ст. ок., Ц.А. и число неспаренных (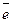 );
);
3. Найдите Ц.А. в частице;
4. Укажите К.Ч. (Ц.А.) и число 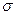 связей;
связей;
5. Графически изобразите валентные (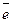 ) Ц.А. в соответствующей степени окисления.
) Ц.А. в соответствующей степени окисления.
6. Определите валентные электроны, участвующие в образовании связей в периферийных атомах и покажите их перекрывание с ГАО Ц.А.
7. Изобразите структурную формулу, указывающую геометрию частицы.
Установите соответствие:
3. Тип гибридизации Ц.А. Частица
1) sp2 a) Н2О
2) sp3 б) ВН3
3) sp3d в) SCl6
4) sp3d2 г) CO
5) sp д) PCl5
Рассмотрите по алгоритму те частицы, в которых Ц.А. в sp3 и sp3d гибридизации.
Укажите номер правильного ответа:
4. Если в момент химического равновесия 2NO + O2 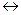 2NO2 концентрации NO, O2 и NO2 соответственно равны 8 моль/л., 6 моль/л., 4 моль/л., то начальные концентрации исходных веществ (NO и O2) были:
2NO2 концентрации NO, O2 и NO2 соответственно равны 8 моль/л., 6 моль/л., 4 моль/л., то начальные концентрации исходных веществ (NO и O2) были:
5) 12 моль/л и 8 моль/л
6) 14 моль/л и 8 моль/л
7) 16 моль/л и 12 моль/л
8) 32 моль/л и 24 моль/л
5. Окисление аммиака протекает по уравнению:
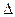 Н обр. 4NH3 + 3O2 = 2N2 + 6 H2O
Н обр. 4NH3 + 3O2 = 2N2 + 6 H2O 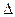 Н x.p. = -1528 кДж
Н x.p. = -1528 кДж
кДж/моль г г г ж (-285,84)
теплота образования аммиака (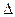 Н0 обр.(NH3)) равна:
Н0 обр.(NH3)) равна:
1) -92,15 кДж/моль
2) 92,15 кДж/моль
3) 46,76 кДж/моль
4) -46,76 кДж/моль
6. Реакция восстановления оксида меди (II) алюминием возможна
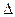 G0 обр. 3CuO + 2Al = Al2O3 + 3Cu
G0 обр. 3CuO + 2Al = Al2O3 + 3Cu
кДж/моль -129,8 -1582
свободная энергия Гиббса (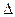 G х.р.) равна:
G х.р.) равна:
1) -1192 кДж
2) -3576 кДж
3) +1192 кДж
4) +3576 кДж
7. Массовая доля уксусной кислоты в растворе, полученном при смешивании 300 г 20%-ного раствора, равна_____________г
| 1) 16,7 | 2) 8,45 | 3) 33,4 | 4) 20,5 |
8. Объём 0,1 н раствора NaOH необходимый для нейтрализации 20 мл 0,15 н раствора уксусной кислоты, равен ______г
| 1) 30 | 2) 25 | 3) 50 | 4) 40 |
9. При температуре 200С давление насыщенного пара бензола равно 100 кПа. Давление насыщенного пара над раствором бензола (М = 78 г/моль), в 83 г которого содержится 12,8 г нафталина (М = 128 г/моль) составляет ___г
| 1) 100 | 2) 99 | 3) 90 | 4) 80 |
10.Осмотическое давление раствора, содержащего 0,2 г растворённого вещества в 300 мл раствора при 270С равно 27,7 кПа. Молярная масса растворённого вещества равна _____г
| 1) 60 | 2) 30 | 3) 90 | 4) 66 |
11. Для того, чтобы повысилась температура кипения воды на 1,040С, необходимо в 500 г растворить _________________ граммов глюкозы (М = 180 г/моль). Е (Н2О) = 0,52 (град·кг)/моль.
| 1) 180 | 2) 362 | 3) 90 | 4) 250 |
12. При взаимодействии 1 моль ортофосфорной кислоты с 1 моль гидроксида натрия образуется:
1) ортофосфат натрия 3) дигидроортофосфат натрия
2) гидроортофосфат натрия 4) фосфат натрия
Составьте молекулярно-ионные уравнения реакций. Сумма всех коэффициентов в кратком ионном уравнении равна________
13. Метилоранж становится желтым при растворении в воде каждой из двух солей:
1) K2S и K3PO4 3) LiCl и FeSO4
2) KNO3 и K3PO4 4) CH3COOK и K2SO4
Составьте молекулярно-ионные уравнения реакций гидролиза.
14. При взаимодействии водных растворов солей сульфата алюминия и карбоната натрия, сумма коэффициентов в кратком ионном уравнении равна:
1) 10 2) 12 3) 13 4) 9
15. Кислая среда образуется при растворении в воде каждой из двух солей:
1) BaCl2 и AlCl3 3) CuCl2 и LiCl
2) K2S и K3PO4 4) NH4NO3 и Zn(NO3)2
Составьте молекулярно-ионные уравнения гидролиза, выведите константу гидролиза по первой ступени.
16. В уравнении реакции, схема которой
 FeSO4 + KMnO4 + H2SO4 Fe2(SO4)3 + MnSO4 + K2SO4 + H2O,
FeSO4 + KMnO4 + H2SO4 Fe2(SO4)3 + MnSO4 + K2SO4 + H2O,
сумма коэффициентов перед формулами исходных веществ равна:
1) 20 2) 18 3) 25 4) 22
Используйте ионно-электронный метод.
17. В Г.Э. Ag | AgNO3 | | Fe(NO3)2 | Fe укажите процессы на электродах:
1) Fe0 – 2e ® Fe2+
2) Fe2+ + 2e ® Fe0
3) Ag0 – 1e ® Ag+
4) Ag+ + 1e ® Ag0
Рассчитайте ЭДС при н.у.
18. При электролизе раствора сульфата цинка с графитовым анодом и катодом на катоде выделится:
| 1) цинк 2) водород | 3) кислород 4) цинк и водород |
19. Рассмотрите электролиз раствора нитрата серебра, если:
а) графитовые электроды
б) серебряный анод
20. Протектором для железа может быть:
1) хром 2) олово 3) серебро 4) золото
Условно - графическая схема Г.Э. ______ в кислой среде, химизм процессов на электродах ___________
21. В системе при рН < 7, если корродирует железо:
 1) Fe – A 3) Pb – A
1) Fe – A 3) Pb – A
2) Cr – K 4) Pb – K Cr Fe Pb
Г.Э. имеет условно-графическую схему ______
Химизм процессов на электродах____________
СПИСОК РЕКОМЕНДУЕМОЙ ЛИТЕРАТУРЫ
1. Глинка, Н. Л. Общая химия: учебник для бакалавров / Н. Л. Глинка; под ред.: В. А. Попкова, А. В. Бабкова. - 19-е изд., перераб. и доп. - Москва: Юрайт, 2014. - 900 с.
2. Глинка, Н. Л. Задачи и упражнения по общей химии: учеб. пособие / Н. Л. Глинка. - Изд. стер. - М.: КноРус, 2012. - 240 с.
3. Князев, Д. А. Неорганическая химия: учебник для бакалавров / Д.А. Князев, С.Н. Смарыгин. - 4-е изд. - Москв: Юрайт, 2012. - 587 с.
4. Пресс, И. А. Основы общей химии для самостоятельного изучения: учебное пособие / И.А. Пресс. - Изд. 2-е, перераб. - Санкт-Петербург; Москва; Краснодар: Лань, 2012. - 492 с.
5. Глинка, Н. Л. Общая химия: [учеб. пособие] / Н. Л. Глинка. - М.: КноРус, 2011. - 746 с.
6. Павлов, Н. Н. Общая и неорганическая химия: учебник / Н.Н. Павлов. - Изд. 3-е, испр. и доп. - Санкт-Петербург; Москва; Краснодар: Лань, 2011. - 493 с.
7. Кодолов, В. И. Основы общей химии / В.И. Кодолов. - Ижевск: ИжГТУ, 2010. - 396 с.
8. Хомченко, Г. П. Неорганическая химия: учебник / Г.П. Хомченко, И.К. Цитович. - Изд. 2-е, перераб. и доп., репр. - СПб.: Квадро, 2009. - 460 с.
9. Коровин, Н. В. Общая химия: учебник / Н. В. Коровин. - Изд. 10-е, доп. - М.: Высш. шк., 2008. - 557 с.
10. Задачи и упражнения по общей химии: учеб. пособие для вузов / [Адамсон Б. И. и др.]; под ред. Н.В. Коровина. - Изд. 2-е, испр. - М.: Высш. шк., 2004. - 255 с.
ПРИЛОЖЕНИЕ А
Таблица А.1 - Стандартные электродные потенциалы металлов
| Металл | Электродный процесс | φ0298, В |
| Li | Li ↔ Li+ + ē | -3,045 |
| Rb | Rb ↔ Rb + + ē | -2,925 |
| К | K ↔ K + + ē | -2,924 |
| Cs | Cs ↔ Cs + + ē | -2,923 |
| Ra | Ra ↔Ra2++2 ē | -2,92 |
| Ва | Ba ↔ Ba2+ + 2 ē | -2,905 |
| Sr | Sr ↔ Sr2+ + 2 ē | -2,888 |
| Са | Ca ↔ Ca2++2 ē | -2,886 |
| Na | Na ↔ Na + + ē | -2,714 |
| La | La ↔ La3++3 ē | -2,522 |
| Се | Се ↔ Се3+ + З ē | -2,48 |
| Mg | Mg ↔ Mg2+ + 2 ē | -2,363 |
| Sc | Sс ↔ Sc3+ + 3 ē | -2,077 |
| Ru | Ru ↔ Ru3++3 ē | -2,031 |
| Th | Th ↔ Th4+ + 4 ē | -1,899 |
| Be | Be ↔ Be2+ + 2 ē | -1,850 |
| Hf | Hf ↔ Hf4+ + 4 ē | -1,700 |
| Al | Al ↔ Al3+ + 3 ē | -1,66 |
| Ti | Ti ↔ Ti2+ + 2 ē | -1,63 |
| Zr | Zr ↔ Zr2+ + 4 ē | -1,539 |
| Mn | Mn ↔ Mn2++2 ē | -1,179 |
| V | V ↔ V2++2 ē | -1,175 |
| Nb | Nb ↔ Nb3++3 ē | -1,1 |
| Cr | Cr ↔ Cr2++2 ē | -0,913 |
| Zn | Zn ↔ Zn2+ + 2 ē | -0,763 |
| Cr | Cr ↔ Cr3++3 ē | -0,744 |
| Ga | Ga ↔ Ga3+ + 3 ē | -0,53 |
| Fe | Fe ↔ Fe2++2 ē | -0,44 |
| Cd | Cd ↔ Cd2++2 ē | -0,40 |
| Tl | Т1↔ Тl+ + ē | -0,336 |
| Co | Co ↔ Co2+ + 2 ē | -0,277 |
| Ni | Ni ↔ Ni2++2 ē | -0,250 |
| Mo | Mo ↔ Mo3++3 ē | -0,200 |
| Sn | Sn ↔ Sn2+ + 2 ē | -0,136 |
| Pb | Pb ↔ Pb2+ + 2 ē | -0,126 |
| Fe | Fe ↔ Fe3++3 ē | -0,037 |
| H2 | H2 ↔ 2H + +2 ē | 0,00 |
| W | W ↔ W3++3 ē | +0,11 |
| Sb | Sb ↔ Sb2++2 ē | +0,15 |
| Bi | Bi ↔ Bi3++3 ē | +0,215 |
| Cu | Cu ↔ Cu2+ + 2 ē | +0,34 |
| Re | Re ↔ Re3++3 ē | +0,3 |
 2015-01-07
2015-01-07 841
841








