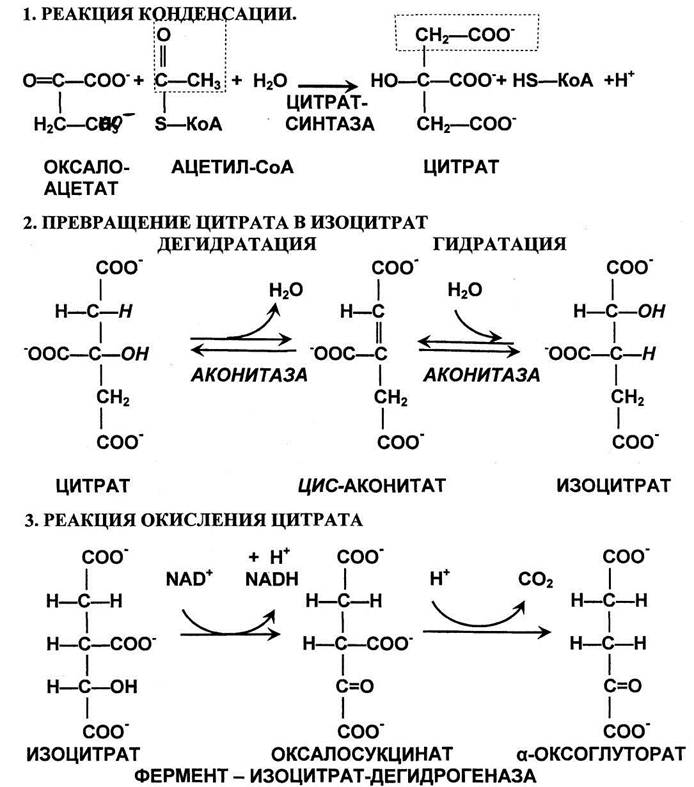
1. Реакция образования цитрата (лимонной кислоты). Эта реакция представляет
собой альдольную конденсацию с последующим гидролизом, катализирует цит-
рат-синтаза. При расщеплении тиоэфирной связи освобождается коэнзим А и вы
деляется значительная тепловая энергия. Равновесие в реакции сильно сдвинуто
вправо.
2. Превращение цитрата в изоцитрат. Изомеризация цитрата осуществляется пу
тем дегидратации с последующей гидратацией. В результате происходит взаимо
перемещение Н и ОН. Фермент назван аконитазой, поскольку промежуточное со-

 единение цис-аконитат не покидает активный центр фермента. 3. Реакция окислительного декарбоксилирования изоцитрата катализируется изо-цитрат-дегидрогеназой и ведет к образованию а-оксоглутарата (а-кетоглутарата). НАД+ в реакции играет роль второго субстрата захватывая пару высокоэнерге-тичных электронов и в форме НАДН вовлекает их в процесс окислительного фосфорилирования. Самая медленная реакция цикла. Аллостерически активируется АДФ.
единение цис-аконитат не покидает активный центр фермента. 3. Реакция окислительного декарбоксилирования изоцитрата катализируется изо-цитрат-дегидрогеназой и ведет к образованию а-оксоглутарата (а-кетоглутарата). НАД+ в реакции играет роль второго субстрата захватывая пару высокоэнерге-тичных электронов и в форме НАДН вовлекает их в процесс окислительного фосфорилирования. Самая медленная реакция цикла. Аллостерически активируется АДФ.
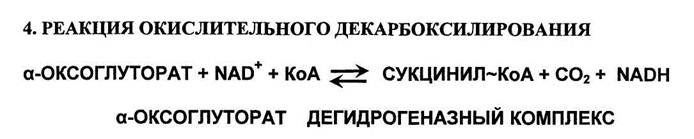
Реакция катализируется а-оксоглутарат дегидрогеназным комплексом (мульти-ферментный комплекс), который структурно и функционально сходен с пируват дегидрогеназным комплексом. Механизм этой реакции сходен с механизмом превращения пирувата в ацетил-КоА. В состав комплекса также входят 5 кофермен-тов: тиаминдифосфат (ТДФ), липоевая кислота, ФАД, НАД* и КоА. а-Оксоглутарат дегидрогеназный комплекс отличается от пируват дегидрогеназ-ного комплекса тем, что в нем отсутствует сложная система регуляции активности. Равновесие реакции сильно сдвинуто вправо, в сторону образования сукци-нил~КоА. Биохимическое значение реакции состоит в удалении карбоксильной группы (—СОО") поскольку атом углерода в ней почти полностью окислен, и извлечь из неё электроны высокой энергии невозможно. Из неё можно извлечь всего 2е".
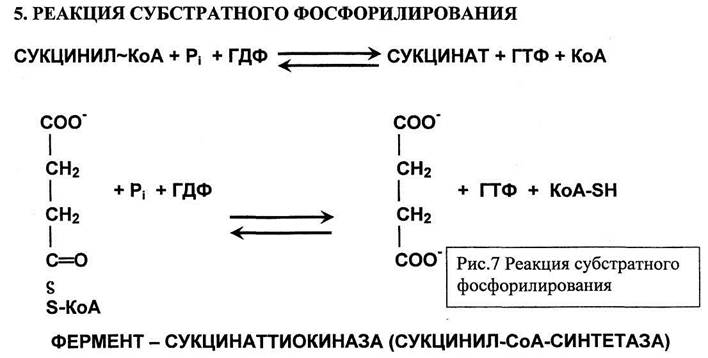
В этой реакции для синтеза ГТФ используется энергия молекулы сукцинил-КоА. Энергия разрыва тиоэфирной связи в молекуле сукцинил-КоА на 9% превышает ту энергию, которая необходима для фосфорилирования ГДФ с образованием ГТФ. Поэтому реакция легко обратима. Однако равновесие процесса сдвинуто вправо, поскольку ГТФ далее входит в реакцию переноса своей фосфатной группы на АДФ с образованием АТФ, который расходуется в клеточных процессах.
ГТФ + АДФ «-> ГДФ + АТФ Эту реакцию катализирует нуклеозидфосфаткиназа. На этом заканчивается первая стадия цикла трикарбоновых кислот.
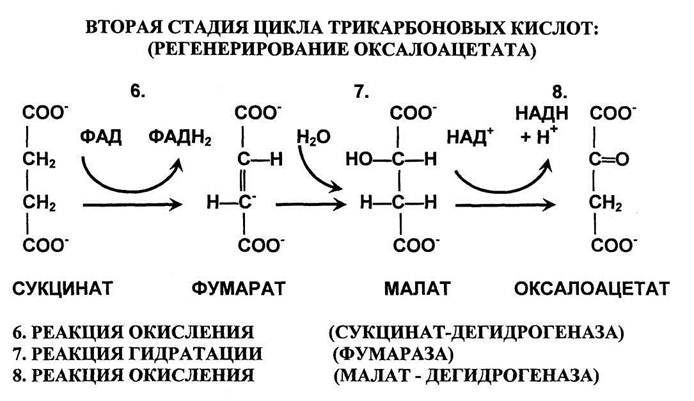
6. Фермент сукцинат-дегидрогеназа, действующий в 6 реакции - флавопротеин,
содержащий ковалентно присоединенный ФАД в своем активном центре. В отли
чие от других ферментов цикла трикарбоновых кислот сукцинат-дегидрогеназа
прочно закреплена во внутренней митохондриальной мембране. Фермент состоит
из двух субъединиц, одна из которых содержит ФАД. В состав двух субъединиц
включены железо-серные центры. В одной субъединице в форме - Fe2S2, а в дру
гой в форме - Fe4S4. Оба железо-серных центра сопряжены с компонентами дыха
тельной цепи и участвуют в транспорте электронов.
7. Реакцию гидратации катализирует фермент фумарат-гидратаза (фумараза), ло
кализованный в матриксе митохондрий. Особенностью реакции является абсо
лютная субстратная специфичность этого фермента. Фермент катализирует гид
ратацию только транс-формы фумарата.
8. Заключительную реакцию цикла трикарбоновых кислот катализирует НАД-
зависимая малат-дегидрогеназа, локализованная в митохондриальном матриксе.
Особенность реакции состоит в том, что в ней равновесие сильно сдвинуто влево.
Поскольку оксалоацетат, синтезируемый в этой реакции постоянно расходуется
на образование цитрата (цитрат-синтазная реакция), то в интактных клетках рав
новесие в этой реакции сдвинуто вправо.
 2015-01-07
2015-01-07 1545
1545
