1. Может ли протекать реакция при стандартных условиях:
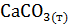 +
+ 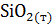 =
= 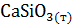 +
+ 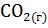 .
.
2. Какие из карбонатов: 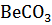 или
или 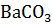 – можно получить по реакции взаимодействия соответствующих оксидов с
– можно получить по реакции взаимодействия соответствующих оксидов с 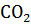 ? Какая реакция идет наиболее энергично? Вывод сделайте, вычислив
? Какая реакция идет наиболее энергично? Вывод сделайте, вычислив 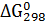 реакций.
реакций.
3. Вычислив 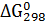 реакции образования моноалюмината кальция
реакции образования моноалюмината кальция
CaO 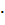
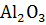 , являющегося главным минералом глиноземного цемента:
, являющегося главным минералом глиноземного цемента:
СаО + 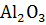 = CaO
= CaO 
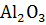 на основе
на основе 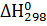 ,
, 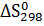 реагирующих веществ, определите, возможна ли эта реакция.
реагирующих веществ, определите, возможна ли эта реакция.
4. Вычислите значение 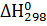 ,
, 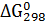 ,
, 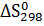 для процесса
для процесса 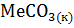
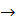
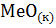 +
+ 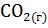 и составьте ряд термической стабильности карбонатов:
и составьте ряд термической стабильности карбонатов: 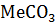 ,
, 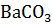 ,
, 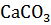 . Как влияет на течение этих процессов температура?
. Как влияет на течение этих процессов температура?
5. В каком направлении будет протекать реакция:
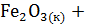
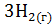 =
= 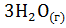 +
+ 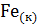 .
.
6. Как ведет себя магний в атмосфере кислорода, углекислого газа, паров воды? Ответ подтвердите расчетами.
7. Вычислите 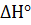 ,
, 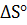 ,
, 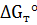 реакции, протекающей по уравнению:
реакции, протекающей по уравнению:
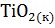 +
+ 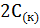 =
= 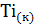 + 2
+ 2 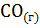 .
.
Возможна ли реакция восстановления 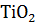 углеродом при температурах 1000, 3000 К?
углеродом при температурах 1000, 3000 К?
8. Определите, при какой температуре начинается реакция восстановления
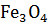 , протекающая по уравнению:
, протекающая по уравнению:
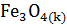 +4
+4 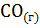 = 3
= 3 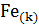 +
+ 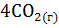 ;
; 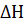 = +34,55 кДж.
= +34,55 кДж.
9. Вычислите, при какой температуре начинается диссоциация пентахлорида фосфора, протекающая по уравнению:
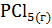 =
= 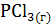 +
+ 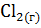 ;
; 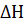 = +92,59 кДж.
= +92,59 кДж.
10. Тепловой эффект и изменение энергии Гиббса при 25 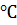 для реакции
для реакции
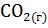 +
+ 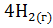 =
= 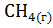 +
+ 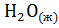 соответственно равны -253,02 Дж
соответственно равны -253,02 Дж 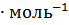 ; -130,1 Дж
; -130,1 Дж 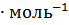 . Определите
. Определите 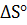 для этой реакции.
для этой реакции.
11. Подсчитав 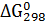 реакции, определите возможность протекания реакции
реакции, определите возможность протекания реакции 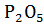 + 3
+ 3 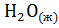 =
= 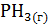 +
+ 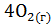 при стандартных условиях.
при стандартных условиях.
12. Реакция 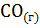 +
+ 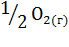

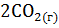 протекает при 298 К. Рассчитайте
протекает при 298 К. Рассчитайте 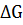 химической реакции.
химической реакции.
13. Установите возможность или невозможность самопроизвольного протекания реакции при температуре 298 К.
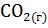
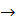
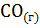 +
+ 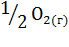 .
.
14. Установите возможность самопроизвольного протекания реакции
ВаО + 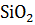 =
= 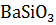 при температуре 298 К.
при температуре 298 К.
15. Установите возможность самопроизвольного протекания реакции 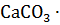
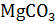 = CaO + MgO +
= CaO + MgO + 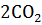 при температуре 298 К.
при температуре 298 К.
16. Установите возможность самопроизвольной диссоциации доломита при температуре 298 К: 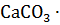
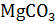 = Mg +
= Mg + 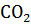 +
+ 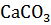 .
.
17. Установите возможность самопроизвольной реакции разложения сульфатных соединений: 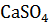
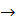 CaO +
CaO + 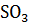 ;
; 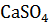
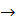 CaO +
CaO + 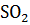 +
+ 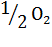 .
.
18. Установите возможность протекания реакции растворения трехкальциевого силиката: 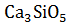 +
+ 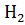 O
O 
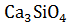 +
+ 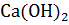 .
.
19. Установите возможность протекания реакции:
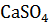 +
+ 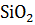 =
= 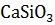 +
+ 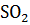 +
+ 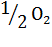 .
.
20. Приведите значения 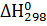 ,
, 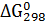 ,
, 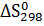 реакции для синтеза аммиака. Как влияет температура на величину
реакции для синтеза аммиака. Как влияет температура на величину 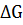 реакции?
реакции?
21. Образование какого оксида СО или 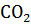 – наиболее вероятно при сгорании угля. При ответе используйте данные
– наиболее вероятно при сгорании угля. При ответе используйте данные 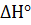 ,
, 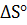 ,
, 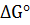 .
.
22. Вычислите 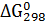 процессов взаимодействия
процессов взаимодействия 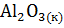 и
и 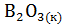 с Ca
с Ca 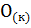 .
.
23. Вычислите 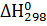 ,
, 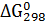 ,
, 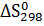 окисления кислородом оксидов кальция, бария до их пероксидов.
окисления кислородом оксидов кальция, бария до их пероксидов.
24. Вычислите 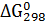 процессов окисления аммиака кислородом с образованием NO или
процессов окисления аммиака кислородом с образованием NO или 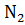 . Какой из этих процессов наиболее вероятен при сжигании аммиака?
. Какой из этих процессов наиболее вероятен при сжигании аммиака?
25. Какая из приведенных ниже реакций
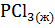 + 3
+ 3 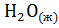 =
= 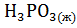 +
+ 
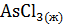 + 3
+ 3 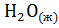 =
= 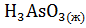 +
+ 
Обратима в обычных условиях, а какая нет? При обосновании ответа вычислите 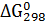 реакций.
реакций.
 2015-01-13
2015-01-13 1111
1111
