1. Растворимость 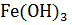 равна 1.9
равна 1.9 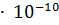 моль
моль 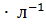 . Вычислите величину ПР(
. Вычислите величину ПР(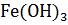 ).
).
2. В 2 л Н;0 при 250С может раствориться 2.2 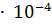 г AgBr. Вычислите ПP(AgBr).
г AgBr. Вычислите ПP(AgBr).
3. Растворимость сульфата бария в воде равна 1: 428000. Вычислите произведение растворимости 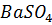 .
.
4. Растворимость  при 18°С равна 1.3
при 18°С равна 1.3 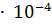 моль
моль 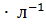 . Вычислите произведение растворимости
. Вычислите произведение растворимости  .
.
5. Растворимость 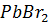 при 18°С равна 2.7
при 18°С равна 2.7 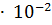 моль
моль 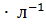 . Вычислите произведение растворимости
. Вычислите произведение растворимости 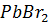 .
.
6. Растворимость 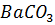 равна 8.9
равна 8.9 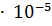 моль
моль 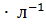 . Вычислить: концентрации ионов
. Вычислить: концентрации ионов 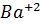 ,
, 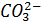 в г
в г 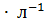 и произведение растворимости
и произведение растворимости 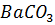 .
.
7. ПР(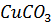 ) при 25 °С равно 236
) при 25 °С равно 236 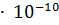 . Определите концентрацию ионов
. Определите концентрацию ионов 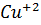 в насыщенном растворе
в насыщенном растворе 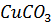 , содержащем
, содержащем 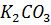 в количестве 0.001 моль/л; степень диссоциации
в количестве 0.001 моль/л; степень диссоциации 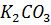 равна 95 %.
равна 95 %.
8. Насыщенный раствор 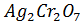 объемом 5 л содержит 0.5 моль
объемом 5 л содержит 0.5 моль 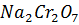 . Найдите концентрацию ионов
. Найдите концентрацию ионов 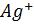 в этом растворе, если ПP(
в этом растворе, если ПP(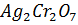 )=2
)=2 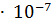 и α (
и α (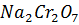 ) = 75 %.
) = 75 %.
9. Определите растворимость 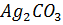 в воде: ПP(
в воде: ПP(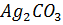 )=6.15
)=6.15 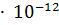 .
.
10. Насыщенный при комнатной температуре раствор 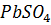 объемом 3 л содержит 0.132 г соли. Вычислите ПP(
объемом 3 л содержит 0.132 г соли. Вычислите ПP(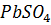 ).
).
11. Насыщенный раствор 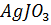 объемом 3 л содержит в виде ионов 0.176г серебра. Вычислите ПP(
объемом 3 л содержит в виде ионов 0.176г серебра. Вычислите ПP(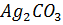 ).
).
12. ПP(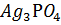 ) составляет 1.8
) составляет 1.8 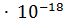 . В каком объеме насыщенного раствора содержится 0.050 г растворенной соли?
. В каком объеме насыщенного раствора содержится 0.050 г растворенной соли?
13. ПP(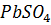 )=2.3
)=2.3 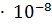 . Чему равна концентрация
. Чему равна концентрация 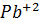 в насыщенном растворе сульфата свинца?
в насыщенном растворе сульфата свинца?
14.Сколько воды потребуется для растворения при комнатной температуре 1 г 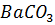 ? ПР(
? ПР(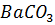 ) = 1.9
) = 1.9  .
.
15. ПP(CuS)=4 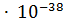 . Сколько литров воды понадобится для растворения 1г сульфида меди (II)?
. Сколько литров воды понадобится для растворения 1г сульфида меди (II)?
16. ПP(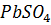 )=2.3
)=2.3 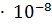 . Сколько граммов
. Сколько граммов 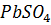 можно растворить в 1 л
можно растворить в 1 л 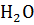 при обычной температуре?
при обычной температуре?
17. Растворимость М  при некоторой температуре равна 0.012 г
при некоторой температуре равна 0.012 г 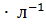 . Определите ПP(М
. Определите ПP(М  ).
).
18. ПP(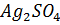 ) = 7
) = 7 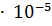 . Образуется ли осадок, если к 0.02 Н раствору
. Образуется ли осадок, если к 0.02 Н раствору 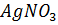 прибавить равный объем нормального раствора серной кислоты?
прибавить равный объем нормального раствора серной кислоты?
19. ПP(AgCI) = 1.6 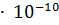 . Выпадет ли осадок, если смешали 20мл 0.01 Н раствора КСl с 5 мл 0.001 М раствора
. Выпадет ли осадок, если смешали 20мл 0.01 Н раствора КСl с 5 мл 0.001 М раствора 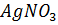 ?
?
20. ПР(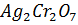 ) = 2.0
) = 2.0 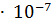 . Выпадет ли осадок, если смешали равные объемы 0.01 Н растворов
. Выпадет ли осадок, если смешали равные объемы 0.01 Н растворов 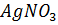 и
и 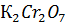 ?
?
21. ПР( ) = 1.7
) = 1.7 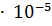 . Выпадет ли осадок, если смешали 1 мл 0.2 М раствора
. Выпадет ли осадок, если смешали 1 мл 0.2 М раствора 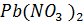 и 2 мл 0.01 М раствора NaCl?
и 2 мл 0.01 М раствора NaCl?
22. Произведение растворимости AgCl = 1.56 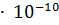 . Сколько граммов этой соли содержится в 100 мл насыщенного раствора?
. Сколько граммов этой соли содержится в 100 мл насыщенного раствора?
23. Произведение растворимости сульфата стронция 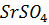 равно 2.8
равно 2.8 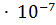 . Вычислите растворимость этой соли в воде в моль
. Вычислите растворимость этой соли в воде в моль 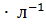 .
.
24. Образуется ли осадок Fe 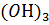 , если к одному литру 0,006 H Fe
, если к одному литру 0,006 H Fe 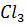 прибавить 0.125 л 0.0001 М КОН? ПР(Fe
прибавить 0.125 л 0.0001 М КОН? ПР(Fe 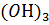 ) = 3.8
) = 3.8 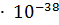 . Степень электролитической диссоциации исходных веществ принять, равной 1.
. Степень электролитической диссоциации исходных веществ принять, равной 1.
25. Выпадет ли осадок сульфата кальция, если к 0.1 л 0.01 М 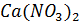 прибавлено 0.4 л 0.001 H
прибавлено 0.4 л 0.001 H 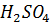 ? Степень электролитической диссоциации
? Степень электролитической диссоциации 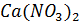 и
и 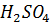 равна 95 %. ПP(
равна 95 %. ПP(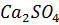 ) = 6.1
) = 6.1 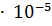
 2015-01-13
2015-01-13 1600
1600
