1. Определите 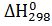
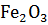 , если при реакции 2Fe +
, если при реакции 2Fe + 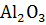 =
= 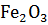 + 2Al
+ 2Al
на каждые 80г 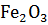 поглощается 426,5 кДж теплоты.
поглощается 426,5 кДж теплоты.
2. При растворении 16г Са 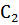 в воде выделяется 31,3 кДж теплоты. Определите стандартную теплоту образования Са
в воде выделяется 31,3 кДж теплоты. Определите стандартную теплоту образования Са 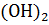 .
.
3. Определите количество теплоты, выделяющееся при взаимодействии 50г 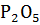 с водой по реакции:
с водой по реакции: 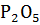 +
+ 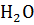 = 2НР
= 2НР 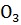
Если тепловые эффекты реакции равны:
2Р + 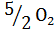 =
= 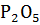 ;
; 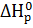 = -1549,0 кДж
= -1549,0 кДж
2Р + Н + 3 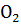 = 2НР
= 2НР 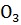 ;
; 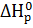 = -1964,8 кДж
= -1964,8 кДж
4. Сколько нужно затратить теплоты, чтобы разложить 200г 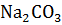 до оксида натрия и диоксида углерода, если тепловые эффекты реакции равны:
до оксида натрия и диоксида углерода, если тепловые эффекты реакции равны:
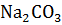 + Si
+ Si 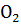 = Na Si
= Na Si 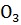 +
+ 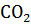 ;
; 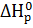 = 819,29 кДж
= 819,29 кДж
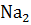 О + Si
О + Si 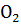 = Na Si
= Na Si 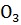 ;
; 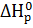 = -243,5 кДж
= -243,5 кДж
5. При сгорании 9,3 фосфора выделяется 229,5 кДж теплоты. Рассчитайте 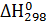 оксида фосфора (V).
оксида фосфора (V).
6. Вычислите теплоту разложения 1кг  по уравнению:
по уравнению:
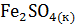 =
= 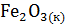 +
+ 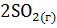 + 0,5
+ 0,5 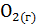 .
.
7. Вычислите теплоту реакции сгорания водяного газа (СО + 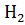 ) по реакции:
) по реакции: 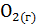 +
+ 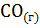 +
+ 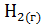 =
= 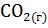 +
+ 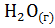 .
.
8. Сколько тепла выделится при реакции горения 100л 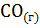 до
до 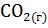 .
.
9. Стандартная теплота образования 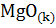 и
и 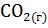 соответственно равна -601,8 и -393,5 кДж
соответственно равна -601,8 и -393,5 кДж 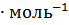 . Теплота разложения
. Теплота разложения 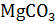 на MgO и
на MgO и 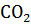 ?
? 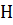 = +100,7 кДж
= +100,7 кДж 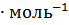 . Используя эти данные, найдите теплоту образования
. Используя эти данные, найдите теплоту образования 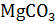 из элементов.
из элементов.
10. При сжигании графита образовался оксид углерода (IV) массой 8,86 г. Вычислите теплоту образования 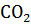 из элементов. Тепловой эффект реакции ?
из элементов. Тепловой эффект реакции ? 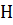 = -79,2 кДж.
= -79,2 кДж.
11. Найдите 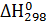 реакций:
реакций:
а) 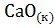 +
+ 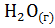 = Са
= Са 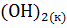
б) 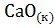 +
+ 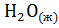 = Са
= Са 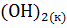
12. Исходя из теплового эффекта реакции
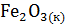 +
+ 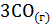 = 2
= 2 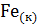 + 3
+ 3 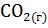 , равного -26,8 кДж; вычислите
, равного -26,8 кДж; вычислите 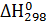 образования оксида железа (III).
образования оксида железа (III).
13. Вычислите тепловой эффект реакции нейтрализации между К 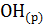 и
и 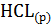 ; С
; С 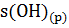 и
и 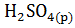 ;
; 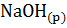 и
и 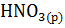 в расчете 1 моль
в расчете 1 моль 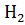 О в стандартных условиях. Почему тепловые эффекты этих реакций одинаковы?
О в стандартных условиях. Почему тепловые эффекты этих реакций одинаковы?
14. Процесс гашения оксида кальция представлен следующим термохимическим уравнением: 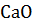 +
+ 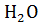 = Са
= Са 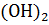 + 16 ккал. Сколько теплоты выделиться при гашении 1т извести, содержащей 20% посторонних примесей.
+ 16 ккал. Сколько теплоты выделиться при гашении 1т извести, содержащей 20% посторонних примесей.
15. Определите теплоту образования двуокиси кремния, если известны:
тепловой эффект реакции восстановления кремния из кремнезема магнием; равный 86,5 ккал, и теплота образования оксида магния, равная 145,8 ккал.
16. Рассчитайте расход тепловой энергии при реакции:
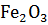 + 2Al =
+ 2Al = 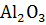 + 2 Fe, если было получено 336г железа.
+ 2 Fe, если было получено 336г железа.
17. Вычислите тепловой эффект реакции восстановления оксида железа (II) водородом, исходя из следующих термохимических уравнений:
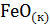 +
+ 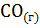 =
= 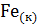 +
+ 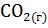 ; ?
; ? 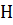 =-13,18 кДж
=-13,18 кДж
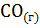 +
+ 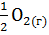 =
= 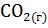 ; ?
; ? 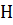 =-283 кДж
=-283 кДж
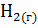 +
+ 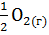 =
= 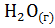 ; ?
; ? 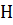 =-241,83 кДж
=-241,83 кДж
18. Тепловой эффект какой реакции равен теплоте образования гидроксида кальция? Вычислите теплоту образования гидроксида кальция, исходя из следующих термохимических уравнений:
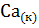 +
+ 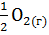 =
= 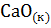 ; ?
; ? 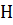 =-635,6 кДж
=-635,6 кДж
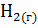 +
+ 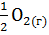 =
= 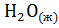 ; ?
; ? 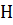 =-285,84 кДж
=-285,84 кДж
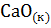 +
+ 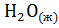 = Са
= Са 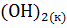 ; ?
; ? 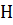 =-65,06 кДж
=-65,06 кДж
19. При получении эквивалентной массы Са 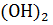 из
из 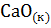 и
и 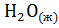 выделяется 32,53 кДж теплоты. Напишите термохимическое уравнение этой реакции и вычислите теплоту образования СаО.
выделяется 32,53 кДж теплоты. Напишите термохимическое уравнение этой реакции и вычислите теплоту образования СаО.
20. Тепловой эффект какой реакции равен теплоте образования метана? Вычислите теплоту образования метана, исходя из следующих термохимических уравнений:
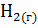 +
+ 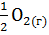 =
= 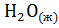 ; ?
; ? 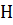 =-285,84 кДж
=-285,84 кДж
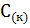 +
+ 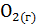 =
= 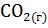 ; ?
; ? 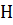 =-393,51 кДж
=-393,51 кДж
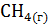 +
+ 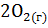 =
= 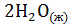 +
+ 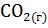 ; ?
; ? 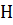 =-890,31 кДж
=-890,31 кДж
21. При получении азотной кислоты из 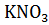 протекают следующие реакции:
протекают следующие реакции:
а) 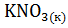 +
+ 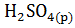 =
= 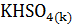 +
+ 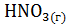
б) 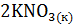 +
+ 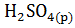 =
= 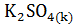 +
+ 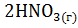
Сколько теплоты выделяется или поглощается при получении 1 кг азотной кислоты, если 80% ее образуется по реакции [a];
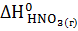 = -133,90 кДж
= -133,90 кДж 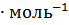 .
.
22. Вычислите количество теплоты, которое выделятся при сгорании 20 л диборана (н.у.), если 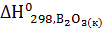 и
и 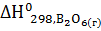 соответственно равны – 1264 и +31,4 кДж
соответственно равны – 1264 и +31,4 кДж 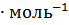 . Целесообразно ли использовать в качестве топлива диборан вместо этана, если стандартная теплота сгорания этана -1559,88 кДж
. Целесообразно ли использовать в качестве топлива диборан вместо этана, если стандартная теплота сгорания этана -1559,88 кДж 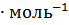 ?
?
23. Разложение гремучей ртути про взрыве идет по уравнению
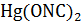 = Hg + CO +
= Hg + CO + 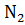 ;
; 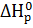 = -364,2 кДж.
= -364,2 кДж.
Определите объем выделившихся газов (н.у.) и количество теплоты, выделившейся при взрыве 1,5 кг 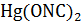 .
.
24. Найдите теплоту сгорания алмаза, если стандартная теплота сгорания графита равна -393,51 кДж 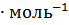 , а теплота фазового перехода графита в алмаз равна 1,88 кДж
, а теплота фазового перехода графита в алмаз равна 1,88 кДж 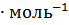 .
.
25. Какое количество теплоты выделяется при превращении 1 кг красного фосфора в черный, если 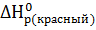 = -18,41;
= -18,41; 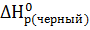 = 43,20 кДж
= 43,20 кДж 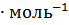 .
.
 2015-01-13
2015-01-13 2207
2207








