В водном растворе соль K2SO4 диссоциирует: K2SO4 Á 2К+ + SO2–4 .
К катоду подходят катионы К+ и молекулы Н2О, к аноду – ионы SO2–4 и молекулы Н2О. Поскольку потенциал системы 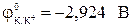 (см. табл. 9.1) меньше, чем –1,4 В, на катоде будут восстанавливаться молекулы воды (см. вышеприведенную схему).
(см. табл. 9.1) меньше, чем –1,4 В, на катоде будут восстанавливаться молекулы воды (см. вышеприведенную схему).
Анионы SO2–4 – это сложные ионы, в водных растворах они не окисляются. Поэтому на аноде окисляются молекулы воды.
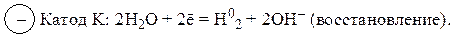
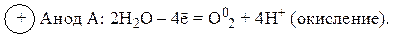
Раствор у катода подщелачивается (появляются ионы ОН–), у анода становится более кислым (появляются ионы Н+). Суммарное молекулярное уравнение реакции электролиза:
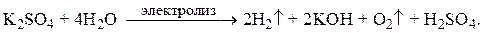
КОН и Н2SO4 образуются из К+ и ОН–, Н+ и SO2–4, находящихся в растворе.
Пример 2. Составить уравнения катодного и анодного процессов, протекающих при электролизе раствора CuCl2 с медным анодном.
 2015-02-27
2015-02-27 1078
1078
