Потенциал 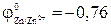 В (см. табл. 9.1) и лежит в области
В (см. табл. 9.1) и лежит в области
–1,4 В < j < -0,41 В. Следовательно, на катоде будет идти совместное восстановление катионов Zn2+ и, частично, молекул воды:
Zn2+ + 2ē = Zn
2H2O + 2ē = 2OH- + H2 (частично, побочный процесс)
Для определения теоретического количества выделившегося на катоде цинка воспользуемся уравнением закона Фарадея:
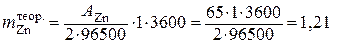 г.
г.
Выход по току вычисляется по формуле
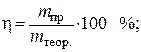
следовательно
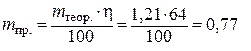 г.
г.
На получение цинка на катоде расходуется 64 % всего прошедшего через электролит тока, остальной ток тратится на восстановление воды.
Задачи
271–277 Составьте электронные уравнения процессов, протекающих на катоде и аноде при электролизе:
1) расплава вещества А с графитовыми электродами;
2) раствора вещества Б с графитовыми электродами;
3) раствора вещества В с растворимым (активным) анодом.
Масса твердого вещества, выделившегося на катоде при электролизе раствора вещества Б при прохождении тока I (А) в течение времени τ (ч), составляет m (г). Вычислите выход по току. Объясните, почему в ряде случаев не весь ток расходуется на выделение металла.
| № задачи | Соединения | Растворимый анод | I, А | τ, час | m, г | ||
| А | Б | В | |||||
| KCl | SnCl2 | ZnSO4 | Zn | 8,5 | 36,6 | ||
| FeCl2 | ZnSO4 | MgCl2 | Mg | 1,5 | 11,3 | ||
| NaOH | FeCl2 | MnSO4 | Mn | 0,5 | 4,2 | ||
| PbCl2 | Cu(NO3)2 | FeCl2 | Fe | 7,1 | |||
| Ca(OH)2 | NiCl2 | AlCl3 | Al | 9,3 | 18,8 | ||
| LiBr | MnSO4 | CoCl2 | Co | 10,5 | 0,5 | 3,0 | |
| SnCl2 | FeSO4 | Pb(NO3)2 | Pb | 8,8 | 14,2 |
Ответ: 271) 97 %; 272) 62 %; 273) 67 %; 274) 99 %; 275) 91,9 %;
276) 55,8 %; 277) 77,3 %.
278–284. Составьте электронные уравнения процессов, протекающих на катоде и аноде при электролизе:
1) расплава вещества А с графитовыми электродами;
2) раствора вещества Б с графитовыми электродами;
3) раствора вещества В с растворимым (активным) анодом.
Вычислите время, необходимое для практического получения 100 г металла из раствора вещества Б при силе тока I, если выход по току h.
| № задачи | Вещества | Растворимый анод | I, A | h, % | ||
| А | Б | В | ||||
| SnCl2 | Fe(NO3)2 | NiSO4 | Ni | 66,7 | ||
| Ni(OH)2 | CoCl2 | Pb(NO3)2 | Pb | 9,5 | ||
| MgCl2 | ZnSO4 | NiSO4 | Zn | 6,4 | ||
| ZnCl2 | AgNO3 | CuCl2 | Cu | 14,8 | ||
| CuBr2 | Cd(NO3)2 | AgNO3 | Ag | 8,7 | ||
| NaOH | Pb(NO3)2 | NiCl2 | Ni | 5,9 | ||
| PbCl2 | CоSO4 | Mg(NO3)2 | Mg |
Ответ: 278) 12 ч; 279) 10 ч; 280) 17,3 ч; 281) 1,7 ч; 282) 6,4 ч; 283) 4,7 ч; 284) 12,3 ч.
285–291 Составьте электронные уравнения процессов, протекающих на катоде и аноде при электролизе:
1) расплава вещества А с графитовыми электродами;
2) раствора вещества Б с графитовыми электродами;
3) раствора вещества В с растворимым (активным) анодом.
Как изменится масса анода после пропускания тока силой I (А) в течение времени τ (ч) через раствор В?
| № задачи | Вещества | Растворимый анод | I, A | τ, час | ||
| А | Б | В | ||||
| NaI | MgSO4 | ZnCl2 | Zn | 8,5 | ||
| CaCl2 | Cu(NO3)2 | FeCl2 | Fe | |||
| RbCl | AgNO3 | CuSO4 | Cu | 7,5 | 2,5 | |
| KOH | ZnCl2 | CoCl2 | Co | 3,7 | ||
| CuCl2 | NaNO3 | Pb(NO3)2 | Pb | 2,5 | ||
| NaOH | Bi(NO3)3 | NiCl2 | Ni | 2,0 | 2,5 | |
| CaI2 | H2SO4 | Cd(NO3)2 | Cd | 6,8 | 0,8 |
Ответ: 285) 20,6 г; 286) 31,3 г; 287) 22,4 г; 288) 4,1 г; 289) 38,6 г;
290) 5,5 г; 291) 7,1 г.
292–300 Составьте электронные уравнения процессов, протекающих на катоде и аноде при электролизе:
1) расплава вещества А с графитовыми электродами;
2) раствора вещества Б с графитовыми электродами;
3) раствора вещества В с растворимым (активным) анодом.
Постройте график зависимости изменения массы растворимого анода m от силы тока I при времени электролиза 0,5 ч. Сила тока I равна 0,5; 1; 2; 3 и 5 А.
| № задачи | Соединения | Растворимый анод | ||
| А | Б | В | ||
| KOH | Na2SO4 | NiCl2 | Ni | |
| RbCl | Li2SO4 | Pb(NO3)2 | Pb | |
| NaCl | Ni(NO3)2 | AgNO3 | Ag | |
| AlCl3 | Fe2(SO4)3 | CuSO4 | Cu | |
| NaI | Cu(NO3)2 | ZnCl2 | Zn | |
| SnCl2 | CoSO4 | CuSO4 | Cu | |
| CoCl2 | BiСl3 | AgNO3 | Ag | |
| № задачи | Соединения | Растворимый анод | ||
| А | Б | В | ||
| KCl | SnCl2 | ZnSO4 | Zn | |
| NaI | Cu(NO3)2 | PbCl2 |
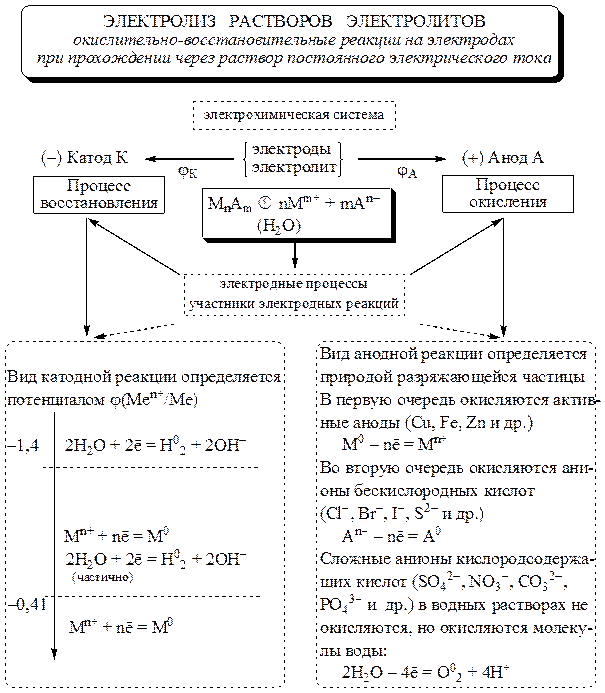
Рис. 11.1. Структурно-логическая схема взаимосвязи электродных процессов при электролизе
 2015-02-27
2015-02-27 808
808








