 Сульфацил-натрий Sulfacilum natrium Сульфацетамид натрия (МНН)
Сульфацил-натрий Sulfacilum natrium Сульфацетамид натрия (МНН)
Относится к группе производных п-аминобензолсульфамида (сульфаниламидов).
Фармакологическое действие сульфаниламидов обусловлено наличием в молекуле лекарственного вещества амида сульфаниловой кислоты. Хорошая растворимость в воде позволяет использовать сульфацил-натрий для инъекций при пневмониях, гнойных трахеобронхитах, инфекциях мочеполовых путей. Назначают в глазной практике в виде 20-30% растворов и мазей. Сульфацил-натрий - белый кристаллический порошок без запаха. Как и другие натриевые соли, легко растворим в воде и метаноле и практически нерастворим в органических растворителях (этаноле, эфире, хлороформе, ацетоне).
Для идентификации используют общие и частные реакции, обуловленные наличием функциональных групп в молекуле: первичной ароматической аминогруппы, ароматического цикла, сульфамидной группы, ацетильной группы.
Общие реакции:
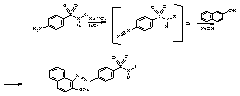
Реакция образования азокрасителя (на первичную ароматическую аминогруппу) основана на образовании хлорида диазония при действии раствором нитрита натрия и разведенной хлороводородной кислотой. Последующее сочетание хлорида диазония с фенолами в щелочной среде приводит к образованию азокрасителя
Лигниновая проба. Это своеобразная разновидность реакции образования шиффовых оснований. Она выполняется на древесине или газетной бумаге, при нанесении на которую сульфацила-натрия и капли разведенной соляной кислоты появляется оранжево-желтое окрашивание.
Реакция галогенирования (на ароматический цикл). Реакция обнаружения серы (в сульфамидной группе). Наличие серы в молекуле сульфацила-натрия можно установить по реакции на сульфат-ион после нагревания препарата с азотной кислотой. Наличие серы устанавливают после минерализации конц-й азотной кислотой. Образющийся сульфат ион затем обнаруживают с раствором хлорида бария:
SO42-+Ba2+→ Ba SO4↓
При термическом разложении сульфацила-натрия в сухой пробирке образуется окрашенный плав и ощущается запах уксусной кислоты.
Реакция с нитропруссидом натрия. Раствор сульфацила-натрия в присутствии едкой щелочи образует окрашеный в красный цвет раствор.
Частные реакции на сульфацил-натрия:
Сульфацил-натрий при действии уксусной кислотой выделяет белый осадок сульфацила, который после высушивания должен иметь температуру плавления около 183°С:
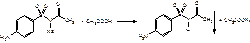
При растворении осадка в этаноле и добавлении концентрированной серной кислоты образуется этилацетат, имеющий характерный запах:
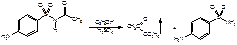
Катион натрия можно обнаружить по окраске бесцветного пламени в жёлтый цвет.
Количественное определение сульфацила-натрия можно провести с помощью физико-химических методов анализа.Используют УФ-спектроскопию, фотоколориметрию, для количественного определения сульфацила-натрия нитритометрию: Титрант - 0,1 М раствор нитрита натрия. Определение ведут в кислой среде при температуре + 4°С в присутствии бромида калия. Точку эквивалентности устанавливают по внутреннему индикатору - нейтральному красному, по внешнему индикатору - иодкрахмальной бумаге.
УФ-спектр сульфацила-натрия имеет максимум светопоглощения при 256 нм. Содержание рассчитывают по раствору стандартного образца.
Сульфацил-натрий как кристаллогидрат при неправильном хранении постепенно теряет воду. Сульфацил-натрий может поглощать углекислый газ, при этом его растворимость уменьшается. При длительном хранении растворы могут желтеть, так как происходит постепенное окисление сульфацила-натрия.
 2015-02-27
2015-02-27 2136
2136








