Осальмид Для испытания подлинности осальмида используют реакцию гидролиза в кислой среде, в результате которой образуются n -аминофенол и салициловая кислота:
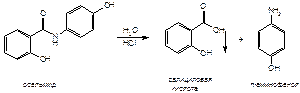
Выделившийся n -аминофенол идентифицируют по цветной реакции с резорцином в щелочной среде:
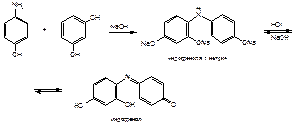
Образуется индофенолят натрия, окрашенный в синий цвет, который переходит в кислой среде в индофенол (красного цвета). Процесс окисления до индофенола происходит за счет кислорода воздуха. В некоторых методиках рекомендуют в качестве окислителя добавлять небольшое количество раствора йода (появляется темно-фиолетовая окраска).
С азотистой кислотой в присутствии концентрированной серной кислоты осальмид образует грязно-фиолетовое окрашивание. Аналогичные результаты получаются при взаимодействии с раствором формальдегида в серной кислоте (реактив Марки). Осальмид при взаимодействии с хлороформом и гидроксидом натрия образует ауриновый краситель желто-зеленого цвета.
Подлинность осальмида устанавливают также с помощью общей реакции на фенольный гидроксил, действуя раствором хлорида железа (III). Учитывая растворимость, для испытания осальмида берут спиртовой раствор, появляется красно-фиолетовое окрашивание.
Количественное определение проводят определяя содержание азота. Осальмид подвергают полной минерализации по методу Кьельдаля (действуя смесью сульфатов калия, меди (II) и концентрированной серной кислотой) до образования сульфата аммония. После этого добавляют 30%-ный раствор гидроксида натрия и количественно отгоняют выделившийся аммиак в приемник (далее поступают как указано выше). Аммиак образует с борной кислотой тетрагидроксиборат аммония:
H3BO3 + H2O ¾® H[B(OH)4]; NH3 + H[B(OH)4] ¾® NH4[B(OH)4]
Отгон титруют 0,1 М раствором хлороводородной кислоты:
NH4[B(OH)4] + HCl ¾® NH4Cl + H3BO3 + H2O
 2015-02-27
2015-02-27 1747
1747








