Сущность метода. При взаимодействии аммиака с гипохлорит – ионами образуется монохлорамин, который с фенолом в щелочной среде образует n – аминофенол:
NH3 + OCl– ® NH2Cl + OH–
C6H5O– + NH2Cl ® n - HOC6H4NH2 + Cl–
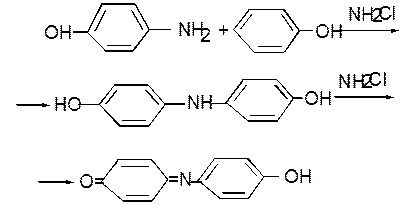 |
Последний, реагируя со второй молекулой фенола, образует сначала 4,4¢- дигидроксидифениламин, окисляющийся хлорамином с образованием синего красителя индофенола:
В качестве катализатора и стабилизирующего агента вводят соль марганца (II). Предел обнаружения 0,01 мг/дм3 NH4+. Диапазон измеряемых концентраций без разбавления пробы – 0,01 –1 мг/дм3 NH4+.
Мешающие вещества. Определению NH4+ фенол-гипохлоритным методом мешают немногие вещества; их значительно меньше, чем при определении с реактивом Несслера. Сильно мешают сероводород и сульфиды. Их можно удалить, подкислив пробу до рН = 3 и пропустив воздух до исчезновения запаха сероводорода. Мешают восстановители, реагирующие с гипохлоритом (например, цианиды, роданиды), большая щелочность пробы (выше 500 мг/дм3), слишком большая кислотность (больше 100 мг-экв/дм3) и вещества, вызывающие окраску воды или мутность. В таких случаях проводят предварительную отгонку аммиака.
Во всех остальных случаях возможно определение NH4+ без предварительной отгонки аммиака.
Реактивы и оборудование
Бидистиллят, не содержащий аммиака. Дважды перегнанную воду пропускают через колонку с катионом КУ-2. Эту воду используют для приготовления реактивов и разбавления проб.
Фенолят натрия: В 100 мл безаммиачной дистиллированной воды растворяют 5 г свежеперегнанного фенола, 25 мл нитропруссида натрия и 0,1 г салициловой кислоты.
Гипохлорит натрия, 3%-ный раствор.
Сульфат марганца (II), 0,003 М раствор.
Стандартный раствор с содержанием ионов аммония 0,05 мг/см3 (свежеприготовленный).
Пипетка на 5 см3
Мерные пробирки
Мерные колбы на 50 см3
 2015-02-27
2015-02-27 1736
1736
