Понимание того, что такое температура пришло много позже введения единиц для измерения температуры как степени нагретости тела.
Шкалу температур от точки таяния льда (0°С) до точки кипения воды разделили на 100 частей и одну такую часть назвали 1 градус Цельсия (10С).
От 0°С шкалу температур такими же шагами (градусами) продлили вниз до точки, где кинетическая энергия поступательного движения молекул равна нулю, и назвали эту температуру абсолютным нулем. По Цельсию это – минус 273,150С. Кельвин предложил отсчитывать температуру от этой точки, а размер градуса сохранить. Тогда – 273,15°С будет соответствовать 0 градусов по Кельвину (0 К), а 0°С будет соответствовать 273,15 К. Под Т в дальнейшем понимается абсолютная температура в К.
Изучая разреженные газы Клапейрон открыл для них связь между термодинамическими параметрами в виде: p·V=C·T. Д.И.Менделеев показал, что коэффициент С в этом уравнении равен: С = ν· R =(m /μ)· R, где универсальная газовая постоянная R = 8,314 Дж/(моль·К) была определена опытным путем. Уравнение p·V=ν · R · T= (m /μ)· R · T = (N / N A)· R · T (4) называется уравнением состояния идеального газа или Клапейрона-Менделеева.
Умножим обе части уравнения (3) на объем V, занимаемый в данных условиях газом: 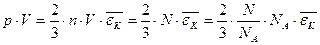 (5),
(5),
где n·V = N – число молекул в объеме V.
Сравнивая уравнения (4) и (5) получим: 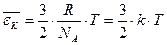 (6),
(6),
где к = R/NA представляет собой газовую постоянную в расчете на одну молекулу. Она называется постоянной Больцмана и равна
k = 8,314 /(6,02 · 1023)= 1,38·10 -23Дж/К (7).
Из (6) следует физический смысл температуры: она характеризует среднюю кинетическую энергию движения молекул. При приведении тел в соприкосновение молекулы сталкиваются друг с другом, обмениваясь энергией. В конце концов средние кинетические энергии молекул соприкасающихся тел выравниваются. Т.о., температура определяется как термодинамический параметр, который выравнивается у тел, приведенных в соприкосновение. На этом основано действие термометров – приборов для измерения температуры, которая после теплообмена становится одинаковой и у тела и у прибора.
Поскольку N/V=n – концентрация, а m /V=ρ – плотность газа, то из (4) можно получить формулы: p=n·k·T и 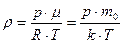 (8).
(8).
 2015-02-04
2015-02-04 1175
1175
