Если степень окисления некоторого атома в химическом соединении промежуточная, то этот атом может как принимать электроны (т.е. быть окислителем), так и отдавать их (т.е. быть восстановителем). Такое поведение, в частности, характерно для пероксида водорода, поскольку в состав молекулы Н2O2 входят атомы кислорода в промежуточной степени окисления минус 1:
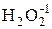 (окислитель) ® Н2O–2 (2O–1 + 2e– ® 2O–2)
(окислитель) ® Н2O–2 (2O–1 + 2e– ® 2O–2)
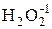 (восстановитель) ® O20 (2O–1 – 2e– ® O20).
(восстановитель) ® O20 (2O–1 – 2e– ® O20).
При прогнозировании поведения пероксида водорода и других веществ, характеризующихся окислительно-восстановительной двойственностью, необходимо учитывать следующее. Если, например, для пероксида водорода партнёром по реакции является вещество, способное быть только окислителем (KMnO4, K2Cr2O7), то H2O2 будет вести себя как восстановитель и окисляться до O2. Если же пероксид водорода взаимодействует с веществом, способным проявлять только восстановительные свойства (KI), то молекулы H2O2 будут выполнять функцию окислителя, восстанавливаясь до молекул H2O.
Окислительно-восстановительная двойственность характерна также для азотистой кислоты и нитритов:
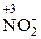 (окислитель) ®
(окислитель) ® 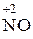 , или
, или 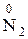 , или
, или 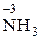 ;
;
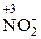 (восстановитель) ®
(восстановитель) ® 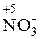 .
.
Активные неметаллы, например, галогены в щелочных растворах подвергаются реакциям самоокисления-самовосстановления (диспропорционирования); в этих реакциях одна часть атомов простого вещества является окислителем, а другая – восстановителем:
Cl20 ® 2Cl–1 Cl20 ® 2Cl–1
Cl20 ® 2 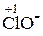 Cl20 ® 2
Cl20 ® 2 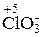
Несмотря на то, что вещества, в состав которых входит атом в промежуточной степени окисления, теоретически могут быть как окислителями, так и восстановителями, на практике часто преимущественно проявляются либо окислительные, либо восстановительные свойства. Например, атомы Mn+4, Cu+2, Fe+2, S+4 в соединениях MnO2, CuSO4, Fe(OH)2, Na2SO3, в принципе, могут проявлять как окислительные, так и восстановительные свойства, однако оксид марганца (IV) в кислых растворах – сильный окислитель, восстанавливающийся в соответствии со схемой:
MnO2 ® Mn2+;
соединения двухвалентной меди проявляют окислительные свойства, восстанавливаясь до соединений одновалентной меди:
Cu2+ ® Cu+1;
соединения железа (II) легко окисляются до соединений железа (III):
Fe2+ ® Fe3+; Fe(OH)2 ® Fe(OH)3;
растворимые соли железа (III) проявляют окислительные свойства, восстанавливаясь до соединений железа (II):
Fe3+ ® Fe2+;
сульфиты – сильные восстановители и легко окисляются до сульфатов:
SO32– ® SO42–.
Некоторые неметаллы (C, S, P, As) окисляются концентрированной азотной кислотой до высшей степени окисления:
С ® CO2; S ® SO42– P ® H3PO4 As ® H3AsO4
Йод окисляется азотной кислотой до степени окисления +5: I2 ® HIO3.
Сама HNO3 в этих реакциях может восстанавливаться как до NO2, так и до NO.
Неметаллы могут также окисляться концентрированной серной кислотой:
С ® CO2; S ® SO2 H2 ® H2O P ® H3PO4
При этом H2SO4 восстанавливается до SO2.
Далее рассматриваются примеры, иллюстрирующие использование приведённого выше теоретического материала при прогнозировании продуктов окислительно-восстановительных реакций.
Пример 4.1 Спрогнозируйте продукты следующей окислительно-восста-новительной реакции и составьте уравнение реакции ионно-электронным методом (т.е. методом полуреакций): K2Cr2O7 + N2H4 + H2SO4 ® ….
При выполнении данного задания следует учитывать, что запись H2SO4 в условии подразумевает разбавленную серную кислоту; если в реакции участвует концентрированная серная кислота – будет применяться запись H2SO4 (конц.).
Разбавленная серная кислота в подавляющем большинстве окислительно-восстановительных реакций (исключение – реакции с активными металлами) не проявляет себя ни как окислитель, ни как восстановитель и применяется для создания кислой среды. Следовательно, окислитель и восстановитель нужно искать среди двух оставшихся веществ. Атом хрома в K2Cr2O7 находится в высшей степени окисления +6. Поэтому в любой окислительно-восстановительной реакции K2Cr2O7 ведёт себя как окислитель. В кислой среде дихромат-ионы восстанавливаются до ионов Cr3+: Cr2O72– ® 2Cr3+.
В молекуле N2H4 атом азота находится в промежуточной степени окисления минус 2. Теоретически атом в промежуточной степени окисления может быть как окислителем, так и восстановителем. Но в данной реакции функцию окислителя выполняет K2Cr2O7. Поэтому гидразин (N2H4) – восстановитель. Как уже было ранее сказано, атомы-восстановители в отрицательной степени окисления обычно окисляются до нулевой степени окисления. Поэтому, даже не зная химии гидразина, можно предположить, что продуктом его окисления в данной реакции будет азот: N2H4 ® N2.
Исходные схемы превращений: Cr2O72– ® 2Cr3+
N2H4 ® N2
Процедура составления ионно-электронных уравнений подробно рассмотрена в методических указаниях по общей химии [2]. Напомним кратко важнейшие правила уравнивания атомов кислорода и водорода при составлении полуреакций.
В ту часть составляемого ионно-электронного уравнения реакции, протекающей в кислой среде, где имеется недостаток атомов кислорода, следует записать на каждый недостающий атом О одну молекулу Н2О, а в другую часть уравнения – два иона Н+.
В ту часть составляемого ионно-электронного уравнения реакции, протекающей в кислой среде, где не хватает атомов водорода следует записать нужное количество ионов Н+.
 Cr2O72– + 14H+ + 6e– ® 2Cr3+ + 7H2O 2
Cr2O72– + 14H+ + 6e– ® 2Cr3+ + 7H2O 2
N2H4 ® N2 + 4H+ + 4e– 3
 |
2Cr2O72– + 3N2H4 + 28H+ ® 4Cr3+ + 3N2 + 12H+ + 14H2O
2Cr2O72– + 3N2H4 + 16H+ ® 4Cr3+ + 3N2 + 14H2O
2K2Cr2O7 + 3N2H4 + 8H2SO4 ® 3N2 + 2Cr2(SO4)3 + 2K2SO4 + 14H2O
Пример 4.2 Спрогнозируйте продукты следующей окислительно-восстановительной реакции и составьте уравнение реакции ионно-электронным методом (т.е. методом полуреакций): Cl2 + KOH ® ….
Щёлочи (LiOH, NaOH, KOH, Ca(OH)2, Ba(OH)2) в водных растворах не проявляют ни окислительных, ни восстановительных свойств. При проведении окислительно-восстановительных реакций эти вещества используются для создания щелочной среды. Следовательно, и окислителем, и восстановителем в данной реакции являются атомы хлора; это реакция самоокисления-самовосстановления (реакция диспропорционирования).
Атомы хлора (нулевая степень окисления), являющиеся окислителем, принимают электроны; их степень окисления становится равной минус 1: Cl2 ® 2Cl–.
Другая часть атомов хлора отдают электроны и приобретают положительную степень окисления; обычно, в реакциях диспропорционирования галогенов это или степень окисления +1 (например, HClO, KClO) или +5 (например, HClO3, KClO3). Очевидно, что в щелочной среде продуктом реакции не может быть кислота. Следовательно, при окислении хлора в щелочной среде может получиться соль (KClO или KClO3). Рассмотрим, например превращение Cl2 ® 2ClO3–.
Исходные схемы превращений: Cl2 ® 2Cl–
Cl2 ® 2ClO3–
В ту часть составляемого ионно-электронного уравнения реакции, протекающей в щелочной среде, где недостаёт атомов кислорода, следует записать на каждый недостающий атом кислорода два иона OH–, а в другую часть уравнения – одну молекулу H2O.
 Cl2 + 2e– ® 2Cl– 5
Cl2 + 2e– ® 2Cl– 5
Cl2 + 12OH– ® 2ClO3– + 6H2O + 10e– 1
 |
6Cl2 + 12OH– ® 10Cl– + 2ClO3– + 6H2O
3Cl2 + 6OH– ® 5Cl– + ClO3– + 3H2O
3Cl2 + 6KOH ® 5KCl + KClO3 + 3H2O
Пример 4.3. Спрогнозируйте продукты следующей окислительно-восста-новительной реакции и составьте уравнение реакции ионно-электронным методом (т.е. методом полуреакций): KMnO4 + H2O2 + KOH ® ….
Атом марганца в KMnO4 находится в высшей степени окисления +7. Поэтому в любой окислительно-восстановительной реакции KMnO4 проявляет свойства окислителя. В щелочной среде атом Mn+7 в составе перманганат-иона восстанавливается до Mn+6 (образуется манганат-ион): MnO4– ® MnO42–.
KOH обеспечивает щелочную среду и не проявляет окислительно-восстановительную активность (см. пример 4.2). Следовательно, восстановителем являются атомы кислорода в молекуле H2O2, степень окисления которых равна минус 1 (промежуточная). Атомы кислорода O–1 окисляются до нулевой степени окисления (типичное поведение восстановителя в отрицательной степени окисления): H2O2 ® O2.
Исходные схемы превращений: MnO4– ® MnO42–
H2O2 ® O2
Составление полуреакции превращения H2O2 ® O2 требует уравнивания атомов водорода: если в какой-либо части составляемого ионно-электронного уравнения реакции, протекающей в щелочной среде, имеется избыток атомов водорода, то в эту часть уравнения на каждый избыточный атом водорода следует записать один ион OH–, а в другую часть уравнения – одну молекулу Н2О.
 MnO4– + e– ® MnO42– 2
MnO4– + e– ® MnO42– 2
H2O2 + 2OH– ® O2 + 2H2O + 2e– 1
 |
2MnO4– + H2O2 + 2OH– ® 2MnO42– + O2 + 2H2O
2KMnO4 + H2O2 + 2KOH ® 2K2MnO4 + O2 + H2O
Пример 4.4. Спрогнозируйте продукты следующей окислительно-восста-новительной реакции и составьте уравнение реакции ионно-электронным методом (т.е. методом полуреакций): KMnO4 + NaNO2 + H2O ® ….
Атом марганца в KMnO4 находится в высшей степени окисления +7 (окислитель). В нейтральной среде (в левой части уравнения – молекулы воды) KMnO4 (Mn+7) восстанавливается до MnO2 (Mn+4): MnO4– ® MnO2¯.
Атом азота в NaNO2 находится в промежуточной степени окисления +3 и поэтому нитрит натрия выступает в качестве восстановителя, окисляясь до нитрата: NO2– ® NO3–.
Исходные схемы превращений: MnO4– ® MnO2¯
NO2– ® NO3–
Следует иметь в виду, что в ходе реакции, которая начинается в нейтральной среде, может происходить либо подкисление раствора, либо подщелачивание, либо среда раствора останется без изменений.
Таким образом, в рассматриваемом примере при составлении полуреакций нужно определиться, как уравнивать атомы кислорода: с помощью ионов H+ и молекул H2O (кислая среда) или же с помощью ионов OH– и молекул H2O (щелочная среда).
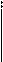 Если предпринять попытку уравнять атомы кислорода по правилу для кислой среды, то получится следующий результат:
Если предпринять попытку уравнять атомы кислорода по правилу для кислой среды, то получится следующий результат:
MnO4– + 4H+ + 3e– ® MnO2¯ + 4H2O 2
NO2– + H2O ® NO3– + 2H+ + 2e– 3
 |
2MnO4– + 3NO2– + 8H+ + 3H2O ® 2MnO2¯ + 3NO3– + 6H+ + 4H2O
2MnO4– + 3NO2– + 2H+ ® 2MnO2¯ + 3 NO3– + H2O
Этот результат противоречит условию: в левой части ионно-молекулярного уравнения оказались ионы Н+, хотя по условию реакция должна начинаться в нейтральной среде. Следовательно, уравнивание атомов кислорода лучше выполнить с помощью ионов OH– и молекул H2O.
 MnO4– + 2H2O + 3e– ® MnO2¯ + 4OH– 2
MnO4– + 2H2O + 3e– ® MnO2¯ + 4OH– 2
NO2– + 2OH– ® NO3– + H2O + 2e– 3
 |
2MnO4– + 3NO2– + 6OH– + 4H2O ® 2MnO2¯ + 3NO3– + 8OH– + 3H2O
2MnO4– + 3NO2– + H2O ® 2MnO2¯ + 3NO3– + 2OH–
2KMnO4 + 3NaNO2 + H2O ® 2MnO2¯ + 3NaNO3 + 2KOH
Варианты заданий по теме прогнозирование продуктов окислительно-восстановительных реакций представлены в таблице 4.1
 2015-02-04
2015-02-04 18963
18963
