Условие: Какой теоретический объем воздуха необходим для полного сгорания 1 кг диэтилового эфира С2Н5ОС2Н5? Температура 100С, давление 1,2 ат, остаточное содержание кислорода в продуктах сгорания 15%.
Решение:
1. Записывают уравнение реакции горения в воздухе
С2Н5ОС2Н5 + 6(О2 + 3,76N2) =4СО2 + 5Н2О +6×3,76N2
Коэффициент перед воздухом обозначается 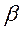 . В данном случае
. В данном случае 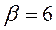
2. Определяют сколько киломолей воздуха необходимо для сжигания одного килограмма горючего.
Из уравнения горения получаем, что для сжигания 1 кмоля горючего требуется:
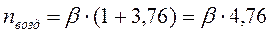
Зная молярную массу горючего можно сказать, что 1 киломоль весит М кг. В рассматриваемом случае М=4·12+10·1+16=74 кг.
Можно записать следующую пропорцию:
Для сжигания М кг (1 кмоль) горючего - требуется 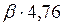 кмолей воздуха
кмолей воздуха
Для сжигания 1 кг горючего – требуется n кмолей воздуха
ОТСЮДА:
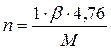 ,
,
для рассматриваемого случая:
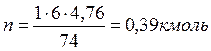
То есть, для сжигания 1 кг диэтилового эфира требуется 0,39 кмоль воздуха.
3. Определяют какой объем занимает найденное количество киломолей воздуха при заданных условиях.
Известно, что 1 кмоль любого газа или пара при нормальных условиях занимает объем равный 22,4 м3, т.е. молярный объем при Н.У. 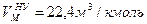
Если условия отличаются от нормальных, то необходимо определить, какой объем будет занимать 1 кмоль любого газообразного вещества при данных условиях. Расчет VМ ведут по формуле объединенного газового закона:
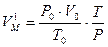 ,
,
где:
Р и Т – данные в задаче температура и давление,
P0, V0, T0 – cоответственно давление, молярный объем и температура при нормальных условиях.
Для заданных в задаче условий:
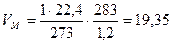 м3/кмоль
м3/кмоль
Исходя из этого, 0,39 кмоль воздуха при заданных условиях займут следующий объем:
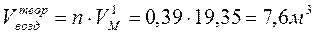
4. Поскольку согласно условий задачи, при горении расходуется не весь кислород воздуха, то коэффициент избытка воздуха 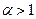 , поэтому следует учесть избыток воздуха при горении.
, поэтому следует учесть избыток воздуха при горении.
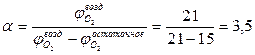
5. Практический расход воздуха равен:
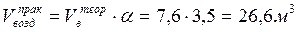
Ответ: Удельный теоретический расход воздуха при горении диэтилового эфира при заданных условиях составляет 7,6 м3/кг, практический расход 26,6 м3/кг
 2015-03-27
2015-03-27 2882
2882








