Условие: Представить диэтиловый эфир С2Н5ОС2Н5 в виде вещества сложного элементного состава и рассчитать теоретический объем воздуха, необходимый для полного сгорания 1 кг этого вещества? Температура 100С, давление 1,2 ат, остаточное содержание кислорода в продуктах сгорания 15%.
Решение:
1. Вычислим массовые доли элементов в веществе:
Молярная масса диэтилового эфира составляет
М(С4Н10О) = 12×4 + 10 + 16 = 74 кг/кмоль
w (С) = 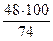 = 64,9 %;
= 64,9 %;
w (Н) = 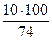 = 13,5 %;
= 13,5 %;
w (О) = 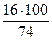 = 21,6 %.
= 21,6 %.
2. Условия отличаются от нормальных, следовательно, необходимо определить, какой объем будет занимать 1 кмоль любого газообразного вещества при данных условиях (расчет VМ).
Для заданных в задаче условий:
VМ = 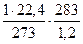 = 19,35 м3/кмоль.
= 19,35 м3/кмоль.
3. Теоретический объем воздуха, необходимый для полного сгорания, составит:
Vвтеор = 1× 0,0119× 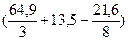 × 19,35 = 7,5 м3
× 19,35 = 7,5 м3
4. Коэффициент избытка воздуха по условию задачи
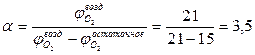
5. Практический расход воздуха равен:
Vвпракт = 7,5 × 3,5 = 26,3 м3
Ответ: удельный теоретический расход воздуха при горении диэтилового эфира при заданных условиях составляет 7,5 м3/кг, практический расход 26,3 м3/кг.
 2015-03-27
2015-03-27 653
653








