При изучении сплавов пользуются специальными терминами: система, компонент, фаза, структурная составляющая.
Системой называют группу сплавов, выделяемую для изучения их строения и свойств. Понятия система «медь – никель» или система «железо – углерод» означают, что для исследования берут сплавы с различной концентрацией (содержанием) в первом случае меди и никеля, во втором – железа и углерода.
Компонентами называют вещества, образующие систему. Компонентами могут быть чистые металлы, неметаллы, устойчивые химические соединения. Например, в сплавах железа с углеродом компонентами будут железо (чистый металл) и карбид железа Fe3C (химическое соединение). В этом случае получается система сплавов Fe – Fe3C.
Фаза – однородная часть сплава, имеющая свой состав, свойства и видимую границу раздела. Сплавы могут быть однофазные, когда все кристаллы однородны, имеют один состав и одинаковые свойства, а границы позволяют судить об их форме и размерах. Сплавы могут быть двух- и многофазные, если они состоят из различных по составу и свойствам кристаллов.
В большинстве случаев входящие в сплав компоненты в жидком состоянии полностью растворимы друг в друге и представляют собой жидкий раствор (одна фаза – жидкость). В твердом состоянии сплавы образуют твердые растворы, химические соединения и механические смеси (рис. 19).
Структурная составляющая – это однородная часть строения, образовавшаяся в результате первичной или вторичной кристаллизации сплава как из жидкого, так и из твердого раствора. Структурная составляющая может состоять из одной или нескольких фаз.
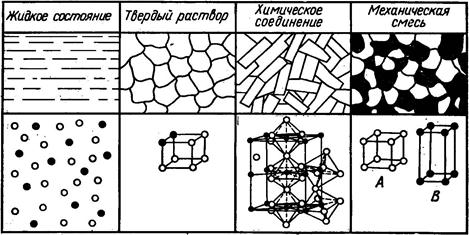
Рис. 19. Структура и строение элементарной ячейки пространственной
кристаллической решетки различных сплавов из двух металлов:
● – атомы металла А; ○ – атомы металла В
 В системе сплавовFe – Fe3C в отличие от других систем фазы, как и структурные составляющие, имеют названия и обозначения, единые в мире. Например, химическое соединение железа с углеродом, имеющее формулу Fe3C (карбид железа), называется цементитом, и на всех языках мира это произносится одинаково.
В системе сплавовFe – Fe3C в отличие от других систем фазы, как и структурные составляющие, имеют названия и обозначения, единые в мире. Например, химическое соединение железа с углеродом, имеющее формулу Fe3C (карбид железа), называется цементитом, и на всех языках мира это произносится одинаково.
Твердым раствором называется сплав, в котором атомы растворенного компонента или компонентов находятся в кристаллической решетке компонента растворителя. Кристаллическую решетку строит один компонент сплава – растворитель. Другой компонент (или компоненты) своими атомами размещается в этой решетке, изменяя ее размеры (параметры).
По расположению атомов в кристаллической решетке различают твердые растворы замещения и твердые растворы внедрения. В твердом растворе замещения атомы растворенного компонента занимают места атомов элемента растворителя, т. е. расположены в узлах общей кристаллической решетки (рис. 20, а). В твердом растворе внедрения атомы растворенного компонента располагаются внутри кристаллической решетки компонента растворителя между его атомами (рис. 20, б).
Твердый раствор состоит из двух или нескольких компонентов, имеет один тип решетки и представляет собой одну фазу. Твердые растворы мягки и пластичны. Благодаря высокой пластичности они хорошо поддаются ковке и другим видам обработки давлением. Литейные свойства и обрабатываемость резанием у твердых растворов низкие.
В системе железоуглеродистых сплавов существуют два твердых раствора. Твердый раствор углерода в альфа-железе называется ферритом. Альфа-железо растворяет углерода очень мало: от 0,006 % при 0°С до 0,025 % при 727°С. Поэтому феррит можно считать технически чистым железом. Твердость феррита (как и железа) – НВ80.
Твердый раствор углерода в гамма-железе называется аустенитом. Растворимость углерода в гамма-железе значительно больше – до 2,14 % при 1147°С. При обычных условиях аустенит в железоуглеродистых сплавах может существовать только при температуре выше 727°С. Как все твердые растворы, феррит и аустенит пластичны (d = 40 – 50 %).
Химические соединения – это фазы, состав которых выражается химической формулой АnВm, где А и В – химические элементы; n и m – простые числа. Свойства и кристаллическая решетка отличаются от решеток компонентов, образующих соединение. С углеродом, азотом, бором металлы образуют химические соединения (карбиды, нитриды и бориды), характеризующиеся высокой твердостью. Так, в системе железоуглеродистых сплавов карбид железа тверже чистого железа в десять раз.
Механическая смесь (сплав-смесь) двух компонентов образуется тогда, когда они не образуют твердых растворов и химических соединений и кристаллы каждого компонента будут сохранять свои состав и свойства. Если в сплаве компоненты находятся в количестве, превышающем их предельную растворимость, то образуется смесь кристаллов твердого раствора и кристаллов химического соединения или смесь кристаллов двух твердых растворов и т. п. Сплавы- механические смеси имеют хорошие литейные свойства.
Сплав-смесь, получающийся из жидкости в результате первичной кристаллизации, называется эвтектикой, которая образуется при определенных температуре и концентрации компонентов сплава.
Сплав-смесь, образованный из твердого раствора при вторичной кристаллизации сплава, называется эвтектоидом, который, как и эвтектика, имеет постоянный химический состав и определенную температуру образования.
В системе железоуглеродистых сплавов эвтектическая смесь кристаллов аустенита и цементита называется ледебуритом, который образуется при температуре 1147°С и соответствует концентрации 4,3 % углерода. Второй сплав-смесь – эвтектоидная смесь кристаллов феррита и цементита – называется перлитом. Температура образования перлита – 727°С, а концентрация углерода – 0,8 %.
Кристаллизация сплавов. Процессы кристаллизации сплавов происходят значительно сложнее, чем чистых металлов. Особенности их кристаллизации можно проследить по кривым охлаждения. Как видно на кривой охлаждения сплава на рис. 21, его кристаллизация протекает в интервале температур от начала (Тнкр) до конца (Тккр) кристаллизации. Значения температуры, при которых в металлах или сплавах происходят какие-либо превращения, называются критическими точками. Следовательно, сплавы в отличие от чистых металлов при плавлении или кристаллизации, как правило, имеют не одну, а две критические точки.
 Сплав с температурой выше температуры начала кристаллизации (точка а на рис. 21) находится в однофазном жидком состоянии; ниже температуры конца кристаллизации (точка b) – в твердом однофазном состоянии. В интервале температур между критическими точками сплав двухфазный и состоит из жидкого раствора и твердых кристаллов. Как указывалось выше, для облегчения изучения сплавов их объединяют в системы.
Сплав с температурой выше температуры начала кристаллизации (точка а на рис. 21) находится в однофазном жидком состоянии; ниже температуры конца кристаллизации (точка b) – в твердом однофазном состоянии. В интервале температур между критическими точками сплав двухфазный и состоит из жидкого раствора и твердых кристаллов. Как указывалось выше, для облегчения изучения сплавов их объединяют в системы.
К конкретной системе относят все сплавы, состоящие из одних и тех же компонентов и отличающиеся друг от друга лишь количественным соотношением этих компонентов, т. е. концентрацией. Количество сплавов одной системы, но разной концентрации настолько велико, что изучать по кривым нагревания или охлаждения все превращения, происходящие в каждом из них, практически невозможно, да и нерационально.
Если какую-то систему изучать по кривым охлаждения сплавов с концентрацией компонентов, увеличивающейся каждый раз на 10 %, то нужно построить и изучить 10 кривых охлаждения. Например, первая кривая – 100 % компонента А и 0 % компонента B, затем – 90 % компонента А и 10 % – компонента В и т. д. Если рассматривать систему компонентов, увеличивающейся каждый раз на 5 %, то будет 20 сплавов, в случае увеличения на 1 %, будет 100 сплавов и т. д. Поэтому для изучения состояния сплавов выбранной системы в зависимости от температуры и концентрации строят ее диаграмму состояния. В настоящее время для всех сплавов, используемых в технике, диаграммы состояния построены и их можно найти в справочной литературе. Они имеют большое практическое значение при выборе режимов термической обработки и горячей обработки давлением, при выборе сплавов для литейного производства, для изготовления различных деталей и металлоконструкций.
 2015-03-08
2015-03-08 4315
4315
