Двухатомные спирты содержат в своем составе две гидроксильные группы. Общая формула гликолей СnH2n(OH)2.
По систематической номенклатуре названия двухатомных спиртов образуются от названия соответствующих алканов с прибавлением окончания «диол», положение -ОН групп указывается цифрами
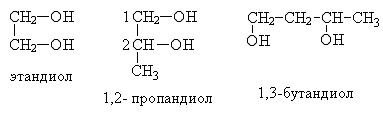
По рациональной номенклатуре сохраняются названия от соответствующих алкенов с прибавлением слова «гликоль»
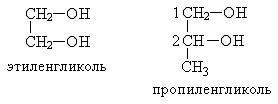
Способы получения гликолей
Двухатомные спирты можно получить теми же способами, что и одноатомные спирты, или другими.
Важнейшие из них – следующие:
1. Гидролиз дигалогенопроизводных:
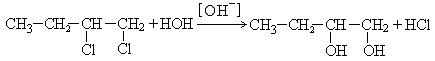
2. Гипохлорирование алкенов:
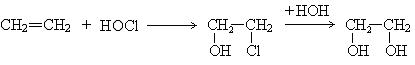
3. Гидролиз окиси этилена:
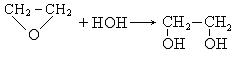
4. Окисление алкенов.
Химические свойства
За счет взаимного влияния атомов подвижность водорода в гидроксильных группах этиленгликоля значительно больше, чем в спиртах. Гликоли обладают большими кислыми свойствами, чем спирты, и взаимодействуют не только с активными металлами, но и с гидроксидами металлов, образуюя комплексные структуры.
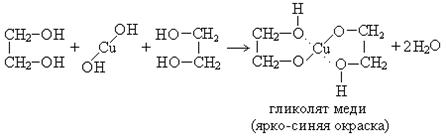
1. Взаимодействие с Cu(OH)2 (качественная реакция на гликоли):
2. Взаимодействие со спиртами:
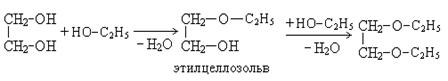
При этом происходит образование моно- и дипроизводных.
3. Межмолекулярная дегидратация гликолей:
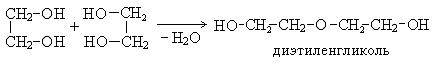
4. Взаимодействие с минеральными кислотами:
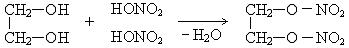
Нитроэфиры обладают взрывчатыми свойствами.
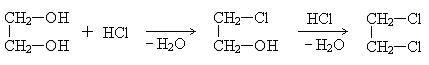
5. Гидрогалогенирование этиленгликоля:
Применение
Этиленгликоль – вязкая бесцветная жидкость, значительно уменьшает температуру замерзания воды и поэтому используется как антифриз, 60% водный раствор этиленгликоля замерзает при -50°С. Этиленгликоль применяется в органическом синтезе для получения полиэфиров, смол, волокна ловсан.
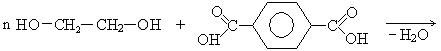
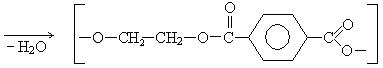
лавсан
Применяется также при изготовлении печатных красок, нанесении рисунка на ткань.
 2015-03-20
2015-03-20 13960
13960








