Реактивы:
1) 0,1 н раствор трилона Б;
2) аммонийно–буферный раствор;
3) индикатор кислотный хром темно–синий.
Ход работы. В коническую колбу отмерить 100 мл исследуемой воды. Добавить 5 мл аммонийной буферной смеси, 5 – 8 капель индикатора кислотного хрома темно–синего и титровать рабочим раствором трилона Б до перехода вишнево–красной окраски в синюю. Раствор трилона Б следует прибавлять по каплям, энергично перемешивая. Расчет жесткости следует производить по формуле:
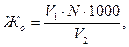
где Ж о – общая жесткость воды, мг-экв/л;
V1 – объем рабочего раствора трилона Б, пошедшего на титрование пробы воды, мл;
N – нормальность рабочего раствора трилона Б, мг-экв.л;
V2 – объем пробы воды, мл.
4.3 Определение ионов кальция и магния
Реактивы:
1) 0,1 н раствор трилона Б;
2) 2 н раствор NaOH;
3) индикатор мурексид сухой;
4) 5% раствор Na2S;
5) 1% раствор гидроксиламина;
6) индикатор хром темно–синий;
7) аммонийно–буферный раствор.
4.3.1 Определение ионов кальция
Ход работы. К 100 мл исследуемой воды добавляют 5 мл раствора NaOH, несколько (6 – 8) капель Na2S и на кончике лопаточки сухого мурексида. Раствор приобретает темно–розовую окраску. Медленно титруют раствором трилона Б до изменения окраски в винно–красную. Содержание кальция (х) вычисляют по формуле:
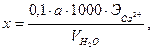
где х – содержание кальция в анализируемой воде, мг/л;
a – количество раствора трилона Б, пошедшее на титрование пробы, мл;
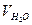 – количество пробы воды, взятое для определения, мл;
– количество пробы воды, взятое для определения, мл;
ЭСа2+ – эквивалент кальция, равный 20.
4.3.2 Определение ионов магния
Ход работы. В пробу после определения ионов кальция добавляют 5 мл аммонийно–буферного раствора, 5 – 6 капель гидроксиламина, 5 – 6 капель индикатора хром темно–синего и медленно титруют 0,1н раствором трилона Б до перехода окраски в синюю. Содержание магния (у) вычисляют по формуле:
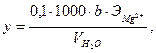
где у – концентрация ионов магния в анализируемой пробе, мг/л;
b – количество раствора трилона Б, пошедшее на титрование пробы, мл;
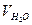 – количество пробы воды, взятое для определения, мл;
– количество пробы воды, взятое для определения, мл;
ЭМg2+ – эквивалент магния, равный 12.
 2015-03-20
2015-03-20 1409
1409
