Риск возникновения новообразований определяется:
1. Интенсивностью воздействия неблагоприятных факторов внешней среды.
2. Степенью предрасположенности к опухолям.
Для развития опухоли, как правило, недостаточно только воздействия, необходимо неблагоприятное сочетание генетических факторов, влияющих на процессы активации и инактивации канцерогенов, эффективность противоопухолевого иммунитета, баланс между делением, дифференцировкой и отмиранием клеток, механизмы репарации ДНК и др.
Появление новообразований явление не одномоментное, в генезе каждой неоплазмы принимают участие как минимум 5-6 относительно независимых мутаций.
По гипотезе Хьюгса, генная регуляция деления осуществляется в каждой клетке системой, состоящей из трех регуляторных генов. В норме отсутствует избыточное деление клеток, так как система генов, регулирующих деление клетки, обеспечивает торможение активности гена, кодирующего инициатор деления клетки. Клетка не делится, ибо появление инициатора клеточного деления при включении гена, кодирующего этот инициатор, тормозит функцию регуляторного гена-репрессора 2, что ведет к дерепрессии регуляторного гена-репрессора 1 и синтеза на его основе репрессора 1, который тормозит функцию гена, кодирующего инициатор клеточного деления (направление стрелок на схеме обозначает тормозящее влияние).
Таким образом, система регуляции имеет обратную связь, которая обеспечивает ее автономность и благодаря ей в норме регуляция установлена на предупреждение клеточного деления.
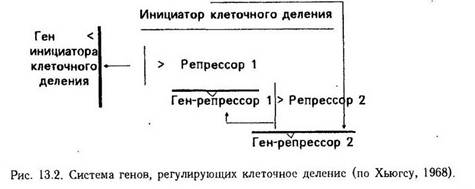 Для размножения клетки необходимо наличие в геноме фактора, который предупреждает репрессию гена-репрессора 2 компонентом инициатора клеточного деления или репрессию гена-инициатора клеточного деления репрессором 1. Если этого фактора нет, система регуляторных генов выключает ген-инициатор. Размножение клетки приостанавливается. На основе схемы регуляции клеточного деления Хьюгса можно представить сущность канцерогенеза.
Для размножения клетки необходимо наличие в геноме фактора, который предупреждает репрессию гена-репрессора 2 компонентом инициатора клеточного деления или репрессию гена-инициатора клеточного деления репрессором 1. Если этого фактора нет, система регуляторных генов выключает ген-инициатор. Размножение клетки приостанавливается. На основе схемы регуляции клеточного деления Хьюгса можно представить сущность канцерогенеза.
Онкоген - один из генов, который в обычных условиях кодирует белок и обеспечивает пролиферацию и дифференцировку клеток (к ним относятся ядерные белки, факторы роста). При мутации онкогенов или активации ретровирусами они могут спровоцировать злокачественный рост. Известно множество онкогенов (ras, р53, мутантный ген хромосомы 17).
Превращение протоонкогена в онкоген приводит к синтезу онкобелка – в количественном или качественном отношении измененного продукта протоонкогена. Онкобелок появляется в клетке либо в увеличенном количестве, либо приобретает измененную структуру и свойства, что обеспечивает данному белку повышенную активность и нарушает его реакцию на регуляторные воздействия. По локализации в клетке различают ядерные, цитоплазматические и мембранные онкобелки.
Ядерные онкобелки), работая в ядре, выполняют роль индукторов и репрессоров генома. С их влиянием связан синтез раковой клеткой необычных для данной стадии онтогенеза или для данной ткани белков (эмбриональные и гетероорганные антигены, эктопические гормоны и т. п.). Цитоплазматические онкобелки являются протеинкиназами, осуществляющими модификацию различных клеточных белков путем фосфорилирования остатков тирозина, серина или треонина. Эти онкобелки ответственны за изменения клеточного метаболизма и приобретение фенотипа, типичного для опухолевой клетки. Онкобелки, локализованные на наружной клеточной мембране могут выступать в качестве рецепторов для естественных факторов роста или сами выполнять роль факторов роста, побуждающих клетку к делению даже в отсутствие внешнего стимула.
Под влиянием онкобелков нарушается регуляция клеточного роста, пролиферации и дифференцировки, создаются условия для ускоренной репликации ДНК и непрерывного деления клетки.
 2015-03-20
2015-03-20 2309
2309







