Пример 3. Как изменится скорость реакции, если общее давление в системе СН4(Г) + 2О2(Г) = СО2(Г) + 2Н2О(Г), уменьшить в 5 раз?
Решение.
В соответствии с кинетическим уравнением реакции, скорость этой реакции будет определяться:
V 1 = k [СН4] · [О2] 2.
При уменьшении давления в пять раз концентрация каждого из газообразных веществ уменьшится также в пять раз. Кинетическое уравнение реакции в этих условиях будет следующим:
V 2 = k 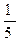 [СН4] · (
[СН4] · ( 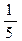 [О2]) 2 =
[О2]) 2 = 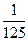 k [СН4] · [О2] 2.
k [СН4] · [О2] 2.
Сравнивая скорости реакций до и после изменения давления
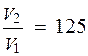
можно определить, что скорость реакции уменьшилась в 125 раз.
 2015-04-12
2015-04-12 798
798








