К газам в стали относят, как правило, азот и водород. Особенностью растворения азота и водорода в металлических расплавах является то, что они диссоциируют на атомы. В этом случае реакция растворения газа (Г) записывается в виде
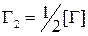 . (34)
. (34)
Величина растворимости газов в чистых металлах невелика (например, при 1873 К растворимость азота в железе составляет 0,044%). Растворы можно считать разбавленными и подчиняющимися закону Сивертса (частный случай закона Генри):
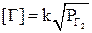 , (35)
, (35)
где 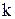 – константа Сивертса, являющаяся функцией температуры.
– константа Сивертса, являющаяся функцией температуры.
Если рассмотреть растворение газов в сплавах, то вместо концентрации следует подставлять значение активности, тем самым учитывать влияние добавляемого элемента на растворимость газа. Связь между растворимостью газа в чистом металле и легированном растворе можно определить, исходя из следующих соображений.
Допустим, что при постоянных температуре и давлении в равновесии с газовой фазой (Г) находятся два расплава: чистый металл (`) и металл с добавками легирующих элементов (``). Естественно, что активность азота в обоих растворах должна быть одинаковой:
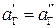 . (36)
. (36)
Причем
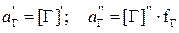 . (37)
. (37)
Из соотношений (36), (37) следует
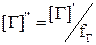 . (38)
. (38)
Выражение (38) позволяет рассчитать концентрацию азота в расплаве известного состава. Значение коэффициента активности целесообразно определять по значениям параметров взаимодействия 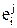 (табл. 10). Константу равновесия реакции (34) определяют по данным об изменении энергии Гиббса (табл. 11).
(табл. 10). Константу равновесия реакции (34) определяют по данным об изменении энергии Гиббса (табл. 11).
При изменении давления и температуры жидкого металла возможно как выделение газа, так и поглощение его расплавом. Для расчета объема газа, выделившегося из расплава при понижении давления и постоянной температуре можно использовать уравнение Менделеева – Клапейрона:
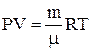 , (39)
, (39)
где 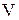 – объем газа,
– объем газа, 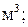
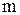 – масса газа,
– масса газа, 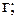
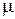 – молекулярная масса газа, г/моль; R=8,314 Дж/(моль·К) – газовая постоянная.
– молекулярная масса газа, г/моль; R=8,314 Дж/(моль·К) – газовая постоянная.
Таблица 10
Значение параметров взаимодействия 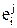 в расплавах на основе
в расплавах на основе 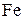 и
и 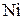 [1]
[1]
| Растворитель | 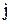 | 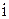 | ||||
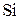 | 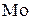 | 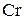 | 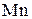 | 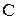 | ||
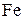 | N | 0,047 | –0,0123 | –0,0467 | –0,0197 | 0,123 |
| H | 0,026 | 0,0020 | 0,0033 | –0,0012 | 0,065 | |
 | N | –0,043 | –0,1000 | –0,051 | 0,090 | |
| H | 0,033 | 0,0020 |
Таблица 11
Изменение энергии Гиббса при растворении газов [4]
| Растворитель | Газ | 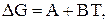 Дж/моль Дж/моль | |
| A | B | ||
 | N | 10 500 | 20,37 |
| H | 36 500 | 30,46 | |
 | N | 69 270 | 18,68 |
| H | 20 100 | 35,10 |
Задание
1. Определить растворимость азота и водорода в расплаве 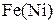 , а также в легированных расплавах на их основе, при температурах Т1 и Т2
, а также в легированных расплавах на их основе, при температурах Т1 и Т2 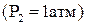 .
.
2. Рассчитать объем газа, выделившегося из расплава при уменьшении давления с 1 атмдо величины 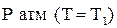 . Данные в табл. 12.
. Данные в табл. 12.
Таблица 12
| № вари-анта | 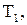 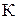 | 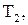 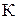 | 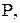 атм атм | Содержание легирующих элементов, % | |||||||
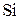 | 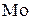 | 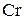 | 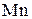 | 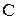 | |||||||
| 0,01 | 0,5 | 1,0 | 1,0 | 0,5 | 0,1 | ||||||
| 0,03 | 0,6 | 0,9 | 1,5 | 0,6 | 0,2 | ||||||
| 0,10 | 0,7 | 0,8 | 2,0 | 0,7 | 0,3 | ||||||
| 0,20 | 0,8 | 0,7 | 2,5 | 0,8 | 0,4 | ||||||
| 0,30 | 0,9 | 0,6 | 3,0 | 0,9 | 0,5 | ||||||
| 0,40 | 1,0 | 0,5 | 3,5 | 1,0 | 0,6 | ||||||
| 0,50 | 1,1 | 0,4 | 4,0 | 1,1 | 0,7 | ||||||
| Окончание табл. 12 | |||||||||||
| № вари-анта | 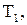 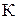 | 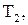 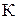 | 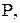 атм атм | Содержание легирующих элементов, % | |||||||
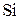 | 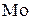 | 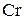 | 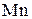 | 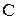 | |||||||
| 0,40 | 1,2 | 0,3 | 4,5 | 1,2 | 0,8 | ||||||
| 0,30 | 1,3 | 0,2 | 5,0 | 1,3 | 0,9 | ||||||
| 0,20 | 1,4 | 0,1 | 5,5 | 1,4 | 1,0 | ||||||
| 0,10 | 1,5 | 0,2 | 6,0 | 1,5 | 1,1 | ||||||
| 0,01 | 1,6 | 0,3 | 6,5 | 1,6 | 1,2 | ||||||
| 0,05 | 1,7 | 0,4 | 7,0 | 1,7 | 1,2 | ||||||
| 0,15 | 1,8 | 0,5 | 7,5 | 1,8 | 1,1 | ||||||
| 0,25 | 1,9 | 0,6 | 8,0 | 1,9 | 1,0 | ||||||
| 0,35 | 2,0 | 0,7 | 8,5 | 2,0 | 0,9 | ||||||
| 0,45 | 1,9 | 0,8 | 9,0 | 1,9 | 0,8 | ||||||
| 0,55 | 1,8 | 0,9 | 9,5 | 1,8 | 0,7 | ||||||
| 0,50 | 1,7 | 1,0 | 10,0 | 1,7 | 0,6 | ||||||
| 0,03 | 1,6 | 1,1 | 9,0 | 1,6 | 0,5 | ||||||
| 0,13 | 1,5 | 1,2 | 8,0 | 1,5 | 0,4 | ||||||
| 0,27 | 1,4 | 1,3 | 7,0 | 1,4 | 0,3 | ||||||
| 0,33 | 1,3 | 1,4 | 6,0 | 1,3 | 0,2 | ||||||
| 0,01 | 1,2 | 1,5 | 5,0 | 1,2 | 0,1 | ||||||
| 0,47 | 1,1 | 1,6 | 4,0 | 1,1 | 1,0 | ||||||
Контрольные вопросы:
1. Понятие растворимости газов в металле.
2. Закон Сивертса.
3. Факторы, влияющие на растворимость газов в металле.
4. Расчет растворимости газов в чистом металле.
5. Расчет растворимости газов в легированном расплаве.
 2015-04-01
2015-04-01 2867
2867
