Реакции гидратации сводятся к присоединению воды по ненасыщенным С——С-связям:
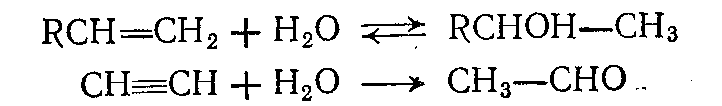
тройной С—N связи нитрилов.: 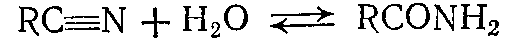 .
.
Это отличает их от гидролиза. Реакции гидратации являются обратимыми (равновесными) и сильно экзотермическими.
Процессы гидратации по способу проведения различают:
1) двухстученчатую гидратацию, при которой сначала при взаимодействии алкена со свободной серной кислотой образовывалась алкилсерная кислота, а затем ее гидролизовали с получением спирта (сернокислотная гидратация), в этом случае серная кислота выполняет две функции- реагента и катализатора:
- 1-ая стадия — отщепление протона от молекулы кислоты, образование карбокатиона и изопропилсульфата относится к реакциям электрофильного присоединения:
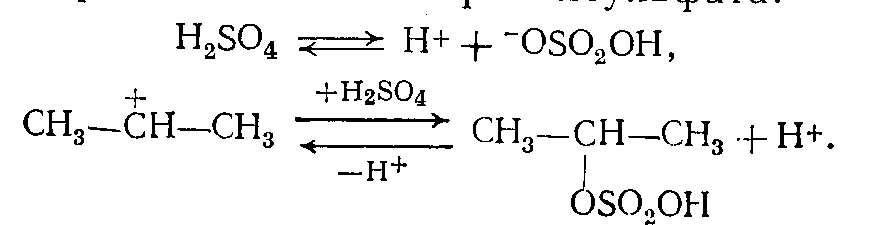
Побочно образуется диалкилсульфат:
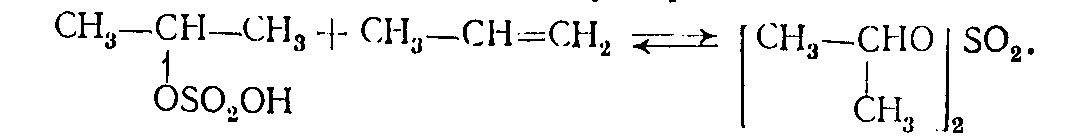
Первую стадию:
а) этилена проводят 96—98%-ной серной кислотой в тарельчатом колонном абсорбере при 80°С и 2,5 МПа;
б) пропилена проводят 70%-ной кислотой при 0,8 МПа и 65—70°С. а соотношение кислоты и пропилена берут таким, чтобы на 1 моль кислоты поглощалось 1,2—1,3 моль олефина.
Реакционная способность олефинов изменяется в последовательности
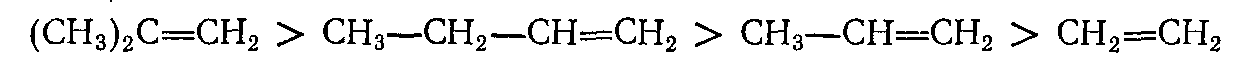
Присоединение происходит по правилу Марковникова, вследствие чего из изоолефинов получаются третичные, из
н-олефинов (кроме этилена)— вторичные и только из этилена — первичные алкилсульфаты и соответствующие им спирты и простые эфиры.
-2-я стадия- это гидролиз полученного алкилсульфата:
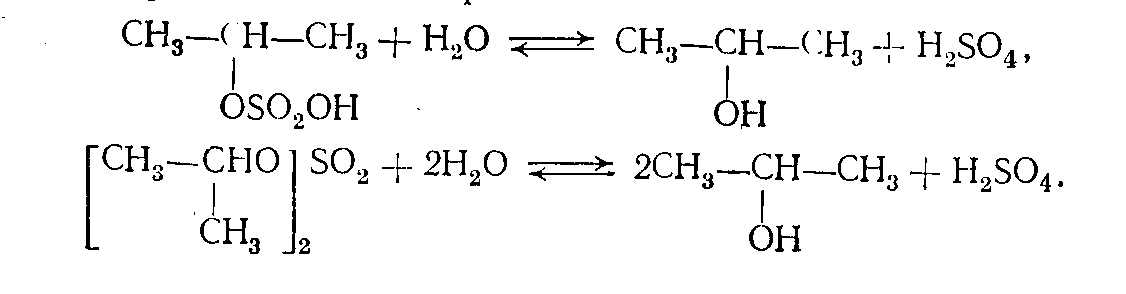
Гидролиз проводят при 2,5 МПа и 65—75 °С в отпарной колонне под действием острого пара.
Побочными продуктами гидратации являются простые эфиры, полимеры, диалкилсульфаты. В общем виде механизм сернокислотной гидратации с образованием основных и побочных продуктов на примере этилена можно записать:
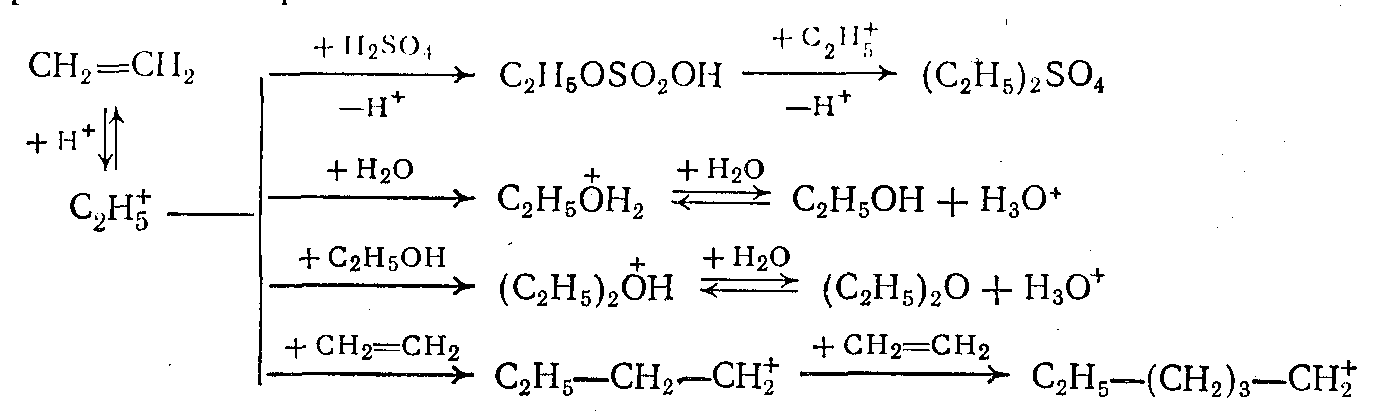
Метод сернокислотной гидратации не получил дальнейшего распространения из-за его неэкономичности: процесс характеризуется высоким расходом серной кислоты, необходимостью применения дорогостоящего кислотостойкого оборудования, а также наличием значительных количеств отходов и побочных продуктов.
 2015-04-20
2015-04-20 865
865








