В пожарных расчетах наиболее распространенным способом определения давления насыщенного пара при заданной температуре является расчет по уравнению Антуана:
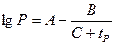
 ; Рs
; Рs 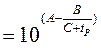 ,
,
где
Рs - давление насыщенного пара, кПа;
tР - рабочая (заданная) температура, 0С;
А, В, С - константы уравнения Антуана из справочной литературы [4].
(таблица 5 приложения).
| Расчет давления насыщенного пара по уравнению Антуана | Пример 9. Определить давление насыщенного пара толуола С6Н5СН3 при температуре 200С по уравнению Антуана. |
Решение:
Для нашей задачи:
tР = 200С;
Константы уравнения Антуана для толуола
А = 6,0507; В = 1328,17; С = 217,713.
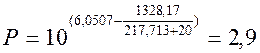 кПа.
кПа.
Давление насыщенного пара может быть так же определено по номограмме (в мм рт.ст.)
Зная давление насыщенного пара можно рассчитать его концентрацию в паро-воздушной смеси и установить пожарную опасность смеси насыщенного пара с воздухом.
| Расчет объемной концентрации паров по давлению насыщенного пара | Пример 10. Резервуар заполнен бензолом С6Н6. Вычислить объемную и массовую концентрацию паров бензола в свободном пространстве резервуара. Температура 100С, давление 780 мм рт.ст. |
Решение:
Зная величину давления насыщенного пара в емкости, можно определить объемную концентрацию паров жидкости при данных условиях. Величина давления насыщенного пара не зависит от объема жидкости в резервуаре.
Объемная концентрация паров (газов) в замкнутом объеме рассчитывается через давление насыщенного пара по формуле:
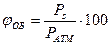 , %,
, %,
где
jОБ - объемная концентрация газа или пара, %;
Р S - давление насыщенного пара при данной температуре, мм рт.ст., кПа,
МПа, атм; Р s рассчитывают по уравнению Антуана или определяют по
номограмме.
Р АТМ - внешнее давление, мм рт.ст., кПа, МПа, атм.
При температуре 100С для бензола Р ПАР = 40 мм рт.ст.(по номограмме). Тогда
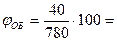 5,1 %
5,1 %
Определяем массовую концентрацию паров бензола.
Для этого воспользуемся формулой для определения массовой концентрации паров
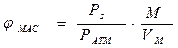
где
jМАС - массовая концентрация, кг(г)/м3;
Рs - давление насыщенного пара, мм рт.ст., кПа, МПА, атм;
Р АТМ - внешнее давление, мм рт.ст., кПа, МПа, атм;
М - молярная масса вещества, г/моль, кг/кмоль,
VМ - молярный объем газа или пара, л/моль, м3/кмоль.
Для нашей задачи:
М (С6Н6) = 78 кг/кмоль;
VМ необходимо рассчитать.
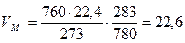 м3/кмоль.
м3/кмоль.
Рассчитаем массовую концентрацию паров бензола.
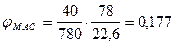 кг/м3 = 177 г/м3.
кг/м3 = 177 г/м3.
Зная концентрационные пределы распространения пламени вещества и объемную концентрацию его паров, можно оценить взрывоопасность паров при заданной температуре. Так КПР бензола составляет от 1,4 до 7,1 % (объемных). Сравним этот интервал с полученной объемной концентрацией паров бензола при заданных условиях – 5,1 %. Можно сделать вывод, что данная концентрация паров бензола взрывоопасна.
 2015-05-05
2015-05-05 23565
23565
