Егер температуралардың бұл айырымы (Т~Тх) жоғары болса, онда жұмысшы денемен сақталған жылуды жоғары потенциалды деп аталады, керісінше, егер бұл айырым төмен болса, онда жылуды төмен потенциялды деп атайды. Жылу көзінің потенциялы түсінігі кең пайдаланатын «энтропия» түсінігімен дублденеді.
«Энтропия» сөзі entropia деген грек сөзінен шыққан, мағынасы айналым немесе айналу. Бұл сөзді Петербург ғылым академиясының корреспондент – мүшесі, неміс физигі Р. Клаузиус (1822 - 1888) енгізді. Энтропияда потенциал сияқты есептеу басының орнатылған деңгейі болмайды; есептерде тек оның айналуларын пайдаланады:
S = q\T
Мұндағы q = c (T – Tx) – қарастырылатын үрдісте жылу көзінің энтальпийлерінің ауыспалы айырмасы; с – оның меншікті жылу сыйымдылығы.
Энтропиялардың өлшем бірліктері жылу сыйымдылықтың өлшем бірліктеріне сәйкс келеді.
Энтропия түсінігімен максималды жұмыс сияқты эксергия түсінігі байланысты, ол жұмыс осы қалыптан қоршаған ортамен тепе – теңдікке көшкен кезде жүйемен жасалынады.
Энтропияны пайдалану есептеуді және үрдістердің графикалық көрінісін жетілдіреді. Үрдістердің «температура – энтропия Т - S» немесе «энтальпия - энтропия I - 5» диаграммаларда құрылуы өте қарапайым, сондықтан да кең пайдаланылады.
«Энтропия» түсінігін түсінуде оның тек бір жұмысшы денеге қатысты екенінен қиыншылықтар туындайды.
Егер бір процесте Дq жүйесінің энергиясының жоғалуы болса, оларды былай анықтауға болады Дs = Дq/Т. Сәйкесінше теориялық үрдістерде энтропия өзгермейді: Дs = 0. Мұндай үрдістерді изоэнтропиялық немесе қайтатын деп атайды. Барлық шын үрдістер энтропияның өсуімен өтеді. Бұл мағынада олар қайтпайтын немесе толтырылмайтын шығындары бар ағынды деп аталады.
Суыту машиналарының жұмыс орындау үрдісі
Суыту машинасын пайдаланып суыту. Т˚ төменгі температураға ие суыту камерасының салқындатылған ауасынан жылутасығыш (хладагент) жылуды алып, Т жоғары температураға ие сыртқы ортаға оны береді. Суыту машанасында циркуляциялайтын хладагент кері айналмалы үрдіс немесе суыту циклын жасайды. Энергетикалық баланстан q сыртқы ортаға суыту машинасынан берілетін жылу салқындату машинасымен шығындалатын L механикалық жұмыс шамасына q 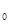 салқындату камерасынан алынатын жылудан көп екені көрінеді:
салқындату камерасынан алынатын жылудан көп екені көрінеді:
q = q 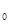 +L
+L
Суыту машинасының жұмысының тиімділігі суыту коэффициентімен бағаланады:
e = q 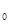 \L
\L
Мұндағы q 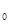 - салқындатылатын өнімнен шығатын жылу мөлшері немесе меншікті суықөнімділік, Дж/кг; L – меншікті механикалық жұмыс, Дж/кг.
- салқындатылатын өнімнен шығатын жылу мөлшері немесе меншікті суықөнімділік, Дж/кг; L – меншікті механикалық жұмыс, Дж/кг.
Суыту коффициенті суыту техникасына Карноның тік циклы бойынша жұмыс істейтін жылу машиналарының термикалық КПД ұқсас.
Әдебиет: 7,245-265 б.,2,67-85б;4,25- 346
Бақылау сұрақтары:
1Жылулық процестер қандай аппараттарда іске асады
2 Жылуөкізгіштік деген не
3 Күрделі жылулық процессінің түсінігі
4 Меншікті жылулық ағын түсінігі
5 Беткі пердесі бар жиделі жылуалмасу аппараттардың құрылысы
6Кожухқұбырлы жылуалмастырғыштардың құрылысы
7 Біркорпусты вакуумды бушықтыру қондырғыларының құрылысы
8 Конденсация үрдісі деген не
9 Мұздың және тұзды мұз ерітінділерінің еруі
10 Карноның тура және кері циклдары. Энтропия
Тақырып 6 Масса алмастыру үрдістері
Мақсаты: Тағам өнімдерінің өндірісінде пайдаланылатын масса алмастыру үрдістерінен мәлемет беру
Жоспары:
1 Масса алмастыру үрдістерінің жіктелуі
2 Ылғалдылықтың материалмен байланысу формалары
3 Кептіргіште жүретін кептірудің әдістері
4 Абсорбция және адсорбция
1 Бастапқы және соңғы өнімдер бір-бірімен заттармен алмасатын үрдістер масса алмастыру аппараттарында жүреді.
Масса алмастыру үрдістері үш негізгі белгілері бойынша жіктеледі: заттың агрегаттық жағдайы бойынша, фазалардың байланыстарының тәсілдері бойынша және олардың өзара әрекеттесу сипаты бойынша.
Үш мүмкін фазалардан екеуден алты түрлі қосылыстарды келтіруге болады; газ – сұйықтық, газ – қатты дене, сұйықтық – сұйықтық, сұйықтық – қатты дене, газ – газ, қатты дене – қатты дене. Екі соңғы қосылыстар масса алмасу аппараттарында пайдаланбайды.
Екі бөлек компоненттер бірдей газ тәрізді және сұйық фазаларда болса, олардың бөлінуі айдау (дистилляция) және ректификация үрдістерінде мүмкін.
Дистилляция (айдау) – фракция құрамы бойынша айырылатын сұйық қоспаларды бөлу.
Ректификация – бірнеше компоненттерден тұратын сұйық қоспаларды бір бірінен бөлу тәсілі. Ректификация сұйықтықтың көпретті булануы мен оның буының көпретті конденсациясына немесе кейінгі көпсатылы компоненттің конденсациясымен қоспаның бірретті булануы негізделген. Ректификацияны, мысалы, спирт өнеркәсібінде спиртаректификатты алу үшін қолданады. Егер судағы этил спиртінің ерітіндісінің бір бөлігі буланса, онда булы фазада спирт концентрациясы қалған сұйықтық пен алғашқы ерітіндіден үлкен болады. Егер одан кейін буды конденсацияласа, онда соңында спирт концентрациясы түрлі екі сұйықтық пайда болады. Осы үрдісті қайталау өте жоғары спирт концентрациясын қамтамасыз ете алады, яғни компоненттердің бөлінуінің өте жоғары дәрежесін қамтамасыз ете алады.
Бір – бірінде ерімейтін әр фазаларда компонент еріген жағдайда, компоненттің газ тірізді фазадан сұйық фазаға ауысу үрдісін абсорбция (көлемді жұту) деп атайды, ал кері үрдісті десорбция деп атайды. Мысалы, егер аммиактың ауамен қоспасын сумен байланысқа түсірсе, аммиактың бір бөлігі суға (су аммимакты абсорбциялайды) өтеді де, ауа біртіндеп одан тазарады. Кері үрдісте аммиактың сұйық ерітіндісін ауамен байланысқы түсірсе, ауаға аммиактың бір бөлігі өтіп – десорбция үрдісі болады.
Егер компоненттердің біреуі фазадан фазаға ауысса, фазалардың біреуінде сұйықтың (еріткіштің) мөлшері азаяды (көбейеді), мұндай үрдісті кептіру (ылғалдандыру) деп атайды. Мысалы, сүт ыстық ауамен байланысқы түссе, судың ауаға ауысуы болады. Мұнда сүт құрғатылып, ал ауа ылғалданады.
Қатты күйден газ тәрізді күйге сұйық фаза болмайтындай етіп ауысуды сублимация деп атайды. Газ бен қатты дене леп тесіктерде және қатты дененің беткі жағында болатын сұйықтықтың тек тасушылары болған жағдайда, жылу бергенде оның буға ауысуы кептіру немесе сублимациялық кептіру деп аталады. Көкөністерде мұндай жағдайда сұйық немесе бу тәрізді күйде ылғалды беткі жаққа береді де, содан кейін оны беткі жақтан жояды, яғни кептіру үрдіс болады. Кері үрдіс – қоспа компоненттерінің газтәрізді фазадан қатты фазаға ауысуын адсорбция (беткі жұту) үрдісі немесе ионды алмасу үрдісі деп атайды (38 бөлімді қараңдар). Адсорбция мысалы ретінде сулы будың бөліктерінің оның ауамен қоспасынан силикагель гранулаларына өтуін және оларды оның леп тесіктерінде ұстауын келтіруге болады; мұнда ауа құрғатылады.
Сұйықтық – сұйықтық жүйесінде бөлу кезінде байланысқа екі бір – біріне ерімейтін сұйықтықтар енгізіледі, олардың әрбіреуі бөлінетін компонентті түрлі дәрежеде ерітеді. Мысалы: этил спирті мен изобутанол қоспасының сумен байланысы кезінде олардың бөлінуі. Мұнда изобутанол белсенді түрде суға өтеді. Егер осыдан кейін изобутанолдың сулы ерітіндісін изобутанол мөлшері өте төмен оның этил спиртімен қоспасынан бөлсе (ал олар тұндырумен жақсы бөлінеді), онда үрдісті изобутанол мен спирттің таза сумен бөлінген қоспасының жаңа байланысы кезінде қайталауға болады да, және одан өте жоғары концентрациялы изобутанол алуға болады. Мұндай үрдісті сұйық экстракция деп атайды.
Өте таза заттарды фракционды кристаллизация үрдістерінде алады. Ерітіндіден түскен және бастапқы ерітіндімен салыстырғанда ластанатын компоненттерінің мөлшері аз кристалдар таза еріткіште ериді де, ерітіндіден қайта кристалданады. Ластанатын заттардың бір бөлігі қайта бөлінеді.
Егер екі фаза сұйықтық – қатты дене жүйесінде бейтарап заттар түрінде болады, ал бөлінетін компонент қатты денеден сұйықтыққа ауысады, бөліну үрдісін қатты дене – сұйықтық жүйесінде экстрагирлеу деп атайды. Осы үрдістің мысалы – шырынның қызылшадан суға (диффузионды шырынға) ауысуы.
Затты сұйық фазадан қатты фазаның бетіне жеткізудің кері үрдісі адсорбция мен ионды алмасу үрдістерінде болады, ал көлем – кері экстракцияның үрдістерінде. Адсорбция мысалы – қоспаларды адсорбциялайтын белсенді көмір басы арқылы өткізгенде қоспалардан суды тазарту. Кері экстракцияның мысалы ретінде ет немесе балық тұздауды келтіруге болады.
Фазалардың байланысу тәсілдері бойынша масса алмасу үрдістерін фазалық байланысы бар үрдістерге, мембрана арқылы байланысы мен фазалардың көрінетін (нақты) шектері жоқ үрдістерге бөледі. Егер фазалар арасында мембраналар орнатса, онда бөлу үрдісі мембранды технологиялар саласына жатқызылады (21 бөлімде қарастырылған).
Фазалардың өзара әрекеттесу сипаты бойынша масса алмасу үрдістері мен аппараттарын периодты және үзіліссіз болып бөлінеді. Одан басқа, үзіліссіз үрдістерде компоненттердің тікбағытты, керібағытты, қиылысқан және комбинирленген қозғалыстарын ұйымдастыруға болады. Үрдісті нақты ұйымдастыруына байланысты уақыт пен аппарат ұзындығы бойынша үрдісте қатысатын заттардың концентрацияларын түрлі өзгертуге болады. Олардың түрлілігі үрдістерді комбинирлеу жолымен ұлғаяды.
Масса алмастыру аппараттарының есептері
Масса алмасу аппараттарының инженерлік есептерін феноменологиялық тәуелділіктер пайдаланады.Олрада,үрдістің қозғалыс күші мен құбылыстың физикалық немесе химиялық мәніне терең енбей, оған түсетін әсерлер арасында байланыстың эмпирикалық коэффициенттерін кеңін қолданады. Масса алмасу үрдістерінің қозғалыс күші – концентрациялардың түрлілігі.
Инженерлік есеп компоненттердің материалды және энергетикалық баланстардың теңдеулерін құруда және де олардың негізінде басты элементтердің меншікті сипаттамалары белгілі болғанда, масса алмасу аппараттардың есептерін толтыруда қорытындыланады.
Ерітіндінің (қоспаның) концентрациясы. Ерітіндідегі (қоспадағы) берілген компоненттің қатысты мөлшері оның концентрациясы деп аталады. Ерітілген заттың үлкен концентрациясымен ерітінділер концентрирленген ал кіші концентрациямен – қосылған деп аталады.
Концентрацияны өрнектеудің келесі тәсілдері көп қолданылады:
-массалық – ерітінді массасының 100 бірлігінде еріген зат массасының бірліктерінің саны. Мысалы, 15% - тік натрий хлориді мен 85 г су бар ерітінді;
-көлемді мольдік – ерітіндінің бір көлемдік бірлігіндегі (1 дм 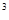 ) ерітілген заттың моль саны.
) ерітілген заттың моль саны.
-массалық мольдік – 1000 г еріткіштегі ерітілген заттың моль саны;
-қатысты мольдік (мольдік үлес) – ерітілетін заттың моль сандарының ерітіндідегі бүкіл заттардың жалпы моль санына қатынасы.
Масса алмасу үрдісі жүйеде тепе – тең концентрация орнатылғаннан кейін тоқтатылады.
Фазалардың тепе – теңдігі. Масса алмасу аппаратында үрдістердің тепе – теңдіктерінің негізгі шарты – фазаларының тепе – теңдігі. Заттар күйінің тепе – теңдіктен ауытқуы, мысалы термодинамикалық параметрлердің өзгеруі нәтижесінде, тепе – теңдікті қалпына келтірудің ауыспалы үрдісі жүреді (Ле Шателье принципы).
Тепе – теңдік қалпы кіріспеде қарастырылған Гиббс фазаларының ережесіне бағынады, оған сәйкес сыртқы факторларды тек температура мен қысым әсер ететін тең салмақты термодинамикалық жүйенің S бостандық дәрежесінің саны к компонентінің санынан ф фаза санын алып екіні қосқанға тең:
S = K – Ф + 2
Бостандық дәрежесінің саны, белгілі болғандай, - бұл тәуелсіз айнымалылардың (температура, қысым, концентрация) саны, олардың әр мәндерінде термодинамикалық тепе – теңдік болуы мүмкін. Мысалы, тек су буынан тұратын жүйеде (компонент саны К = 1, фазалар саны Ф = 1) S = 1 – 1 +2 = 2 болады. Осы жүйенің екі параметрі, мысалы температура мен қысым үлкен шектерде тепе – теңдікті бұзбай, яғни жаңа фазаны тудырмай өзгере алады. Егер осы жүйеде жаңа фаза пайда – сұйықтық пайда болса, онда фазалар саны Ф = 2 болады да, S = 1 – 2 + 2 = 1. Бұл жүйеде тепе – теңдік қалпында тек бір параметр өзгере алады, мысалы, температура. Қысым керек температураға сәйкес келетін деңгейде орнатылады. Бұл сұйықтықтан будың қосымша булануы салдарынан, не будың бір бөлігінің конденсациясы нәтижесінде болады. Мұндай жүйені ылғалды қаныққан бу деп атайды. Егер бұл жүйеде үшінші фаза - қатты дене пайда болса, онда Ф = 3, S = 0. Бұл жағдайда жүйе бостандықтан айырылады, яғни ол сулы бу жағдайынан диаграммасында үштік нүктеге сәйкес келетін критикалық параметрлер кезінде қысым мен температураның тек бір қатаң белгіленген мәнінде болуы мүмкін.
Масса берудің коэффициенті. Масса беру үрдісінде қозғалыс күші қызметін ағын ядросында және С фазаны бөлінуінің шегінде концентрация түрлілігі атқарады, ал жүйенің реакциясының қызметін орын ауыстыратын зат массасының ағыны атқарады. Олардың байланысы феноменалогиялық тәуелділікте мынадай түрде болады:
М = аС,
Мұндағы а – масса тұрақтысы(постоянная).
а- тұрақтысынан аппараттарды санау кезінде аппаратты сипаттайтын көбейткішті бөледі. Бұл F масса алмастырғыштың бетінің ауданы. Онда формула былай өзгереді:
M = вCF; вF = a
в- тұрақтысын масса берудің коэффициенті деп атайды.
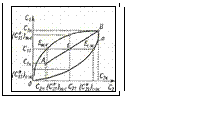
Сурет 19 - Массаалмасу аппараттарында жұмыс және тепе-теңдік сызықтар үрдісі
Тағам өнімдерін кептіру
Ылғалды ауаның қасиеттері
Ылғалды ауа деп құрғақ ауаның құрамындағы сулы бумен ылғал тамшыларымен және мұз кристалдарымен қоспасын атайды. Ол оның параметрлері қанығу шегіне қатысты қандай салаға жататынына байланысты қанықпаған, қаныққан және өте қаныққан болуы мүмкін.
Ауадағы ылғал құрамы 1 кг құрғақ ауадағы ылғал массасымен сипатталады да, х (кг/кг) немесе d (г/кг) арқылы өрнектеледі.
х пен d арасындағы қатынасы келесідей болады:
х = d 10 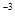
Дальтон заңына сәйкес ауаның жалпы қысымы р құрғақ ауа р 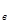 мен сулы будың р
мен сулы будың р 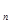 қысымдарының қосындысына тең:
қысымдарының қосындысына тең:
p = p 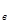 + r
+ r 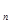
Ауада шектен мүмкін бу құрамымен сипатталатын қанығу жағдайына p 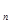 = r
= r 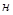 теңдігі келеді, мұндағы p
теңдігі келеді, мұндағы p 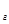 – қанығу жағдайына сәйкес келетін будың парциалды қысымы. p
– қанығу жағдайына сәйкес келетін будың парциалды қысымы. p 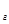 \r
\r 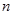 = Ф қатынасы қатысты ылғалдылық деп аталады. Рн қанығу жағдайындағы булардың парциалды қысымы температураның өсуімен ұлғаяды.
= Ф қатынасы қатысты ылғалдылық деп аталады. Рн қанығу жағдайындағы булардың парциалды қысымы температураның өсуімен ұлғаяды.
Ауа – су жүйесінде заттар екі фазада (газ тәрізді және сұйық) болады, ондағы компоненттер саны да екіге тең (ауа мен су), оны бостандық дәрежесінің саны да 2 тең (Гиббс фазаларының ережесі бойынша). Бұл онда тек екі параметр ғана өзгеретінін білдіреді. Олар әдетте t температура және ауаның салыстырмалы ылғалдылығы Ф болады. Жүйенің бүкіл қалған параметрлері тәуелді: меншікті жылу сыйымдылық С, меншікті энтальпия і, ылғал құрамы d, будың парциальды қысымы r 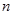 және тағы басқа ылғалды ауаның меншікті жылу сыйымдылығын мынандай тәуелділік пайдаланылады
және тағы басқа ылғалды ауаның меншікті жылу сыйымдылығын мынандай тәуелділік пайдаланылады
С = С 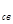 + хС
+ хС 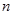
Мұндағы С 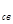 - құрғақ ауаның меншікті жылу сыйымдылығы, КДЖ/ (кг х К); С
- құрғақ ауаның меншікті жылу сыйымдылығы, КДЖ/ (кг х К); С 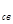 = 1,00 кДж/ (кг х К); С
= 1,00 кДж/ (кг х К); С 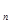 - сулы будың меншікті жылу сыйымдылығы, кДж/ (кг х К); С
- сулы будың меншікті жылу сыйымдылығы, кДж/ (кг х К); С 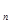 = 1,93 кДж/ (кг х К).
= 1,93 кДж/ (кг х К).
2 Ылғалдылық материалмен келесі тәсілдермен байланыса алады: химиялық (ионды, молекулярлы байланыс); физико – химиялық (адсорбция, осмотикалық, құрылыстық); механикалық (капилляр немесе сулы бетте).
Химиялық байланысқан, химиялық байланыстармен материалмен байланысқан ылғалдылықты тесумен немесе химиялық әдістермен жоюға болады. Оны жою үшін кептіру жарамайды. Басқа байланыс жағдайларында ылғалдылықты кептірумен жоюға болады.
Адсорбциялық байланысқан ылғал молекулалық күшті өрістердің колоидты құрылыстарының дамыған беткі жақтарында ұсталынады. Ол байланысқан су аталады. Және кристалды заттардың еруінде қатынаспайды. Адсорбция гидратацияның жылуын бөлумен бірге жүреді.
Осмотикалық ұсталынатын ылғал гелдың жоғары молекулалық бөліктерінде ұсталынады. Бөлшектердің жоғары молекулалық қабығы ішкіклеткалық ылғалдылықты ұстайтын жартылай өтетін бөгеттердің қасиеттеріне ие.
Егер ылғалдылық гель құрылысының ішіне оның құрылуы кезінде енсе, ол құрылысты деп аталады. Оған өсімдік ұлпаларының ылғалдылығы жатқызылады. Леп тесікті денелердің капиллярларында болатын ылғалдылық механикалық ұсталынатын, ал денелердің беткі жағындағысы – сулану ылғалдылығы деп аталады.
Материалдық ылғалдылық көрсеткіштері.
Тең салмақты ылғалдылық
Материалды ылғалдың болуын ылғалдылық деп атайды және құрғақ (Е) материал немесе ылғал массасынан (W) пайызбен (бірлік үлестерінде) бағалайды:
W = m 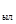 \ m; E = m
\ m; E = m 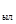 \ m - m
\ m - m 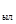
Мұндағы m 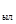 - ылғал массасы, кг; m – ылғалды материалдың массасы, кг.
- ылғал массасы, кг; m – ылғалды материалдың массасы, кг.
Егер ылғалды материалдың үстінде ылғалды ауа болса, онда уақыт өте келе олардың арасында тепе – теңдік орнап, фазалар арасындағы ылғалдылықтың ауысуы тоқтайды. Бұл жағдайдағы материалдың алғалдығы тең салмақты деп аталады.
Материалдың тең салмақты ылғалдылығы, %.
| Материал | Ауаның салыстырмалы ылғалдылығы, % | ||||||||
| Vlyica | 2,2 | 3,90 | 5,0 | 6,90 | 8,50 | 10,1 | 12,6 | 15,80 | 19,00 |
| Ақ нан | 1,0 | 2,00 | 3,1 | 4,60 | 6,50 | 8,50 | 11,4 | 13,90 | 18,90 |
| Макарон | 5,0 | 7,10 | 8,7 | 10,6 | 12,2 | 13,7 | 16,6 | 18,85 | 22,40 |
| Печенье | 2,1 | 2,80 | 3,3 | 3,50 | 5,00 | 6,50 | 8,30 | 10,90 | 14,90 |
| Крахмал | 2,2 | 3,80 | 5,2 | 6,40 | 7,40 | 8,30 | 9,20 | 10,60 | 12,70 |
| Бидай | - | - | 9,3 | - | - | 13,0 | - | - | 24,00 |
| Қара бидай | |||||||||
| 6,0 | 8,40 | 9,5 | 12,0 | 12,5 | 14,0 | 16,0 | 19,50 | 26,00 | |
| Сұлы | 4,6 | 7,00 | 8,6 | 10,0 | 11,6 | 13,6 | 15,0 | 18,00 | 22,50 |
| Арпа | 6,0 | 8,50 | 9,6 | 10,6 | 12,0 | 14,0 | 16,0 | 20,00 | 29,00 |
Ол қоршаған ортада және керек температурада сулы будың парциальды қысымының функциясы болып саналады. Тең салмақты ылғалдылықтың мәндерінің қатарын ауада будың түрлі парциальді қысымдарында ылғал сорбциясының изотермасы деп атайды. Көптеген материалдар үшін тең салмақты ылғалдылық температураға тәуелді емес. Тағам материалдарының бір қатарының тең салмақты ылғалдылығының мәндері кестеде келтірілген.
Кептіру үрдісі
Кептіру – жылулық және диффузионды құбылыстарды пайдаланып ылғалды жоюға негізделген біртекті немесе біртексіз жүйелерді бөлу үрдісі (немесе тәсіл). Материалдан шығатын ылғал кептіру агентіне беріліп, сонымен бірге кептіргіштің жұмыс аумағынан жойылады. Онымен кептіру ылғалды жоюдың басқа тәсілдерінен – механикалық (престе немесе центрифугада сығу) және су алатын құралдарды қолдануға негізделген физика – химиялық тәсілдерінен ерекшеленеді.
Кептіруге қатты материалдар кристаллды (қант, тұз ж.т.б.); коллоидты – дисперсті (эластикалық және нәзік гельдермен капиллярлы леп тесікті денелер) және де сұйықтар: кристаллоид ерітінділері мен каллоидты ерітінділер ұшырауы мүмкін. Эластикалық гельдерге желатин, агар – агар, престелген ұн қамыры жатқызылады. Бұл денелер кептірілген күйінде эластикалық күйін сақтап сығылады. Нәзік гельдерге ағаш көмірін, керамикалық материалдарды жатқызады. Бұл денелер кептіруден кейін нәзік болады. Капиллярлы – лептесікті денелерге торф, ағаш, былғару, астық, нан ж.т.б. жатқызылады.
/Қозғалыстағы күш ретінде кептірудің феноменологиялық көрсетуі бойынша фактілік және жүйенің тең жағдайы ылғал концентрациясының түрлілігін қабылдайды.Оның фактілік концентарциясы кептіру үрдісінде өзгереді, салмағының теңдігі өнімнің түрі ретінде анықталынады, дәл осылай қоршаған ортаның ылғалдығы да анықталынады.
Кептіру үрдісі кептіру агентінің қыздыруын қосады және кептіргіш камерарда кеуіп жатқан материалды ұстаумен көрсетілінеді.
Конвективті кептіруде ылғал материалдың ортасынан материалдың бет жағына ауысады, осылайша ол кептіргіш агентпен жойылады. Бұл диффузионды үрдіс; оның қозғалыс күші ретінде ылғал концентрациясының dc/dx градиенті болды.Сондықтан да ылғал концентрациясының әсерінен ылғал алмастырғыш (кг/с) үшін келесі феноменологиялық көрсетулерді жазуға болады:
Mw=k1F dc/dx
К- тұрақты; F- материал бетінің ауданы, м2.
Метериалдың пораларындағы ылғал және осматикалы ұсталынып тұрған ылғал материалдың бетінде сұйық түрінде көшеді, ал адцорбционды байланыс –бу ретінде болады.
Материалда ылғал диффузиясының күрделенетін себебі, жылудың әсерінен ылғал жылу ағынының бағытымен ауысуынан болады. Қорытындысында осы күрделі үрдісті термоылғалөткізгіш деп атайды. Температура градиентінің әсерінен ылғалдың ауысуын термодиффузия деп атайды.Бұл жоғарғы температурамен және «защемленного» ауаның әсерімен бетіткі жағының тартылуының кемуімен пайда болады.
Берілген себептерге шартталған жалпы массалық ылғал алмастырғыш (кг/с) dt/dx температура градиенті бойынша mt=-k2F, dt/dx –ке тәуелді болуы мүмкін,
мұнда К2- тұрақты.
Екі себетін әсерінен кеуіп жатқан гельдегі ылғал көлемінің суммасы (кг/с), мынау суммаға тең болады: (өзінің белгілерінен):
m=mw+mt
Кептіру үрдісі екі кезенге бөлінеді:
-ылғалдың дене терендігінен бетіне (сыртына) дейін ауысу;
-будың қоршаған ауада ауысуы.
Осылардың бірінші кезеңі қарастырылған. Ылғалдың жойылуы дене ішінде де, дәл солай сыртында да өтеді. Екі жағдайда да жойылған ылғалдың келесі қозғалсы беткі жағынан жүреді.
Материалдың бетінде материал ылғалымен тең болатын жеңіл –булы қабат пайда болады; бу материал температура кезінде қанық болады.
Диффузия күшінің материал бетінен қоршаған ортаға қозғалысы –шектік қабаттағы PH сулы будың түрлі парциалды қысымы р және қоршаған ортада Рв.
Материалдың шектік қабатындағы будың парциалды қысымын қанық будың қысымы деп атайды.
Диффундирленетін будың (кг/с) массалық шығынының m феноменологиялық тәуелділігі осы үш параметрлерден тұрады:
m=B1(Рн~Рв) F1
Мұнда В1- тұрақты.
Ылғал дене бетінен жойылу үшін соңғы көрсеткіш Дальтон заңы деп аталады.
Бұл ылғалдың шығыны ішкі жағынан сыртқы бетіне дейін жеткізілген ылғал ағынына тең болу керек. Уақыт ішінде материал ылғалдығының өзгеруі қисық кептіру деп атайды.
Құрғатудың алдында затты қыздырады кейін ылғалдың жойылу жылдамдығы нөлден кейбір тұрақты шамаға дейін жоғарлайды.
Тұрақты кептіру жылдамдығы кезенінде, материалмен механикалық байланысқан (сырт жағынан және копилярлы) ылғал жойылады.
Төмен бағытталған кептіру жылдамдығы кезінде материалдағы ылғалдың жойылу жылдамдығы азаяды. Осы кезенде материалмен тым тығыз байланысқан, сонымен қатар адсорбционды байланысқан ылғал жойылады.
3 Жалпы мағұлмат. Кептіру әдістерін ұйым үрдісінен материалдан ылғалды сіңіруден ерекшеленіледі және барлық кептіру спецификасын анықтайтын бір немесе бірнеше үрдістердің қолданылуымен сипатталынады. Кеңінен таралған келесі кептіру әдістері: табиғи; конвективті (амалсыз ауа қозғалысы кезінде кептірілетін материалға қатысты); шашыраңқы; кондуктивті (жоғарғы температуралы газды ортада кесілген өнімнің ұсақ тамшыларының кебуі);вальцовты (металды бетіндегі жоғарғы байланысты өнімдердің кебуі); вакуумды немесе сублимационды; экспломазионды; қайнап жатқан үгітілімді өнімнің қабатында; аэрафатонды (пневматикалық); терморадиационды көпірген өнімді алумен және т.б.
Табиғи кептіру. Мұндай кептіруді қолайлы климаттық шарттарда қолданады. Кепкен өнімді арнайы бастун щиталарға салады немесе ашық ауада торға (сеткаға) салады.
Конвективті кептіру. Мұнда кептірілген өнімнің қабатына қатысты қызған ауаның амалсыз қозғалысы қолданылады. Амалсыз (принудительная) конвекцияның жылдамдығы 1...5 м/с.
Конвективті кептірудің басты кезенінде кептіріліп жатқан материал бетінде бос ылғал болғанда, материалдың температурасы оған аз тәуелді болады. Осындай сәйкес шарттар сулы термометрдің температурасына жақын болады. Сондықтан да кептірудің басты кезенінде кептіруді тездететіндіктен кептіргіште температура жоғары болуы мүмкін. Кептірудің басында әдетте температураны 90...1200С-қа дейін жоғарлатады; шашыраңқы кептіргіштерде -140...2000С –қа дейін болады.
Келесі кептіру кезенде температура күйіп кетуден немесе басқа да өнімнің сапасының нашарлауына алып келмейтін белгілі бір белгіге дейін кему керек.Әдетте бұл температура кептірілген материалға байланысты 60...450 С-ты құрайды.
Кептірудің алдындағы сілтілі сульфитті ертіндісімен өндеу, осы температураның жоғарлауына мүмкіндік береді. Өнімді сульфиттеу кептіру кезіндегі побурения (лайлану,қопарылу) мүмкіндігін кемітеді. Дәл осылай аскорбинді немесе лимон қышқылымен өндеуге және шығыс өнімдерді бланжирлеуге болады. Кейде осы кезенде де бірнеше секундқа (кейде 10 секундқа дейін) еш қолайсыз жағдайлар болмаса, температураның жоғарлауы 100...1300С-қа дейін болады.
Материалдың жанып кетуін болдырмау үшін кептіруді екі кезенде өелізеді: негізгі кептіру кезеңі және соңына дейін кептіру. Негізгі кептіру кезенінде материал ылғалдығы 10...15 % -ға дейін кемиді. Сонымен қатар соңына дейін кептіру кезеңінде кептіріліп жатқан материалдың барлық көлемінде ылғалдық тегістеледі. Соңына дейін кептіру құрылғыларында ауаның қозғалу жылдамдығы 1м/с –ке дейін болса, ауа температурасы 40...600С –тан аспайды. Әдетте соңына дейін кептірудің кептіру ұзақтығы негізгі кептіруге қарағанда артығырақ болады.
Кептірілген материалдарда ылғалдың жойылуы беттегі ұшқыш заттың шығаруына әкеп соғады. Осының салдарынан өнім өзінің дәмін және хош иісін жоғалтып, және осындай шығын көрінетіндей жағдайға келуі мүмкін. Бұл заттарды ұстап тұру және кепкен өнімге қайта алып келу үлкен мәселе.
Кондуктивті кептіру. Жылу материалдың өніммен байланысы кезінде беріледі.
Шашыраңқы кептіру. Шашыраған сұйық өнімнің ұсақ тамшылары жоғарғы температуралы ортада тез жоғалады. Шашыраған өнім үлкен кептіру ауданға түсіп интенсивті жылу бергіштігін қамтамасыздандырады. Кептірудің ұзақтығы (1...10 с) аспайды. Шашыраңқы кептіргіште жылу бергіштіктің екі түрінің біреуі белсенді болады –конвекция және радиация, бірақта жалпы жағдайда екуі қатар жүреді.
Шашыраңқы кептіргішті сүттен, жұмыртқадан, шырындардан (сок), гидрализденген крахмалдан, қызылшаның сұйықтығынан, сәбіздің шырынынан және т.б.-дан ұнтақты өнімді өндеу үшін қолданады. Дайын өнімді алу үшін (қайнаған немесе теңіз тұзын сияқты) кептіру кезінде олардың хош иісін сақтауға талап етілмеген кезде қарапайым немесе әмбебап кептіргіші де құрылуы мүмкін (мысалы, кептіру кезінде өнім күйіп кетпеу үшінү, құрғақ сүтті өндіру кезінде)
Білікті кептіру. Кеуіп жатқан өнімнің жұқа қабаты цилиндрлі сәл күйген валдың бетіне «жағылады». Сұйық қабат 40...60 с ішінде кебеді, кейін оның жұқа кепкен түйіршіктері пышақпен алынады.
Өнімдерді көпіру арқылы кептіру. Көпір көкіністі және жемісті материалдарды конвективті ауа ағынындағы перефирленген металды табаларда (лист) кептіреді. Инертті газдың атмосферасында көпіру үшін өнімге миксердағы көпіретін тұңбаларды қосады.
Вакуумды кептіру. Үрдіс кеуіп жатқан материалдың температурасын төмендетуге мүмкіндік беретін төменгі қысым кезінде жүреді.
Сублимационды кептіру. Төменгі температурада витаминдер және бояғыштар бұзылмайтындықтан сублимациялы кептіру кезінде алынатын өнім жоғары сапамен қамтамасыздандырылады. Кепкен материал өзінің бастапқы пішінін сақтайды, сонымен қатар (жиі) –балауса (жаңа) өнімге деген көптеген хош иістер сақталынады.
Сублимация –судың қатты күінен, сұйықтықтан өтіп-су фазасын түземей,тура бу күйіне көшеді. Бұл кептіргіштегі төменгі қысым болғанда болуы мүмкін. Кептіру температурасы кезінде ондағы қалған қысым қанық будың қысымынан төмен болу керек. Бұндай жағдайда судың қайнау температурасы қатты кептірілген өнімнің температурасына қарағанда төмен болады. Табиғи түрде қатты өнімнен (мұздан) алынатын судың молекуласы бірден булы күйге ауысады.
Егер де кептірілетін өнімді кептіргіштің поддонына салсақ, мұздың сұйықтыққа көшуі кезіндегі пайда болатын су бірден қайнайды және бу түрінде жойылады. Бұл үрдісті де сублимация деп атайды.
Эксплозионды, немесе жарылғыш кептіру. Сонымен қатар кептіру түрінде жылулық шоктың пайда болуы қолданылады. Бұл оның толық көлемінде судың қайнауында қотындалынады, нәтижесінде қоршаған ортада бірден қысым төмендейді. Сонымен қатар су көпірілетін метериалда және қайнау температурасына жақын температураға дейін қыздырылған, сыртқы қысымның төмендеуінен тым қызған және қайнаған болады.Нәтижесінде материалдың ішкі құрлымы бұзылады және көпірген сияқты (жеңіл ауалы) болады. Мұндай материал жеңіл кептіріледі. Эксплозия сыртқы қысымның атмосфералыға көшу кезінде мүмкін, (сонымен қатар матетиалдың алғашқы температурасы 1000С-тан асады), дәл осылай атмосфералы қысымнан вакуумды түріне көшу кезінде де болады. Екінші жағдайда бұл үрдіс тым төмен температура кезінде жүреді.
Қайнап жатқан қабаттағы және аэрофатонды (пневматикалы) кептіру. Осы екі кептірудің түрі төменнен жоғары қарай үгітілетін материал қабатынын арасына ауа жібергенде жүреді. Бұл екі жағдайдағы ең негізгісі біреуі ғана болады, бірақ пневматикалы кептіруде ауа жылдамдығы жоғары және кептірілетін материал бөліктерінің арасы үлкендеу болады. Қайнап жатқан қабат ауа ағынының 1...5 м/с жылдамдығында жүреді; аэрафотонды кептіру кезінде оның жылдамдығы 12...14 м/с –ке дейін өседі.
Инфрақызыл кептіру және жоғарғы жиіліктегі тоқ өрісі (поле) аланындағы кептіру. Басқа кептіру түрінен бұл кептіру түрі жылудың сәйке әдісімен ерекшеленеді. Кептіру үрдісінің ұйымы кез –келген болу мүмкін (жоғарыда көрсетілген әдістердің арасынан). Бұндай қыздыру кезінде диффузия үрдістері және ылғалдың термодиффузиясы материалдарды кептіру үрдісі кезінде бір жаққа бағытталған, бұл кептіруді 10 есе жылдамдатады. Инфрақызыл қыздыру кептіргіштерде әдетте жұқа өнімдерді кептіреді (печенье, бетіндегі бояу қабатын), мұнда сәулелендіру жуандығының ортасына дейін өтеді.
4 Cорбция деп (латын тілінен sorbeo –сіңіру) қандайда бір затты (сорбтивті) басқа бір затпен (сорбитпен) сіңірудің кез –келген үрдісін атайды.Механизіміне байланысты сіңіруді адцорбционды, абсорбционды, хемосорбционды және копилярлы конденсациялы деп айырады. Сорбционды үрдістерді сорбцияны қолданып бірдейлі және бірдей емес жүйеден бөлу үшін қолданады.
Абсорбция – барлық сорбинт көлеміндегі бір заттың басқа затпен сіңірілуі. Абсорбция мысал ретінде газдың сұйықтықта еруін айтады. Бұндай үрдісте сіңірілетін затты –абсорбат дейді, ал сіңіретіндерді –абсорбент дейді.
Адсорбция – фазаның бөлу шегінде зат концентарциясының өзгеруі байқалады. Бұл кез –келегн фаза арасының бетінде жүреді және де кез –келген затта адсорбилене алады. Адсорбционды теңдік, демек шектік қабаттың және шектік фазаның арасындағы заттың тең орналасуы динамикалы болады және тез құрылады. Бұндай үрдісте сіңіретін затты –адсорбат,сіңірілетінді –адсорбент деп атайды.
Хемосорбция- химиялық реакциямен жүретін затты сіңіру.
Копилярлы конденсация –микропоралы сорбенттердегі будың сұйылуы.
Бұл сұйықтықтың майысқан менискісінде будың қысымы бірдей температурада сұйықтықтың жазық беткі жағында қаңық будың қысымына қарғанда олармен малынатын тар копилярлларда аз.
Нәтижесінде газ молекуласынның сұйық күйге көшу шамасы өседі және де газдың көлемі азаяды. Осының салдарынан ішке майысқан минискада газдың конденсациясының температурасы қоршған ортаға қарағанда жоғары болады. Сондықтан да газды ортадағы температура конденсация температурасына жақын, бірақ жоғары болмаса, лиофильді материалдан микропоралы сорбиттері енггізілгенмен газдың конденсациясының басталуының басы болу мүмкін. Мұндай үрдіс газдың адсорбциясы сияқты лиофильді микропоралы сорбиттермен сәйкес температуралы режимдерді ұстап қалумен түсіндіріледі.
Кез келеген сорбционды үрдіс фазалар байланысының шегінен кейін басталады, демек адсорбциядан. Шектік сұйық, газ тәрізді немесе қатты фазалар шегі болуы мүмкін.
Десорбция - сорбаттың сорбенттен бөлінуі. Сорбционды үрдіске сіңірудің алынуы (селективті) қасиетті болады. Осындай маңызды қасиет сорбентті таңдау жолымен заттарды бөлу үшін маңызды мүмкіндік тудырады. Сорбционды үрдістердің ағыны кезінде жылулық бөлінеді (кейде сіңіріледі), ал тұйық жүйелерде қысым өзгереді. Және де осыған байланысты сорбциялардың үрдістері, ережеге сай температураның төмендеуімен және қысымның жоғарлауымен жылдамдатылады.
 2015-05-05
2015-05-05 1727
1727








