По совремешшм представлениям (М.М. Илькович, Л.Н. Новикова, 1998; М.М. Иль кович, 2000) морфологические изменения в паренхиме легкого при ИФА можно условно представить в виде трех взаимосвязанных стадий (фаз):
. интерстициалыюго (в меньшей степени альвеолярного) отека;
. интерстициального воспаления (альвеолита);
• интерстициального фиброза.
На рисунке 8.2 схематично изображена последовательность основных морфологических изменений, возникающих на начальном этапе формирования ИФА. Под действием неизвестного этиологического фактора на поверхности альвеолоцитов II типа и колла-геиовых волокнах интерстициальиой ткани происходит экспрессия аутоантигенов; протеины, входящие в состав мембран альвеолоцитов, и коллаген, приобретая новые 
антигенные свойства, распознаются иммунной системой как чужеродные белки, к которым вырабатываются аутоантитела.
Образующиеся иммунные комплексы (аутоантигеи + аутоантитело) инициирую! иммунный воспалительный процесс, затрагивающий интерстициальную ткань и алЪВФ1 лоциты. Так, под действием иммунных комплексов происходит активация альвеолярныл макрофагов, которые вместе с тучными клетками продуцируют медиаторы воспален ни (интерлейкины, лейкотриены, простаглапдииы). При этом резко возрастает нроиицае мость капилляров, что способствует возникновению отека интерстициалыюй ткани и альвеол.
Кроме того, под влиянием иптерлейкииов и других хемотаксических агентов, выра батываемых альвеолярными макрофагами, нейтрофилы и другие клеточные элемент крови инфильтрируют интерстициальную ткань легких. Известно, что активированные нейтрофилы явлются в организме главным источником протеаз, свободных радикалов и других веществ, повреждающих различные ткани. Кроме того, протеолитическои активностью обладают эозинофилы, моноциты, альвеолярные макрофага. Под денет ни ем протеаз (коллагеназ), возросшую во много раз активность которых аптппротсазпьк системы легочной ткани сбалансировать не в состоянии, собственный коллаген легочпог ткани разрушается.
Расщепление коллагена протеазами, высвобождающимися при гибели Нейтрофи лов, сопровождается усиленным ресинтезом патологического коллагена. Важную рои в этом процессе играют альвеолярные макрофаги, моноциты, нейтрофилы и фиброб ласты. Так, активированные альвеолярные макрофаги выделяют фибронектин и дру| и< факторы роста, под влиянием которых происходит пролиферация фибробласпич и других мезепхимальпых клеток, которые синтезируют в большом количестве патологи ческий коллаген, инициируя и поддерживая прогрессирующий фиброз интершщиоль ной ткани. Таким образом, на определенной стадии развития заболевания теряете; контроль за синтезом и распадом соединительной ткани и происходит дезоргапиаапи-последней.
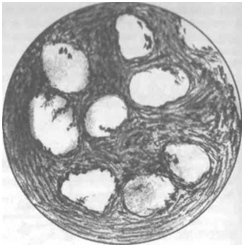 |
ис. 8.3. Нарушение архитектоники легочной сани при ИФА. Заметно разрастание эединительной ткани, утолщение и уплотнение ожальвеолярных перегородок, облитерация львеол и капилляров
Одновременно под действием медиаторов воспаления, супероксидиых радикалов резко возросшей цитотоксичности Т-лимфоцитов происходит повреждение альвеоляр-ого эпителия, в первую очередь альвеолоцитов II типа, и, соответственно, снижение ыработки и изменению качественного состава сурфактанта, что способствует спаде-ию альвеол. Альвеолярный эпителий метаплазируется в кубический эпителий. Разрас-ающаяся соединительная ткань сдавливает альвеолы и капилляры, в результате чего емко нарушается архитектоника легочной ткани (рис. 8.3).
Запомните: В результате выраженной дезорганизации клеток легочной паренхимы при ИФА, легких значительно разрастается соединительная ткань, что приводит к утолщению и уплотне-ию межольвеолярных перегородок, облитерации альвеол и капилляров (М.М. Илькович).
В результате разрастания соединительной ткани резко нарушается архитектоника егочной ткани: альвеолярные пространства уменьшаются почти в 2 раза, просвет ка-илляров сужен за счет склероза и гиперплазии интимы, альвеолярно-капиллярные ембраны утолщены более чем в 2 раза.
В терминальной стадии заболевания формируется картина «сотового легкого», следствие образования в легочной ткани воздушных микрокист, в просвете которых южно обнаружить белковые массы.
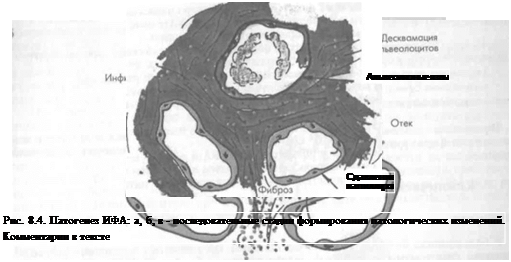
В первой стадии заболевания повышается проницаемость капилляров, что сопровож-ается отеком межальвеолярпых перегородок и появлением внутри просвета альвеол се-озио-фибринозного экссудата. В интерстициалыюй ткани и в просвете альвеол на этой гадин развития болезни определяется небольшое количество клеточных элементов рис. 8.4, а).
Вторая стадия характеризуется развернутой морфологической картиной воспаления — пьвеолита. В интерстициалыюй стадии значительно увеличивается число клеточных цементов — нейтрофилов, макрофагов, лимфоцитов, плазматических клеток, гистиоци-он, фибробластов и т.п. Происходит десквамация альвеолярного эпителия и оголяется азальиая мембрана — образуются так называемые «альвеолярные язвы» (рис. 8.4, б), пачителыю увеличивается в межальвеолярпых перегородках количество фибробластов.
Третья стадия характеризуется значительным разрастанием коллагеиовых волокон, голщепием межальвеолярпых перегородок, облитерацией легочных сосудов и альвеол рис. 8.4, в).
Следует добавить, что в настоящее время различают две клинико-морфологические юрмы ИФА:
• муральиую — с преимущественным поражением интерстициалыюй ткани легкого;
• десквамативную форму — с преимущественным поражением альвеол.
Ирм муралытй форме ИФА в легких происходят более выраженные морфологические изменения в виде значительного фиброза иитерстнциалыюй ткани, сужение капилляров И самих альвеол. В терминальной стадии формируется картина «сотового легкого*.
 2015-05-06
2015-05-06 280
280







